Druckversion des ausgewählten Themas
- zurück zum Originalformat -
SALVIA-COMMUNITY.net _ Zauberpilze _ Mal Wieder Anfängerfragen-pilzgrow
Geschrieben von: Herr von Böde Aug 20 2015, 12:30
Hallo,
bin neu hier im Forum. Lese schon eine ganze Weile mit und hab mich jetzt auch registriert.
Seit Anfang Juli läuft nun die eigene kleine Pilzzucht mit 3 Cubensis Strains:
G.Teacher, Albino A+ und PF-orig.
Ich hab mich vor Jahren schonmal ein wenig in die Pilzzucht eingelesen, war aber nie dazu gekommen mal zu starten.
Einen groben Plan hatte ich also schonmal.
Jetzt in der Praxis treten natürlich doch noch ein paar Fragen auf und hoffe hier ein paar Tipps und Anregungen abstauben zu können, vielen Dank schonmal :-)
Mein Plan sah vor erstmal auf Nummer sicher zu gehen um an Myzel zu kommen welches dann weiter selektiert werden kann und natürlich um überhaupt ertmal Ergebnisse zu haben.
Darum also erstmal jeweils einen Teil der Sporenlösungen aus den Durchstechflaschen für PF-Kuchen verwendet: 3x 125ml Mikrofilterdosen mit G.Teacher und jeweils 1x 430 ml Sturtzglas für die beiden andern Strains.
Soweit hat auch alles schonmal bestens funktioniert, die 3 Golden T. Kuchen setzen seit gestern den 4 bzw. 3 Flush an und die beiden grrößeren Kuchen sind seit 4 Tagen gestürtzt und in der Fruchtungsbox.
erster Flush des schnellsten 125ml Golden T. Kuchens:
die Cakes, am 19.08:
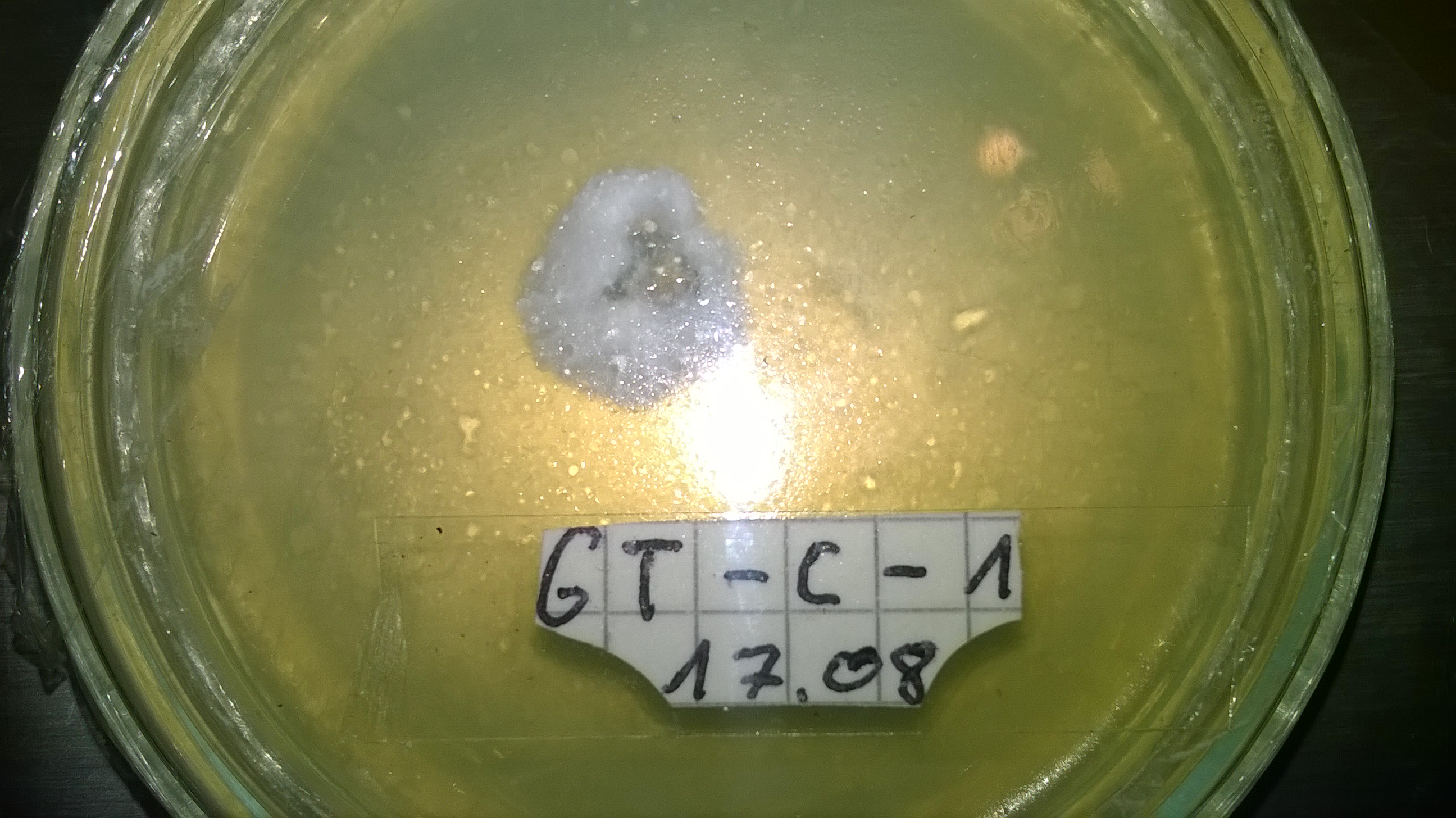
Ich habe beim Stürtzen bzw. bei den Golden T.-Dosen schon als sie gut zur Hälfte durchwachsen waren mit einer Nadel von verschiedenen Stellen der Kuchen Myzel entnommen und auf Petries verpflanzt (KDA), Ziel ist ja ein schnell wachsendes und gut fruchtendes Myzel zu selektieren um dann mit der Casing-Tek weiterzumachen.
Auch das ist im ersten Schritt gut verlaufen, hatte wenige Kontis und tatsächlich auch ein schnell wachsendes Myzel (eine Petrie -80x15mm- war innerhalb einer Woche komplett bewachsen).
Beim weiteren Selektieren bzw. Beimpfen von Roggensubstrat in Gläsern bzw. Mikrofilterbags gab es dann plötzlich Hefeattacken (Petries und Substrate riechen stark nach Wein)und abgesehen von diesem:
gutes Golden T. Myzel (zweite Üerimpfung), die Halos sind keine Kontis: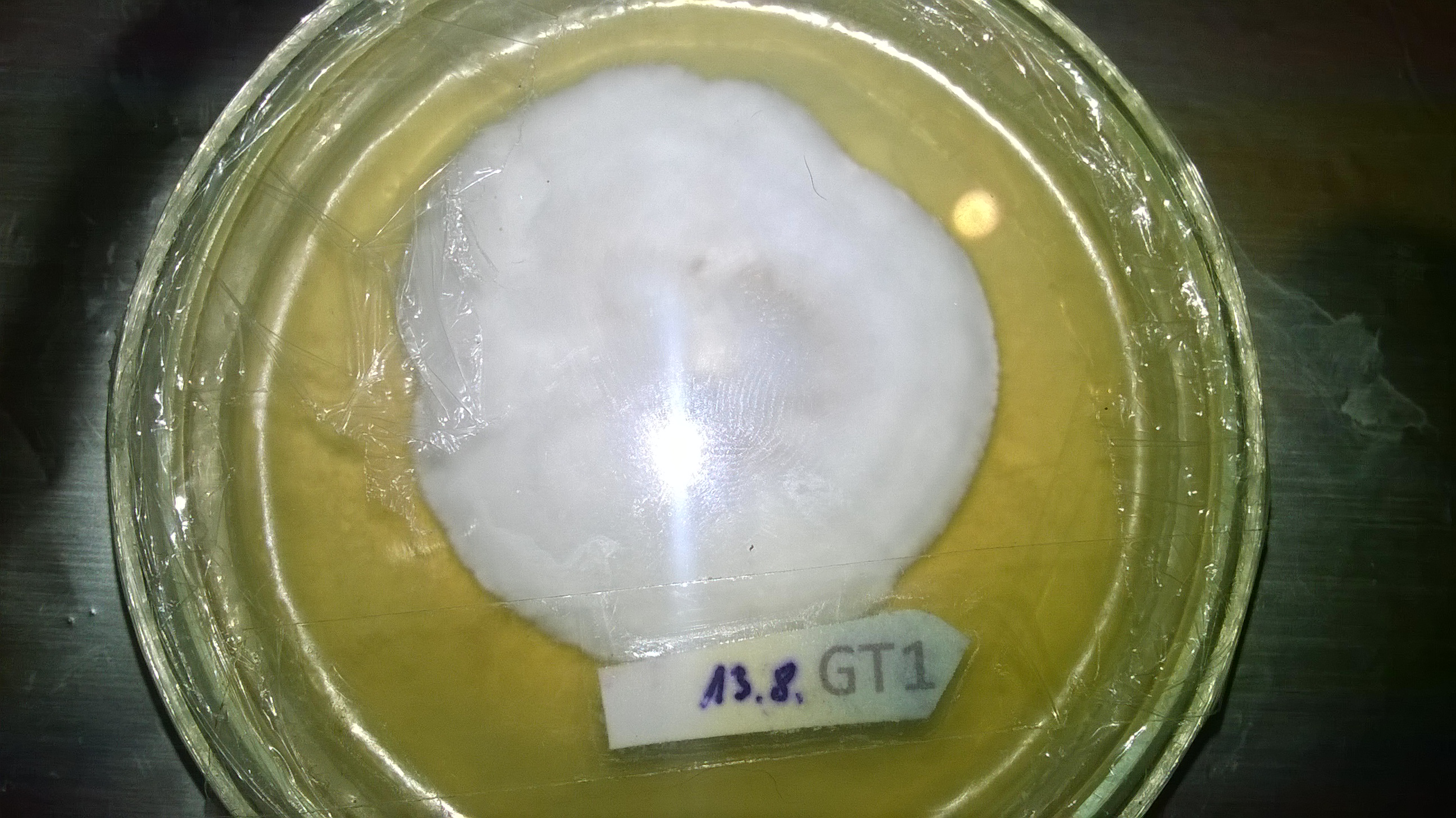
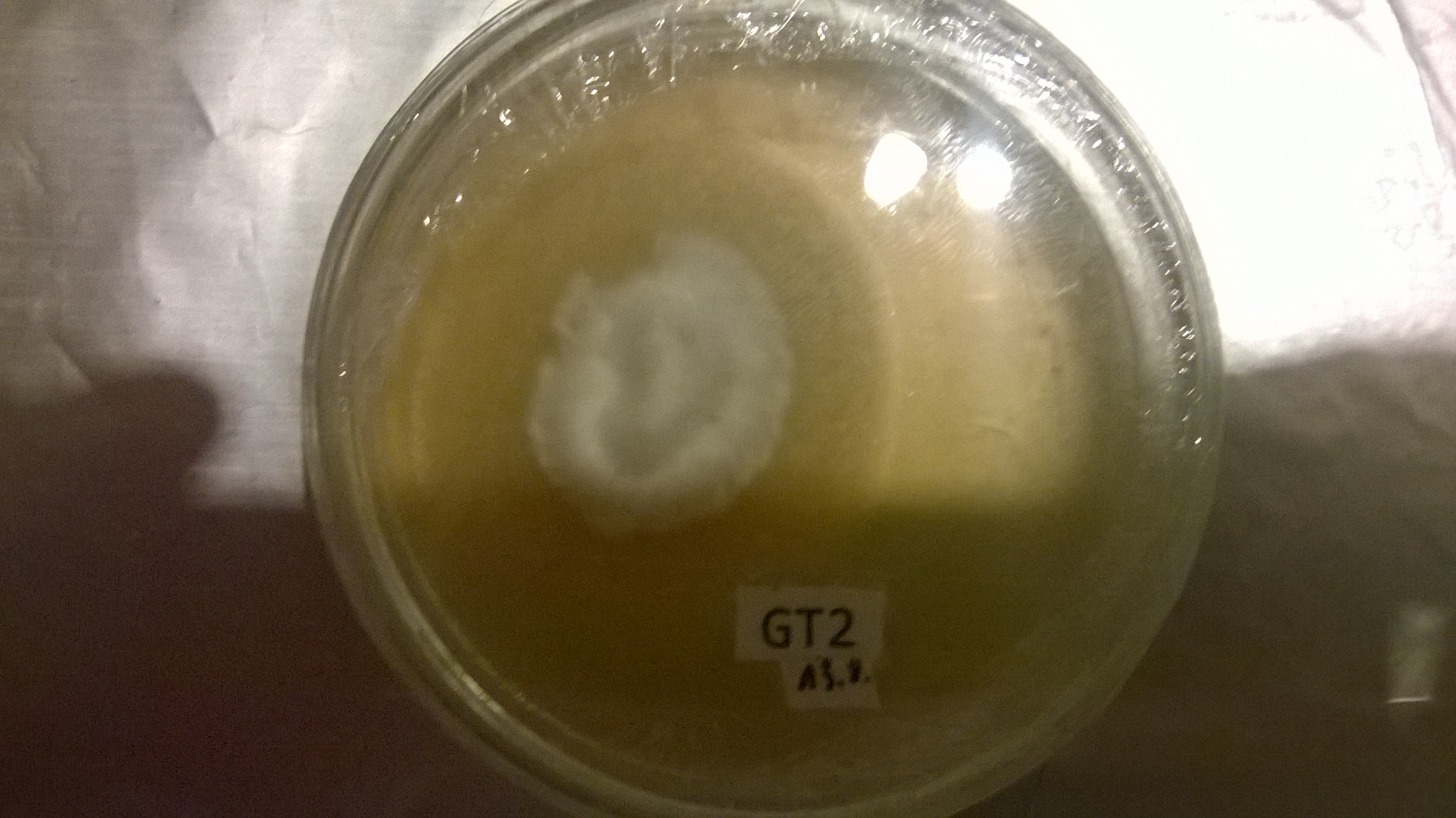

war dann alles verdorben:
Kontis: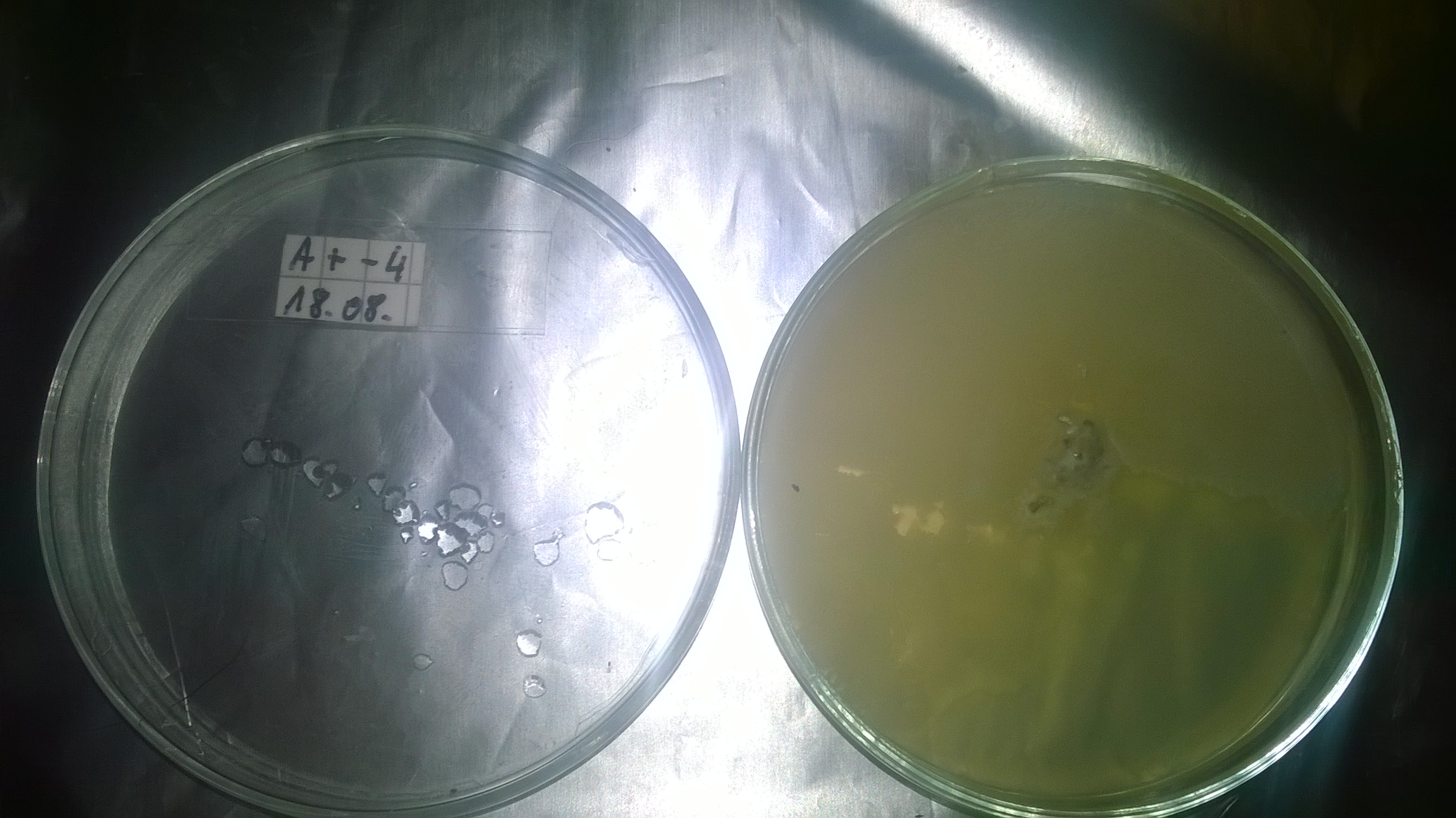
Das bereits selektierte gut wachsende Myzel ging dabei verloren(die Möglichkeit es aus einem der Kuchen wieder herauszubekommen besteht natürlich weiterhin, es dürfte ja noch da sein).
Es gibt auch noch weiteres gesundes Myzel auf Agar aber ich traue mich nicht so recht die Petries zu öffnen bevor ich die Fehlerquellen nicht erkannt und abgestellt habe.
Neuere Petries die hoffentlich kontifrei bleiben: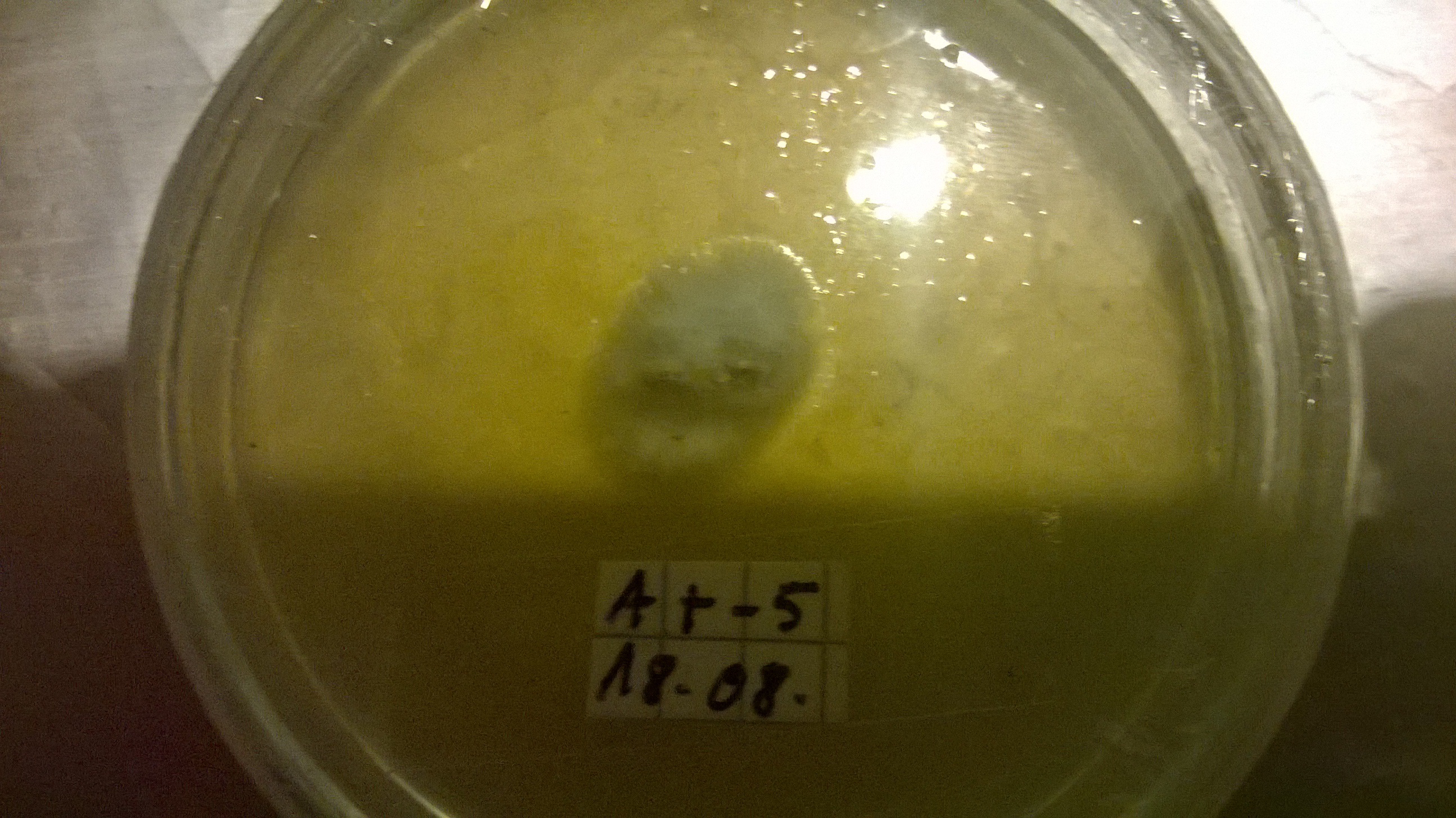

An dieser Stelle zwei weitere Fragen zu Klonen von Fruchtkörpern:
hab bereits versucht das Fleisch eines Hutes zu bekommen, jedoch blaut das sofort extrem und stirbt auf dem Agar, es findet kein Wachstum statt.
Macht es einen Unterschied wenn ich versuche aus dem Stiel zu Klonen?
Ziel ist ja eine einzige Genetik zu bekommen. Ich hab bereits gelesen, das selbst der Fruchtkörper aus unterschiedlichen Myzelien bestehn kann, wie groß ist die Wahrscheinlichkeit tatsächlich einen solchen "multigenetischen" Fruchtkörper
zu erwischen ? Ist die Wahrscheinlichkeit höher wirklich nur einen Genstamm zu erwischen wenn ich nur aus dem Hut klone? Wenn ich Myzel wirklich aus dem Inneren des Stamms nehme (ich könnte einfach größere Stücke entnehem, was die Chance auf weiterwachsende Zellen erhöht) und sicher gehe kein Myzel zu erwischen das evtl. bauschig am Stamm wächst, habe ich dann eine gute Chance auf isolierte Genetik?
Zur Überimpfung benutze ich eine Glovebox (15l transparente Reval Box, mit Frischhaltefolie abgedeckt die mit Paketklebeband von aussen stramm fixiert wird.
Als Desinfektionsmittel benutze ich Natriumhydrogenchlorid (Klorix) aus einem Zerstäuber, auf Alkohlbasierte Desinfektion verzichte ich lieber wegen der Brand-explosionsgefahr beim Ausglühen von Skalpell und Nadel – ausserdem habe ich mit Alk ja keine sporiziede Wirkung (wobei das bei Hefen wohl nicht so wichtig sein dürfte).
Ich habe aber auch schon 70-80 %iges Ethanol versucht (Brennspiritus).
Eigentlich dürften bei den Mengen an Desinfektionsmitteln keine Hefen mehr überleben, ich verstehe also nicht wo die herkommen. Sie treten auch nicht unbedingt an den Impfstellen direkt auf sondern ehr verteilt über das ganze Agar, meist eine Fläche die 2-4 Tage nach der Impfung sichtbar wird. Auszuschliessen ist auch das die Kontis schon vor dem Öffnen der frischen Petries schon vorhanden waren, diese werden oft erst 3-4 tage nach der Sterilisation verwendet und wenn ich sie testweise länger unbeimpft verschlossen in die Brutkammer stelle bleiben sie rein.
Sterilisiert wird im DDKT, immer 3x 6 Petries 20-30 min.
Auch sterilisierter Roggen bleibt- wenn die Gläser nicht geöffnet werden- ohne Fremdwachstum (einige Gläser standen schon 4 Wochen, bis ich dann mal ne Geruchsprobe genommen habe).
Was mir wohl schon aufgefallen ist, ist das die Glovebox einfach viel zu klein ist um halbwegs vernünftig darin handtieren zu können, eine 45l Box ist grade auf dem Weg zu mir.
Trotzdem finde ich es seltsam das in der "Chloratmosphäre" noch Hefen überleben....
Falls hier jemand Ideen hat...
Die Temperaturen:
Ich habe festgestellt das PF-Kuchen bei 33 Grad C viel viel schneller bewachsen sind als bei den oft empfohlenen 27-28 Grad C.
Es wird immer darauf hingewiesen das bei höheren Temperaturen die Chancen für die Kontis steigen, wenig - eigentlich gar nichts - konnte ich in Erfahrung bringen darüber bei welcher Temperatur es den Cubensis wirklich zu warm wird.
Falls mir dazu jemand was sagen kann...
Dann mal zum Sporenabdruck.
Plan ist ne Petrie mit Alufolie zu "polstern", zu sterilisieren und dann einen oder 2 Hüte darauf zu legen, evtl. In der Glovebox.
Nach dem Entfernen der Hüte die Alu zusammenfalten und eintüten.
Bekommt man so ne halbwegs sterilen Abdruck, oder besser die Alu weglassen und nach dem Entfernen des Hutes die Petrie versiegeln?
Näme natürlich etwas mehr Platz weg aber weniger Material bedeutet wahrscheinlich die Sterilität ist höher?
Ein weiterer Plan ist es auf das lästige Öffnen von sterielen Substratbehältern weitgehnd zu verzichten (bei Backups auf Petries geht das natürlich nicht) und darum selektiertes Myzel in flüssiger Form zum Impfen bereit zu halten.
Rezepte für Flüssigmedien sind hier jezt erstmal zweitrangig, es kommt mir mehr auf die Technik an:
Meine Idee wäre es 400-500 ml Gläser mit Schraubdeckel zur Hälfte mit Flüssignährmedium zu sterilisiern.
In den Deckel sollen zwei jeweils mit Silikon wider verschlossene Löcher, eines um mit einer langen dicken Kanüle Myzel entnehmen zu können bzw. bei Bedarf steriles "Zuckerwasser" nachfüllen zu können, ein zweites um mit einer dünneren, kürzeren Kanüle, die aussen irgendwie mit Polifil gesichert wird Druckausgleich bzw. Gasaustausch zuzulassen.
Kann das funktionieren und wie verstopfe ich die "Lüftungsnadel am besten? Einfüren müsste ich sie quasie ja nur wenn auch Myzel entnommen wird. Wie sicher ist das Polifil ?? Wie dick müsste aussen die Lüftungskanüle gepolstert sein, reicht es den Stutzen der Kanüle vollzustopfen?
Und dann mal zum Casing:
Ich sehe Perlite als Grund und Cocohum und Vermiculite als Deckschicht vor.
Soweit ich das bisher gelesen habe sollten alle 3 Schichten etwa die gleiche Dicke haben, meist 2cm Boden, 2cm Substart, 2cm Deckschicht. Bringt es Vor-oder Nachteile zb. auf jeweils 3,4,5 cm pro Schicht zu gehen? Hab da noch nicht so viel gefunden...
Und zuletzt noch eine Frage zu P.cyanescens.
Ich hab wenig über gut geignetes Substrat gefunden.
Die Boden und Deckschicht scheint man ähnlich wie bei Cubensis gestalten zu können aber das Substrat? Roggen+25% pasteurisierter Pferde-oder Rinderdung?
Kleiner Tipp wäre klasse...
Ich weiss, eine Menge Text... werd die Tage zur Auflockerung und näheren Erleuterung noch ein paar Fotos einbauen ;-)
Danke für das Interesse !!
Geschrieben von: hogie Aug 20 2015, 17:01
Nur mal ein paar Dinge, die mir nach dem langen Text spontan dazu einfallen. Natürlich hast du mit Alkohol eine sporizide Wirkung, aber die Konzentration muss zwischen 70 und 80% und die Einwirkungsdauer sehr lang sein (mind. 10min). Desinfektion ist immer ein langsamer Zeitvorgang, deshalb wird eine Desinfektion das Ausglühen des Impfbestecks nie ersetzen können. Auch das Natriumhypochlorit ist keine sinnvolle Lösung, dazu noch äußerst eklig - wenn man die ganze Zerfallsreihe betrachtet (Klorix ist mit Natriumcarbonat stabilisiert).
Setze bei allem, was du machst, auf geringste Kontiraten. Das ist der Schlüssel zum Erfolg. Wenn du Pilze klonst, entnimmst du das Material, das du mit höchster Wahrscheinlichkeit steril heraus bekommst. Bei zarten Pilzchen ist das seltenst was vom Hut, sondern ein aufgerissener Stiel.
Wenn du schon mit Sporen aus wahrscheinlich professioneller Quelle angefangen hast, gleich kleinste Mengen auf Petris aufbringen und dort selektieren. Auf Petris kann man auch Kontis gut beherrschen, was in Flüssigmedien völlig unmöglich ist.
Geschrieben von: Herr von Böde Aug 21 2015, 01:00
Hallo hogie ![]() ,
,
also so wie das gelesen habe hat Alkohol egal in welcher Konzentration keine wesentlich sporenabtötende Wirkung ![]()
Hauptgrund für den Einsatz von Klorix ist aber die Nichtbrennbarkeit, wie Du ja schon sagst ersetzt keine Desinfektion das ständige Ausglühen vom Impfbesteck und da habe ich einfach Angst das mir die Impfbox irgendwann mal um die Ohren fliegt ![]()
Mit Schimmel (auf dessen Sporen ich es abgesehn hatte) habe ich bisher gar keine Probleme, auch nicht bei Versuchen mit dem auf 70-80 vol %igem verdünntem Brennspiritus. Es sind allein die Hefen, die meines Wissens ja nicht sporenbildent sind.
Schon allein damit sich der Spühnebel setzen kann und mir nicht in die Petries kommt warte ich nach der Spühdesinfektion immer 10-15 min bis ich mit dem Arbeiten anfange.
Auf der Klorixflasche steht übrigens das als einziger nicht flüchtiger Rückstand Natriumchlord, also Kochsalz, übrigbleibt.
Natürlich ist Flümy noch schwieriger zu handhaben in Bezug auf Kontis. Backups von gutem Myzel wird es deshalb immer auf Petries geben.
Und ausgedehntere Versuche mit Flümy wird es sicher erst geben wenn mindestens 80 % meiner überimpften Petries und Substratgläser kontifrei bleiben, derzei liegt die Ausfallquote etwa in der Höhe ![]()
Ich denke nur das, wenn ich mal ne steriiele Flümykultur habe, die Kontirate beim Beimpfen des Substrates noch weiter heruntergeschraub werden kann ausserdem
dürfte sich flüssiges Myzel natürlich besser im Substrat verteilen als Agarstückchen.
Aber klar, das steht im Moment nicht an ![]()
Gut, also Klonen aus dem Stiel ist ok, erscheint mir auch viel einfacher derzeit.
Macht es die Isolation einer einzigen Genetik betreffend also keinen unterschied ob das die Myzelstückchen aus Stiel oder Hut kommen?
Angenommen das Phänomen des Fruchtkörpers aus 2 oder mehr Myzel(eltern)
ist real und verbreitet...
Ach so, wie schon gesagt bei der ersten "Petriegeneration", also Myzel aus den PF-Kuchen auf Agar übertragen gab es seltsamerweise kaum Ausfälle.
Ausserdem dachte ich, dass wenn ich Myzel aus einem Kuchen entnehme eine gewisse "Vorselektion" bereits stattgefunden haben dürfte: die schneller wachsenden Myzelien dürften schon verbreiteter im Kuchen gewesen sein als die langsameren. Darum hab ich keine Petries direkt mit der Sporenlösung beimpft.
An dieser Stelle war das auch kein Problem in Bezug auf Kontis.
Geschrieben von: Herr von Böde Aug 22 2015, 19:40
Nochmal was ganz anderes:
ich würd gern (nur zu Testzwecken) die Cakes nach dem jetzigen Flush (ist wohl in 3-4 Tagen soweit) zu einem Casing weiterverarbeiten, es wäre 1x der 4 und 2x der 3te Flush).
Geplantes Vorgehen:
Cakes einzeln oder alle zusammen (was ist-unabhängig von der Kontigefahr-besser?)
in einer Platikbrottüte zerbröseln und etwa 10h im Kühlschrank in einer 2-3 %igen sterielen Dextrose-Wasserlösung Dunken.
Das ganze in einer 1l Eisdose auf eine 2cm Schicht sterielem Perlit und unter eine evtl. etwas dickeren Schicht Vermiculite (ich denke auf Cocohum werd ich hier verzichten) packen.
Evtl. noch 125ml (1/3 der ursprünglichen Cakesubstratmasse) sterieles, fertiges Roggensubstrat auf die zerbröselten Cakes unter dem Vermiculite verteilen.
Hauptfrage ist ob die Cakes tatsächlich miteinander vermischt oder doch besser einzeln auf dem Perliteboden verteilt und dann abgedeckt werden sollten.
Hintergrundgedanke dabei ist nicht so sehr die Kontiangst (wenn was drin ist wirds wohl eh nichts) sondern ehr dass nicht unnötige Myzelkonkurentz entsteht, die kräftigsten Myzelien aus den einzelnen Kuchen könnten so "in Ruhe" lokal ihre Deckschicht durchwachsen, ohne das sie sich erst erneut im PF-Substart durchsetzen müssten.
weitere Tipps hier zur Vorgehensweise sind sehr willkommen ![]()
Danke !!
Geschrieben von: hogie Aug 22 2015, 22:06
Geschrieben von: Herr von Böde Aug 22 2015, 23:09
Ok, wegen dem Zerbröseln, dem Zucker im Wasser oder dem Kühlschrank?
Wie besser vorgehen?
Hab die Cakes bis jetzt nach jedem Flusch, natürlich unzerbröselt, über Nacht im Glas und Kühlschrank gedunkt (der nächste Flush startete dann auch jedesmal 2-4 Tage später, der Cake der jetzt den 4ten Flush ansetzt hat schon 5 tage gebraucht) mehr als 1-2ml Wasser (habs gewogen) werden dabei nicht aufgenommen. Pro Flush ging als jedesmal etwa die 5-10 fache Menge Wasser verloren.
Alternativ die Boden und/oder Deckschicht etwas feuchter lassen als üblich und die Cakes gar nicht bröseln, den Platz zwischen den Cakes mit etwas feuterem Roggensubstart auffüllen?
thx
Geschrieben von: chronic Aug 22 2015, 23:16
Herr von Böde so wird das nix. Verschiedene Pilzstämme, sogar der gleichen Art und des gleichen Strain vertragen sich nicht. Multispore von einem Print geht, aber was nicht geht ist verschiedene Stämme von dem Print selektieren und dann wieder zusammen bringen. Jeder Stamm wird versuchen sich durch zu setzen. Am Ende schaft es keiner oder das Ergebniss fällt grotig aus.
Wenn die Substratkuchen von verschiedenen Strains zerkleinert und vermischt werden finden die einzelnen Hyphen nicht mehr zueinander.
Dunken in 2-3 %igen steriler Dextrose-Wasserlösung wird zu erhöhter Kontianfälligkeit führen. Wenn Dunken dann dann am besten als Casing in reinem Wasser. Leitungswasser reicht.
Noch etwas zur Reinigung und Desinfektion. Chlorlösung kannst du für eine abschließende Reinigung deiner Glovebox wie auch der Arbeitsfläche nehmen. Mehr nicht.
70% Alkohol ist das Mittel der Wahl zur Desinfektion bevor du anfängst zu arbeiten um die Arbeitsfläche zu reinigen und eine "Luftwäsche" durch zu führen. Eine Kombination mit Chlorlösung ist absolut Kontra, alleine weil die Einwirkzeit von Chlor deutlich länger ist als die von Alkohol.
Geschrieben von: Herr von Böde Aug 23 2015, 02:39
Hi, es geht um die ganz oben erwähnten Golden T. "Startcakes" die mit Sporenspritzen beimpft wurden.
Alles was ich an selektiertem Myzel habe stammt aus Cakes die so beimpft wurden (ich wollte eine gewisse Vorselektion, die Wahrscheinlichkeit rasch wachsendes Myzel bei der Entnahme aus den Kuchen zu erhalten ist höher).
Nochmal zum Alkohol, was bitte macht man gegen die Explosionsgefahr?
Meine Überlegung die mich zum Chlor geführt hat war nicht nur die sporizide Wirkung sondern vor allem die Brandgefahr beim Alkohol:
Wenn ich den Innenraum einer luftdicht verschlossenen Box mit 70%igem Alkohl einsprühe, so das die Luft gesättigt wird und die Oberflächen feucht sind, müsste ich doch nach dem Abtrockenen ein explosives Gasgemisch in der Box haben (der verdampfte Alkohol kann ja nicht raus) ??
Ich habe schlicht Angst, das mir die Kiste um die Ohren fliegt ![]()
Geschrieben von: hogie Aug 23 2015, 20:49
Ohje. Bei Zimmertemperatur verdunstet Ethanol so langsam, bis du da ein explosionsfähiges Gemisch bekommst, musst du dich schon ziemlich albern anstellen. Größere Bedenken habe ich schon mit der Brandgefahr. Ich habe immer einen Eimer Wasser bereit gestellt. Denn falls mal ein Handschuh oberflächlich Feuer fängt, dann zählt jede Sekunde, dass du ohne Verbrennung davon kommst.
Wenn es um Ex*losivität und Druckwellen geht, solltest du mal Meyers Ex*losivstoffe lesen. Der bezeichnet Schwarzpulver lapidar als leicht schiebende Wirkung
Geschrieben von: Herr von Böde Aug 24 2015, 13:49
Ok, dann steige ich auf Ethanol um (werd nen Foto meines Gesichtes einstellen wenn ich mich zu albern angestellt habe ;-) )
Interessanterweise habe ich vorgestern 7 Backups von dem GT-1 Myzel (oben das zuerst abgebildete) angelegt und habe plötzlich 0 Kontis (zumindest von den Hefen war nach dieser Zeit schon immer deutlich was zu sehen).
Um schneller arbeiten zu können habe ich die Glovebox nicht als solche benutzt, einfach auf die Sete gestelllt (Handsychuhe ausgestülpt und Löcher mit Alu+Heisskleber verschlossen) und nur nen "Voghang" aus Frischhaltefolie daor gemacht.
Ich hab dann sozusagen von unten durch diese Vorhang mit blossen Händen (natürlich gewaschen und desinfiziert) gearbeitet.
Die Cakes werden heute und morgen abgeerntet:
und dann zu Casings verarbeitet.
Ich denke ich werde wirklich auch in 3 verschiedenen Behältern (wahrscheinlich 500g Quarkbecher) casen:
Einen Cake lass ich komplett unzerbröselt und packe Ihn nach 12h dunken in Wassen in das Casing.
Den 2ten werd ich zerbröseln und in dem Zustand dunken und casen.
Der dritte wird zerbröselt und vor dem Casen in Dextrosewasser gedunkt.
Alle bekommen noch 2-3 Essllöffel frischen Roggensubstrat dabei.
Kann ich durch diese Gegenbenheit eigentlich auf einer Petrie checken ob es sich um identisches Myzel handelt ?
Ich hab ja aus jedem (mit Sporensptitze beimpften)Kuchen bisher midesten 3 von unterschiedlichen Stellen stammendes Myzel entnommen und einzeln auf Agar verpflanzt.
Kann ich nun also -sobald die Petries bewachsen sind- wieder aus jeder Petrie bewachsene Agarstücke entnehmen und gemeinsam auf eine Petrie pflanzen um aus der Reacktion der Myzelien beim Aufeinandertreffen (durch das Wachstum) darauf schliessen ob es sich evtl. um ein und das selbe Myzel handelt?
Also indentisches Myzel wächst zusammen unterschiedliches Myzel behält ne mehr oder wenoger deutliche Abgenzung.
Geschrieben von: Herr von Böde Aug 30 2015, 15:13
Heute brach durch alle 3 Casings das erste Myzel, leider aber auch in weit größerem Maße ein Schimmelkonti, wahrscheinlich Aspergillus niger...
Hab die Casings direkt draußen an der Mülltonne aufgebrochen, es sieht so aus als wären die frischen Roggensubstratkörner Keimboden der Kontis, ausser dem Schwarzschimmel vermute ich mal wieder Hefen, des süßlich alkoholischen Geruches wegen.
In ein paar Tagen kann ich wahrscheinlich ein paar mit A+ Sporen und Golden T. Sporen (bei diesen =selbstgemachter Abdruck+Spritze) beimpfte Gläser (Roggensubstrat) ins erste planmäßige Casing packen.
Werd bei der Gelegenheit einzelne Körner zwecks Myzelselektion auf Agar legen.
Die ersten A+ wachsen aus dem Pf-Kuchen (430ml), interessanterweise
wachsen auf dem gleich gr0ßen Pf.-orig. Kuchen, der 3-4 Tage früher gestürzt wurde, bisher nur 2 Pilzchen.
Geschrieben von: hogie Aug 30 2015, 18:42
Geschrieben von: Herr von Böde Aug 31 2015, 10:08
Pfusch ? , naja für mich war das schlicht und einfach ein Versuch...
Die beiden letzten Cakes werd ich nach dem 3ten Flush ähnlich behandeln, nur ohne frisches Roggensubstrat.
Mit allem anderen bin ich recht zufrieden.
Hab gestern noch 8 Petris und 7 Roggensubstratgläser mit Myzel beimpft, wenn die großteils sauber bleiben hab ich vielleicht den Bogen schon raus, einfach das Desinfekt länger einwirken lassen und in der Glovebox schneller arbeiten.
Nächster Schritt ist dann halt tatsächlich mal nen Casing flushen zu lassen :-)
Geschrieben von: hogie Aug 31 2015, 16:26
Sobald du den durchwachsenen Kuchen mal aus dem Glas genommen hast, ist er äußerlich genügend kontaminiert. Da darfst du keinerlei besiedelbares Substrat und Nährstoffe mehr zufügen. Auch die Idee mit der Zuckerlösung geht 100% schief. Denn unerwünschte Kontaminanten sind schneller als dein gewünschtes Mycel.
Geschrieben von: Herr von Böde Aug 31 2015, 16:47
![]()
Joa, das liest man ja auch überall, wollts aber einfach nicht so recht glauben ![]()
Als ich den Schimmel durch den Klarsichtdeckel sah hatte ich zuerst sogar schon befürchtet das mir oben die Deckschicht (reines, feuchtes Vermiculite) schimmelt,
darum hab ich die Casings draußen auch auseinandergebrochen um mich davon zu überzeugen das dem nicht so ist und war dann echt beruhigt das der Schimmel offensichtlich von dem Roggen ausging.
So, was meint Ihr, noch 1 Woche oder ehr 2-4 Tage bis ein solches Glas bei 25-27 Grad C bereit zum Casen ist ?
Ich weiss, es ist etwas feucht geraten..
Geschrieben von: hogie Aug 31 2015, 17:27
lieber länger warten, bis die Körner dicht durchwachsen sind. Das macht sie robuster.
Geschrieben von: Herr von Böde Sep 5 2015, 19:46
So, gestern wurden 4 mit "Albino A+" Sporensritze beimpfte 430 ml Gläser ins Casing gepackt.
In den nächsten Tagen folgen noch 2 Gläser die mit selbst gesammelten Golden T. Sporen beimpft wurden.
Die Deckschichten sind evtl. etwas dick, hab hier grad mehrfach gelesen das gerne mit unter 1cm dicken Deckschichten gerarbeitet wird.
Drei der Gläser wurden in 500 ml Quarkdosen gecased und eines in einer 1000ml xl "Heimchendose mit Deckel".
Sobald ich mehrere Gläser mit einem genetisch identischen Myzel bereit habe sollte es ja kein Problem sein diese Gläser miteinander zu vermischen und bsplw. in 2l Eisdosen zu casen.
Habe vor 3 Tagen auch mehre Gläser mit Flümy einer isolierten Golden T. Genetik beimpft. Bei der grade stattgefundenen ersten Kontrolle der Gläser sehe ich das erste Myzelwachstum, an vielen Stellen in den Gläsern.
Die "Sicherheitsprobe" des Flümys auf 3 Petries mit KDA sind noch absolut rein und kontifrtei. Interessanterweise scheint das Myzel aber auf dem Nähragar schlechter - langsamer Fuß fassen zu können als in den Substartgläsern.
Die Methode mit den zwei "Ottto-normal"- Silikonimpfports - die halten das Autoklavieren problemlos aus (einen zur Entnahme, 1nen für eine zweite, dünnere Nadel deren Stutzen mit Polyfil gestopft ist für den Druckausgleich) , scheint im ersten Durchlauf zu funktionieren. Da kein Unterdruck im Glas herscht und daher der Schraubdeckel sicher nicht 100%ig dicht halten kann, ist dieser ebenfalls mit Silikon zusätzlich abgedichtet.
Ich habe ausserdem herausgefunden woher die plötzlich aufgetretende Hefekontiattacke kam.
Ich hatte ca 25 Petries auserhalb des DDKTs abkühlen lassen, nichtmehr gestapelt, sondern nebeneinander unter 2 Schichten Alufolie
(hatte es da einfach zu eilig).
Da wurde beim Abkühlen wohl doch weit mehr Luft eingesaugt als ich erwartet hatte.
Ich lasse die Petries jetzt -noch gestapelt und in Alufolie gepackt- in der sterilisierten , inzwischen ausreichend großen Glovebox über Nacht abkühlen- soviel Zeit muss sein...
Geschrieben von: hogie Sep 5 2015, 23:36
Ein Weg zu perfekten Petris läuft bei mir so: Gerite statt Agar. Der ist etwas tricky zuzubereiten, führt aber zu einem wunderbaren, glasklaren Gel, das mehrfach autoklavierbar ist und dabei nicht mehr wieder schmilzt, sobald er ein Gel gebildet hat .Wenn die Petris abgekühlt sind, verschließe ich sie und schweiße sie in Sterilverpackung ein. Dann werden die Petris in der Sterilverpackung autoklaviert. Da sie bei geringer Luftfeuchte kontaminationssicher verpackt sind, kann man sie bei trockener Luft trocknen lassen, bis sie kondenswasserfrei sind. Dauerhaft nahe 100% RF dürfen aber nicht in der Sterilverpackung sein, weil sie sonst durchwachsen werden kann.
Geschrieben von: Herr von Böde Sep 6 2015, 03:43
"Gerite" muss ich gleich erstmal googeln, hört sich interessant an.
Ich möchte aber - wenn sich die Methode als längerfristig brauchbar erweist - zum Substratbeimpfen lieber das Flümy benutzen und Petries ehr um Backups von bevorzugten Myzelien anzulegen.
Beim Agar stört einfach das Festkleben - natürlich ausgerechnet der bewachsenen Seite - der Stückchen am Glas.
Ausserdem scheint das Flümy die Besiedlung tatsächlich erheblich zu beschleunigen. Ich sehe nach 4 Tagen, sicher über 15 infizierte Stellen gut verteilt in jedem Glas, dies auch noch mit nur 1xigem Schütteln
(ich hab dabei immer Angst das mir doch was durchs Polyfil gesaugt wird oder dieses sich mit besiedelbarer Feuchtigkeit anreichert).
Ich glaub das wäre mit Agar nicht möglich, schon der benötigten Agarmenge bzw. der daraus resultierenden Konsistenz des Nährbodens wegen.
Ausserdem reicht es locker aus den Roggen 30 min zu köcheln (beim nächsten Versuch werd ichs sogar mal mit 20 min versuchen) da 7-10ml
Flümy pro Glas gut nachfeuchten.
Hängt aber tatsächlich davon ab wie lange so ein Glas mit 250 ml Flümy zu erhalten bzw, kontifrei zu erhalten ist.
Hat eigentlich jemand Erfahrungen mit der Anreicherung der Nährböden (Agar, Gerite, Flümy oder Substrat) mit Kaliumhydrogenphosphat?
Hab die jetzigen Roggengläser mal mit 0,14g des Salzes pro 500g (trockenen) Roggen angereichert.
Geschrieben von: hogie Sep 6 2015, 03:52
Das war leider ein Tippfehler. Es ist Gelrite.Ich benutze das Zeug auch längst im Kartoffel- oder Wurstsalat.
Geschrieben von: Herr von Böde Sep 7 2015, 20:23
Musste heute schonmal lauern und stelle erstaunt und erfreut fest das in dem "Heimchendosencasing" das erste Myzel schon durchbricht (ist sicher kein Schimmel), Deckschicht ist übrigens recht locker und besteht aus jeweils etwa 50vol.% Cocoohum und Vermiculite:
Jetzt kommt doch nochmal die eine oder andere Frage auf, bezüglich "Overlay" und "Patchen":
Aus dem was hier und an anderer Stelle gelesen habe schliesse ich mal, dass "Overlay" soviel bedeutet das die Deckschicht irgendwie zu schnell komplett durchwachsen wird, bevor es zur Fruchtkörperbildung kommt.
Kann man mir diesen Begriff evtl. nochmal etwas genauer erklären?
Mir ist nicht klar welches Problem das totale Durchwachsen verursacht (spätestens beim 2ten Flush dürfte die Deckschicht ja ohnehin komplett durchwachsen sein).
Bei einigen Anleitungen (ich glaub zB. bei der "Simple-Tek.") wartet man ohnehin bis die Deckschicht komplett bewachsen ist bis man die Casings in die Fruchtung schickt, bei anderen Teks wird gepatcht, so das die Deckschicht gleichmäßig durchwächst, dies bedeutet dann wohl aber auch das die Deckschicht am Ende komplett durchwachsen ist ?
Wieder andere Teks leiten die Fruchtung bei etwa 30% Durchwachsen der oberen Schicht ein.
Irgendwo habe ich auch gelesen das die Deckschicht nach jedem Flush abgekratzt und eine neue aufgetragen wird, wahrscheinlich weil die durchwachsene Schicht nicht mehr soviel Wasser aufnehmen kann wie eine Frische es liefern würde. Macht sowas tatsächlich Sinn oder kostet das dem Substratkern nur unnötig Power ?
Also, hier herrscht bei mir noch einige Verwirrung ...
Wenn mich jemand über die genauen Zusammenhänge und Bedeutungen aufklären könnte wäre das super :-) Danke schonmal!!
So rein nach meinem "grünen Daumen Gefühl" würd ich bei dem oben gezeigten Casing noch 1-2 Tage warten, bis das Myzel deutlicher sichtbar ist und dann ggf. etwas Patchen sollte bis dahin noch kein Myzel
an dem Rest der Deckschicht zu sehen sein.
Andererseits: 30% der Oberfläche sind es fast schon die Myzelwachstum zeigen, nach anderen Teks könnte der Behälter also fast schon in die Fruchtungskammer überführt werden...
Danke für das Interesse und jeden Tip :-)
Geschrieben von: hogie Sep 7 2015, 21:40
Verlass dich besser auf deinen grünen Daumen. Je dichter der Pelz gewachsen ist, desto robuster wird der Kuchen.
Geschrieben von: Herr von Böde Sep 8 2015, 19:37
Juchuh, überall Myzelwachstum, im "Heimchendosencasing" scheint es doch recht gleichmäßig zu wachsen:
Casing 2:
Casing 3:
Casing 4:
Die beiden Golden T. Gläser aus selbstgeernteten Sporen wurden gestern Abend ebenfalls gecased.
Edit
By the way:
Die beiden letzten PF-Tek Cakes verhalten sich übrigens ehr merkwürdig,
Der Albino Cake (rechts) wurde wärend des Lüftens von meinem Hund weggetragen ![]() ,
,
darum hab ich den Teil welchen er im Maul hatte entfernt, sieht auch nach nur einem Flush entsprechend blau aus. Der zweite Flush besteht offenbar aus einem einzigem Pilz...
Links, der noch vollständige 430ml PF.orig. Cake hatte bisher einen Flush, bestehnd aus 3 Pilzchen (der größte war allerdings sehr kompackt) und wiegt jetzt im trockenem Zustand 1,1g.
Der nächste Flush kommt nicht so recht in die Pötte.
Keine Ahnung was da los ist, wahrscheinlich Feuchtigkeitsmangel.
Werd nach dem nächsten Flush mal volle 48h im Kühlschrank dunken, mach aber 3+ wenn die blöden Cakes durch sind und ich mich auf die Casings konzentrieren kann ![]()
Geschrieben von: hogie Sep 8 2015, 21:48
Das dunken der PF-Cakes kannst du dir sparen. Die nehmen so gut wie nichts auf. Wenn sie nicht mehr flushen, würde ich sie weg werfen oder deinen Hund fressen lassen. ![]()
Geschrieben von: Herr von Böde Sep 9 2015, 03:30
![]()
Neue Experimente mit der Umstellung auf carnivore Pilzernährung stehen noch nicht an
Ansonsten kann ich Dir nur recht geben.
Hatte die kleinen GoldenT. 125ml Cakes nach jedem Flush über Nacht im Kühlschrank gedunkt und das hinzugefühgte und dann das wider abgegossene Wasser mal gewogen... das waren Minimengen die da aufgesogen wurde.
Um den Albino Cake täte es mir wenig leid, da ist ja nun einiges zu erwarten, selektiertes Myzel auf Petrie gibts davon auch inzwischen.
Beim Pf-orig. werd ich noch versuchen zumindest nen Sporenabdruck rauszuholen, ich hatte -etwas übermütig- den Rest der original Sporenlösung in 2,5l Roggensubstrat in einem Mikrofilterbeutel inijeziert, der dann leider voller Kontis war (Verschluss und Impftechnik war alles andere als ideal).
Ausserdem "will" der Cake auch offensichtlich: Myzel wächst auf die feuchte Alufolie (leider unmöglich das mit der Handycamera einzufangen), beim ersten Flush sah es sogar so aus als würde ein Pilz senkrecht aus der Alufolie wachsen, ziemlich getrennt vom Kuchen.
Werd also noch warten bis die Casings in die Kammer können, mal das Perlite wechseln und den Kuchen wohl zerbröseln und (ohne frischen Roggen und Zuckerwasser) casen.
Edit:
gesagt, getan. Hab den PF-orig. Cake gecased, echt unglaublich wie fest das Myzel die Bestandteile zusammenzieht, nicht ganz einfach den Cake in einer Brottüte zu zerböseln ohne Löcher in die Tüte zu drücken.
Hab gute 100-150ml Wasser mit in die Tüte gegeben, dieses wurde von den am Ende (wenig)Matsch- ca. max.1 cm3 großen "Bröseln" auch komplett absorbiert, denke der Cake war wirklich sehr trocken, wog auch nur gute 120g ...
Mir ist nicht ganz klar wie das sein kann, betrifft aber sicher beide Cakes.
Hatte das Gemisch mit 2-1-1 (Vermi. Reism.-Wasser) angerührt, vielleicht wieder die schreckliche Ungeduld und Druck wurde nach der Sterilisationszeit direkt abgelassen ?? Seis drum...
Ich versteh übrigens gar nicht wiel Leute den Pilzduft- und Geschmack so ekelig finden können, ich fand den Duft der beim Bröseln und Umfüllen aus der Tüte kam
wirklich sehr sehr angenehm, organisch frisch, pilzig
Geschrieben von: hogie Sep 10 2015, 00:49
Deshalb verwenden modernere Autoklaven immer Vakuumpumpem und evakuieren vorher mehrfach.
Von normalen Haushaltsfolien sollten Gefrierbeutel dafür ganz gut geeignet sein. Die sind fast steril (musst mit etwa 5 Keimen pro Quadratzentimeter rechnen), sind zäh und besseren Herstellern auch aus etwas dickerem PE (die von Aldi sind nicht schlecht).
Hatte das Gemisch mit 2-1-1 (Vermi. Reism.-Wasser) angerührt, vielleicht wieder die schreckliche Ungeduld und Druck wurde nach der Sterilisationszeit direkt abgelassen ??
Ja das war es 100pro. Den Druck darfst du nicht ablassen, denn sonst siedet der Inhalt der Gläser schlagartig. Wären die Deckel der Gläser nicht so konstruiert, dass sie Überdruck ablassen können, würden dabei alle Gläser platzen. Am Scherbenhaufen würde das jeder gleich bemerken
Beim Aufwallen verlierst du nicht nur viel Wasser aus den Gläsern (obwohl du denkst, sie seien fest zugeschraubt und hermetisch dicht), sondern es kann dir auch Stärkerotz durch die Filter drücken. Solche Gläser kannst du gleich weg schmeissen und brauchst sie erst gar nicht beimpfen, weil sie zu 99% kontaminieren. Denn die Filter sind keine Barriere mehr, sondern werden bald durchwachsen.
wirklich sehr sehr angenehm, organisch frisch, pilzig
Der Geruch ist pilzig und durchaus noch angenehm. Aber der Geschmack, naja. Ich finde ihn schon zum Kotzen. Als ich vom ersten Pilzchen mal ein Stück probiert habe, dachte ich auch, gar nicht so schlimm. Der Geschmack war nach dem ersten Trip aber bereits unerträglich. Da brennt sich wohl Vergiftungssymptomatik im Gehirn ein.
Geschrieben von: Herr von Böde Sep 10 2015, 03:30
Joa, die Physik des Autoklavierens ist mir schon halbwegs klar, kann mir darum auch gar nicht so recht vorstellen einen solch fatalen Fehler (bei den PF- Cakes) gemacht zu haben.
Da solches aber sicher oft gemachte Anfängerfehler sind darf das gern nochmal erwähnt werden.
Wer nicht versteht warum man den Druck keinesfalls schlagartig ablassen darf sollte sich mal mit dem Prinziep des Vakuumtrocknens beschäftigen ;-)
Das Substrat im Beutel wurde übrigens nicht geköchelt sondern im Beutel eingeweicht, dann strammst möglich zusammengedrückt und 2h
sterilisiert.
Luftnester schliesse ich daher aus. aber 3h wären evtl. wirklich noch besser gewesen.
Ich glaub aber doch das es an der Verschluss und Impftechnik lag:
Hab son kleines Handfolienschweissgerät mit Batterie , ich hatte schon beim Verschweissen das Gefühl dass das suboptimal läuft und hab der Schweissnaht nicht wirklich getraut zumal sie das Autoklavieren ja noch aushalten musste bei dem sich der Beutel unweigerlich spannt.
Zum Impfen hab ich nach dem Auskühlen einfach nen dicken Silikontropfen auf den Beutel gemacht und da durchgestochen, in der Annahme dass das Loch sich wieder zuzieht...das hat es sicher auch aber beim Hantieren mit dem Beutel fiel der geschlossene Silikonpfropf bald komplett ab.
Die Beutelaktion war insgesamt tatsächlich Pfusch, darum werd ich auf Beutel verzichten bis ein anständiges Folienschweissgerät zur Hand ist
und ich mich über das Beimpfen besser informiert habe.
Psilos habe ich tatsächlich auch schon oft gegessen ![]() und ich mag den Geschmack.
und ich mag den Geschmack.
Grade der sich haltende Nachgeschmack gibt mir beim Hochfahren des Trips ein gutes Gefühl auch genug gegessen zu haben .
Der Geschmack bzw. die Konsistenz ist für mich auch ein Grund die frischen, ungetrockneten Wichtel zu bevorzugen.
Ansonsten:
Das "Heimchendosencasing" steht seit ca. 19:00 Uhr in der Fruchtungsbox, das Myzel bedeckte schon das komplette Casing.
Die "Quarkdosencasings" brauchen sicher noch 24-36h.
Habe wärend des Hantierens in der Brutkammer übrigens den typischen sauer-alkoholischen Hefegestank feststellen müssen, darauf wurden 8
von 9 mit Flümy beimpfte Gläser - nach Geruchsprobe am Polyfil-
bzw. deren Inhalt- entsorgt.
Flümytechnig also noch nicht ausgereift, die nächsten Gläser
werden wieder mit Agar beimpft...
Nächstes wichtiges Zwischenziel ist es also tatsächlich konstant erfolgreich mit (selektiertem) Myzel - und nichtmehr mit Sporen- Substrat zu beimpfen, sprich das Arbeiten mit der Glovebox muss sicher werden...
Geschrieben von: hogie Sep 10 2015, 04:45
Das hört sich alles super an. Du bist endlich mal wieder einer, der sich nicht nur was rein pfeifen will, sondern auch etwas auf dem Kasten hat und die Zusammenhänge versteht. Ich bin zwar ein alter Sack, aber noch nicht völlig senil. Ich freue mich auf weitere Posts oder Threads mit dir!!!
Zum Folienschweissen: es kommt auch auf die Breite der Naht an. 2mm sind schon sehr wenig und als Minimum anzusehen. Den Haushaltsscheiß mit einem Draht, kannst du knicken.
Geschrieben von: Herr von Böde Sep 10 2015, 09:04
Zum Folienschweissen: es kommt auch auf die Breite der Naht an. 2mm sind schon sehr wenig und als Minimum anzusehen. Den Haushaltsscheiß mit einem Draht, kannst du knicken.
Danke danke
OMG, alter Sack ?? Mit 40 ? Keine 3 Jahre mehr
2mm ? Dann wundere ich mich nicht mehr, waren wohl grad mal 0,8mm...
Hab zu Testzwecken auch mal Heisskleber der erst bei ca. 170 Grad C schmelzen soll zum Verschliessen versucht aber das gab eine schöne Sauerei im DDKT, der Druck reichte wohl aus um den dann nur sehr zähflüssigen Kleber rauszudrücken und sich im Topf zu verteilen, würde aber halten.
Evtl. geht die Kombination: Heisskleber unter der zu dünnen Schweissnaht.
Werd das bei Gelegenheit mal testen.
Geschrieben von: hogie Sep 10 2015, 17:55
Es lohnt sich auch, ein ordentliches Schweißgerät zu kaufen. Ich benutze es im Haushalt ständig und häufiger als die Kaffeemaschine. Wenn du Schweißnähten vertrauen kannst, machst du mit Plastiktüten, wozu andere Tupperschüsseln verwenden. Die Tüten sind nahezu steril, der Platzverbrauch im Kühlschrank viel geringer und ressourcenschonend, weil eine Tüte fast nichts wiegt und in der Müllverbrennung nicht nachteilig ist.
Geschrieben von: Herr von Böde Sep 11 2015, 17:05
Wie gesagt, vom Kleben her funktioniert es wunderbar mit dem Heisskleber, hält auch bei Zug.
Einziges Problem der feste Kleber an den Topfrändern nach dem Sterilisieren.
Silikon geht nicht, da hat man das Problem das Du beschrieben hast.
Aber der Bügeleisen-Backpapiertipp wird demnächst mal ausprobiert.
Ich hab nen Single-haushalt, ich verwerte fast alles frisch, keine Tupperdosen im Einsatz.
Son besseres Folienschweissgerät hätte also nur einen Zweck, bleibt aber eine Überlegung wert. Nen Hepa wäre aber wohl ehr dran, das Hantieren mit der rumrurtschenden Glovbox, das in die Handschuhe quälen, die trübe Sicht durch das onehin schon milchige Plastik nervt mich zunehmend^^
Edit:
Habe grade das Pf-orig. Casing entsorgt, dem Geruch nach war das voller Hefe, habs jetzt noch in der Nase ![]()
Zum Glück gibts noch unselektiertes Myzel auf Petrie.
Nochmal Fotos der guten A+ Casings, grad sind auch die 3 in den Dosen in die Fruchttungskammer umgezogen:


Geschrieben von: fluchsDirMaus Sep 12 2015, 19:40
Der Herbst naht, und damit die Outdoor-Saison. Dann wird sich zeigen, ob sich die Mühe der unsterilen Vermehrung gelohnt hat :)
Geschrieben von: Dioxis Sep 13 2015, 16:10
Kleiner Tipp: Für die meisten sachen (z.B. für Petris) reicht zum sterilen Arbeiten ein Bunsenbrenner und eine mit ordentlich Desinfektionsmittel gereinigte Oberfläche (und keine starke Zugluft, sollte selbstverständlich sein).
Einfach in einem kleinen Radius auf der Oberfläche um die Flamme arbeiten, die ausfallquote durch kontamination ist minimalst vorausgesetzt das Medium und verwendete Instrumente sind Steril (selbst bei Vollmedien ohne Antibiotika) und wenn doch, hat man meistens den Finger in der Petrie gehabt oder kontaminierte Infektionslösung verwendet.
Wenn man nicht gerade mit empfindlichen Pflanzlichen und Tierischen Zellkulturen (für mehr haben wir die selbst im Labor nicht benutzt) arbeiten will oder Pilze im Industriellem Massstab produzieren möchte, ist ein Hepa eine ziemliche Geldverschwendung.
Kauf dir lieber einen billigen Brutschrank, davon hast du mehr.
Geschrieben von: Herr von Böde Sep 13 2015, 20:18
Hallo Dioxis,
Du wohnst wohl im OP ?
Vielleicht schaffen es sehr gebüte Hände entsprechend schnell zu arbeiten und damit Kontis beim Beimpfen ohne Glovebox oder Hepa vor Fremdkeimen zu schützen, ich hab immernoch hohe Kontiraten (immer Hefe soweit ich das beurteilen kan) wenn ich in der Glovebox beimpfe, egal ob mit 70-80%igem Ethanol oder mit Klorix desinfiziert wird.
Wie das mit einem Bunsenbrenner funktionieren soll ist mir überhaupt nicht klar, der schafft ja erst zusätzliche Luftverwirbelungen und ich glaube nicht das ich damit Erfolg haben könnte.
Da scheint mit das Arbeiten im Wasserdampf noch einleuchtender, weil der Dampf ein größeres (auch noch gut sichtbares)Volumen einnehmen würde das Kontis fernhält.
Inkubatoren habe ich in ausreichender Menge und Größe (züchte auch noch Reptilien).
Mir gehts beim Hepa in erster Linie um die Bequemlichkeit, sobald werd ich mir aber wohl keinen zulegen.
Bin im Moment dabei Kontiqellen mittels Petries zu ermitteln, irgentwo ist nach wie vor der Wurm drin.
Morgen werd ich 9 Gläser mit bewachsenem Agar beimpfen und- wohl auf Kosten der Durchwachszeit, dafür muss der Glasdeckel aber kürzer angehoben werden- nur mit einem Stück (etwa 1/3 8cm Petrie) impfen.
Geschrieben von: hogie Sep 13 2015, 21:58
Von Gloveboxen halte ich gar nichts. Lieber eine noch primitivere Box und ein Teil der vorderen Öffnung mit Frischhaltefolie zuhängen. Wichtig ist, dass du extrem schnell arbeiten kannst. Das Arbeiten in der Glovebox geht viel zu langsam. Je schneller das Beimpfen geht, desto geringer ist das Risiko. Auch in ziemlich unsteriler Atmosphäre kannst du gute Ergebnisse erzielen.
Geschrieben von: Herr von Böde Sep 14 2015, 20:13
Ja, hab das irgendwo in einem Beitrag von Dir auch schon gelesen und hab das auch schonmal probiert, soweit ich mich erinnere brachte das auch tasächlich brauchbare Ergebnisse.
Da ich mir jetzt aber ne schöne Glovebox zusammengeschustert habe werd ich damit mal Trockenübungen machen um schneller arbeiten zu können.
Am längsten dauert eindeutig das Ablösen der herausgeschnittenen Agarstücke vom Skalpell auf Petries oder Substrat. Das geht leider auch mit der Vorhangmethode nicht schneller.
Extrem festsitzende Deckel auf den Gläsern in der verschlossenen Innobox mit rutschigen Handschuhen zu öffnen ist natürlich schwer und mach regelmäßig das erneute Öffnen und anschliessende Desinfizieren der Box nötig.
Insgesamt alles ehr unpraktisch...
Aber werd wie gesagt damit erstmal üben.
Bin grad dabei neues Substrat zu köcheln, diesmal mit Sittichfutter, etwa im Verhältniss etwa 2:1 (Volumen).
Hab festgestellt das das Futter -wenige- Presspelletts enthält, die aber laut Angabe auch nur aus Getreide bestehen, mal schauen ob das stark matscht, wäre natürlich blöd.
Die beiden Multisporen G.T. Casings sind inzwischen auch zu etwa 50% durchwachsen, morgen oder übermorgen gehts in die Fruchtung.
Drückt die Daumen :-)
Ach so, nochmal was ganz anderes: kann man einen erneuten Alufolienüberzug nach dem Beimpfen getrost weglassen oder macht ein solcher Sinn? Der Luftaustausch dürfte dadurch ja nicht allzusehr verhindert werden..
Geschrieben von: hogie Sep 14 2015, 23:02
Mehrfachverpackungen sind in der Steriltechnik mehr als üblich und äußerst nützlich. Wenn du z.B. sterile Skalpelle, chirurgisches Besteck, Kompressen, Tupfer, Spritzen, Kanülen hast, dann schauen manche akribisch auf das Verfalldatum. Das ist blanker Unsinn, weil der Hersteller mit dem Verfalldatum die Funktionsfähigkeit garantiert, aber nicht die Sterilität. Denn die kann bei falscher Lagerung in kürzester Zeit schon lange vor Erreichen des Verfalldatums hinüber sein.
Noch eine Lage drüber machen, senkt die Kontigefahr.
Ich hatte einst auch mit einer Glovebox angefangen. Die Dinger kann man auch nur schwer sauber desinfizieren (außer mit EO oder Formalin). Falls du der Meinung bist, sie ist nicht optimal, wirft sie fort und heule ihr keine Sekunde hinterher. Mach das in der Pilzzucht bei allem so. Wenn du merkst das Substrat ist viel zu feucht oder zu trocken, gleich in die Tonne und erst gar nciht beimpfen. Dann sind 2 Stunden und ein Euro Getreide futsch und nicht mehrere Wochen Arbeit oder mehr.
Geschrieben von: Herr von Böde Sep 15 2015, 19:07
Hogie, könntest Du das Problem der schweren Desinfizierbarkeit von Gloveboxen nochmal genauer erläutern?
Es sind ja relativ glatte Oberflächen, auch die potentiellen Problemstellen, die "Handchuhstutzen" -aufgeschnittenene und geteilte 500 ml Konservendosen ("Erbsensuppe" -war ne Qual das Zeug zu essen !!)- sind ziemlich glatt und sauber eingebracht.
Für die Vorhangmethode würde ich ja eine ähnliche Box benutzen (in meinem Fall eine 60X40 "Rival-Eurobox" mit Deckel -der natürlich als Boden dient).
Wegschneissen muss ich auch schlecht geratenes Getreidesubstrat nie, hab verschiedene Futtertierzuchten (Nager, Insekten) die das gekochte Zeug mit Begier vertilgen ![]()
Hab auch inzwischen ein Feeling für das Köcheln, zumindest bei purem Roggen, jetzt mit dem Sittichfutter, der ganzen ungeschälten Hirse ist das natürlich noch nicht so.
Die erste Charge ist mir aber ganz gut gelungen glaube ich.
Die Presspelletts haben sich offenbar komplett aufgelöst, da ich geköcheltes Substrat im Sieb nach dem Köcheln, vor dem Abdampfen immer nochmal mit kochendem Frischwasser abspühle, hab ich die Menge des Spühlwassers diesmal einfach verdoppelt um möglicht alle Hinterlassenschaften der Pelletts herauszubekommen.
Ein paar Fotos :
Zwei möglichst nahe Aufnahme des Alb. A+ "Heimchendosencasings", stelle etwas erschreckt, zumindest verwundert viele viele weisse "Pünktchen" im Myzel fest... sind das nun erste Verdichtungen oder ein massives Kontiproblem ??

mich erstaunt die Anzahl der weissen Pünktchenj, sind sicher nicht mal eben zählbar... Hatte die Fruchtungsbox gestern mal eine h draussen, offen in der feuchten Regenluft sthen (natürlich ohne das was reinregnen konnte) um mal eine Sauerstoffdusche zu geben, beim wieder reinstellen gab es diese Punkte noch nicht.
Die beiden Golden T. Casings heute:
Und die jetzt gut gefüllte Fruchtungskammer:
Geschrieben von: Mister.T Sep 15 2015, 21:54
So wie deine beiden Golden T Cakes sieht meiner auch aus. Nur stehen sie seit knapp 10 Tagen in der Fruchtungskammer, aber nichts passiert :(
Geschrieben von: Herr von Böde Sep 15 2015, 22:13
Bis heute ist bei den schon seit einigen Tagen in der Box stehenden A+ Casings auch nicht mehr wirklich viel passiert, das Myzel hat deutlich langsamer zugelegt als noch in der Inkubation.
Aber das ist ja wohl auch ganz richtig so, wir wollen jetzt ja Fruchtkörper ![]()
Erst heute halt die weissen Pünktchen, was auch immer das ist. ![]()
Denke ein paar Tage Geduld noch dann wird sich bei Dir auch was tun ![]()
Geschrieben von: hogie Sep 16 2015, 04:54
Es sind ja relativ glatte Oberflächen, auch die potentiellen Problemstellen, die "Handchuhstutzen" -aufgeschnittenene und geteilte 500 ml Konservendosen ("Erbsensuppe" -war ne Qual das Zeug zu essen !!)- sind ziemlich glatt und sauber eingebracht.
Die Erbsensuppe zu essen, grenzt ja an Masochismus
An Glovboxes sind einfach viel mehr Ecken und Kanten, die immer ein Problem sind, wenn man nicht mit einem Gas desinfiziert. Aber ich glaube durchaus, dass du die sehr gut gebaut hast. Ein Bild davon habe ich jetzt nicht im Kopf.
Desweiteren musst du davon ausgehen, wenn du Haustiere hast, hast du schnell höhere Keimzahlen in deiner Bude. Für einen gesunden Menschen ist das absolut kein Problem, für eine sterile Petrischale, die du beimpfen willst aber schon. Ganz schlimm sind Haustiere, die Staub verursachen. Extremfall: Vögel.
Wenn du 2 Papageien in der Bude hast, brauchst du ohne Hepa erst gar nicht weiter machen und dann auch daran denken, dass sich der Staub nachts absetzt und tagsüber aufgewirbelt wird. Am frühen Morgen sind die Keimzahlen viel geringer. Nicht nur zu Hause, sondern auch in einer Arztpraxis. Für geplante Eingriffe mit irgend einer Infektionsgefahr solltest du dir einen möglichst frühen Termin aussuchen
Geschrieben von: Herr von Böde Sep 16 2015, 05:53
Ok, es geht bei der schwereren Desinfizierbarkeit der G.-box also um den verwinkelteren Aufbau und nicht etwa um das Material.
Alle heikleren Arbeiten (sprich Beimpfen, Überimpfen, Sporenabdrücke etc.) finden bei mir in einem komplett leeren, verschlossenen Raum (naja, ein paar Regale und Kisten mit Werkzeug aber nichts was staubt) hinter der Küche statt, der selten betreten wird.
Die Futtertierzuchten finden- zumindest Sommers- draußen statt.
Die Reptilien im Wohnzimmer stauben sicher nicht und die Terrarien werden penibel sauber gehalten. Der Hund kommt bis zur Küchentür.
Den Plan Zebrafinken mit in die Futtertierpalette aufzunehem ist also mal gestorben...(Papageienvögel würde ich sicher niemals verfüttern).
Den Tipp mit dem morgentlichen Arbeiten werd ich direkt mal umsetzen.
Wollte heute Abend ein paar Gläser und Petries ansetzen, werd das dann mal auf Donnerstag früh verschieben.
Geschrieben von: hogie Sep 16 2015, 06:06
Die Futtertierzuchten finden- zumindest Sommers- draußen statt.
Die Reptilien im Wohnzimmer stauben sicher nicht und die Terrarien werden penibel sauber gehalten. Der Hund kommt bis zur Küchentür.
Den Plan Zebrafinken mit in die Futtertierpalette aufzunehem ist also mal gestorben...(Papageienvögel würde ich sicher niemals verfüttern).
Den Tipp mit dem morgentlichen Arbeiten werd ich direkt mal umsetzen.
Wollte heute Abend ein paar Gläser und Petries ansetzen, werd das dann mal auf Donnerstag früh verschieben.
Das klingt alles soweit super gut. Ich weiß, dass du gut drauf bist und Kiddie- oder Dau-Fehler völlig unwahrscheinlich sind. Doch die Schwachstelle mit den massiven Hefekontis haben wir imho noch nicht gefunden. Zufall ist das nicht, das 100pro eine Schwachstelle in deiner Anordnung. Diese müssen wir bloß finden...
Geschrieben von: Herr von Böde Sep 16 2015, 06:32
Ja, ich bin mir inzwischen klar das zumindest bei den Petries ein erheblich Teil der Kontis schon bei der Abkühlung ins Agar geraten (das spricht sicher schonmal für eine relativ hohe Hefebelastung in der Raumluft):
Zuletzt (8.9.) 15 Petries nach erreichen des Normaldrucks in Alufolie belassen in die Glovebox überführt und auskühlen gelassen.
Nach 24h 11 Petries beimpft, aus 3 Ausgangspetries.
Ausgangspetrie 1: 4 beimpft, 3 Ausfälle durch Hefen
Ausgangspetrie 2: 4 beimpft 2 Ausfälle (Hefen)
Ausgangspetrie 3: 3 beimpft 1 Ausfall (Hefen)
(Box wurde zwischen Ausgangspetrie 2&3 1x kurz geöffnet, erneut desinfiziert und 15 min gewartet)
Alle Ausgangspetries sahen (und sehen noch heute, Löcher teilw. wieder überwachsen) klasse aus, was mich stutzig macht ist das es bei der letzten Ausgangspetrie die wenigsten Ausfälle gab.
4 Petries wurden nach dem Impfvorgang der anderen unbeimpft herausgenommen und mit Frischhaltefolie umwickelt, in einen Inkubator bei 32 gestellt und gestern Abend gegen 22:00 Uhr ausgepackt, alle hatten Hefekontis.
Das der DDKT richtig arbeitet schliesse ich erstens aus der Tasache das ich mit 1l Wasser locker 3h sterilisiern kann (ständige leichte Überdruckdampffahne auf Stufe 1 1/2), ausserdem sind sterilisierte Roggengläser mit Polyfil (also nicht unter Unterdruck) zumindest nach 14 tagen noch absolut frisch und wohlrichend.
Ich muss dazu sagen das dieses wieder eine extrem schlechte Petriecharge war, ich hab zwischendurch immer mal wieder welche mit nur 1-2 Ausfällen... macht alles noch ein wenig rätselhafter.
Die Petries die morgen Früh beimpft werden sollen (14 St.) wurden am Abend sterilisiert und bleiben nun bis unmittelbar vor der Verwendung im DDKT.
Mal schauen wie das wird.
Geschrieben von: Mister.T Sep 16 2015, 11:16
Wie sieht denn eine Hefekontamination aus ? vereinzelte Punkte oder saurer Geruch ?
Ich habe auch noch ein paar Anfängerfragen und wollte nicht extra ein neuen Thread aufmachen.
Ist es sinvoll in die Fruchtungskammer viele Löcher zu bohren ? Auf einigen Seiten wird dies empfohlen. Würde dadurch jedoch nicht die Luftfeuchtigkeit sinken und die Kontaminationsgefahr steigen ? Oder ist die Kontigefahr in diesem Stadium nicht so groß ?
Geschrieben von: Herr von Böde Sep 16 2015, 20:16
Also ich hab die Fruchtungskammer nicht angebohrt.
Es ist kein wirklicher Deckel darauf sonder die Kiste ist mit Frischhaltefolie bespannt.
2-3x tgl. öffne ich das ganze, wedel Frischluft rein (teilw. am offenem Fenster) wische das Kondenswasser von den Wänden (um die Keimrate gering zu halten) und besprüh neu (immer mit abgekochtem Wasser, dieses ist keimämer und viele Härtebildner sind ausgefällt).
Damit kein sich bildendes Kondenswasser in die Casings tropfen kann steht die Box etwas geneigt, so kann das Wasser nach vorne abrinnen.
Bilder von Hefekontis liefere ich nach :-)
Meist weissliche Schlieren und der typische fiese süß-saure weinartige Geruch.
Wenns ganz arg ist bzw. ein älteres Glas bilden sich gern mal Blasen.
Kontis in Punktform weisen wohl ehr auf Schimmel oder Bakterien hin,
wobei Schimmel schnell in pilzartiger Weise wächst und Bakterien stärker abgegrenzt sind und (in den 1-2 Fällen die bei mir auftraten) sehr langsam wachsen.
Hefe-Kontis:
etwas älter, Petrie vom 29.08:
Edit 20:16 Uhr :
So, da ich nirgendwo Teppich habe, wurde jetzt die gesamte Bude mal mit Klorix gewischt (1l -5%ig auf 5 l -kaltem- Wasser), der Duft hier stimmt schonmal auf die kommende Hallenbadsaison ein ![]() .
.
Frage mich grade ob ich den DDKT nochmal anschalte, werd das aber wohl lassen, so gewaltig wird der Luftaustausch im Topf nicht sein, ausserdem sind die Petries in mehre Schichten (vorher befeuchtete) Alufolie gewickelt. Beim Öffnes des Topfes morgen Früh werd ich das Petriepäckchen mit Klorix pur einsprühen...
Geschrieben von: hogie Sep 16 2015, 22:52
Das würde ich nicht machen, denn Aluminium und Natriumhypochlorid reagieren miteinander.
Geschrieben von: Herr von Böde Sep 17 2015, 08:12
Wow, es sieht doch tatsächlich so aus als entwickeln sich aus den weissen Pünktchen Primordien, ist wohl einfach das fehlende Pigment des Strains das die so schimmelverdächtig aussehen lässt, die Menge überrascht aber auch, wird wohl unzählige Aborts geben:



Edit 06:01 Uhr:
Die Aktion beginnt.
Mir fällt grade ein weiteres nicht unwesentliches Argument für nen Hepafilter auf:
Die nötige Zeit.
Es werden von einer Petrieschale mit selektiertem GT Myzel 4 Gläser und 4 Petries beimpft, das gleiche von einer Petrie mit selektiertem A+ Myzel.
Von 2 Petries mit unselektiertem PF-orig. Myzel sollen ebenfalls jeweils 4 Gläser und 4 Petries beimpft werden.
Da mit mehr als 4 Gläsern bzw. 8 Petries + den jeweiligen 2 Ausgangspetries nicht sinvoll in der Box gearbeitet werden kann, sind mehre Durchgänge mit Öffnen, erneutem Desinfizieren und 15-20 minütiger Einwirkzeit nötig.
Da ich sicherlich zwischendurch mal ne länge Pause mit Frischluft brauche wird der Vormittag dafür draufgehen...
Nur eine gut funktionierde Flümymethode wäre eine langfristige Alternative zum Filter, denke ich.
Edit 08:09 Uhr:
Hab mich entschieden jetzt erst mal zumindest die Ergebnisse der 8 Gt und A+ Petries abzuwarten bevor ich mit dem PF.orig. Myzel weitermache.
Hab grad auch schlicht keine Lust mehr ... ![]()
Geschrieben von: hogie Sep 17 2015, 14:06
Um gut funktionierende Flüssigmycelien herzustellen, sind noch viel höhere Anforderungen an Sterilität nötig. Ich empfehle Gläser mit Mycelstücken aus Petris zu beimpfen.
Denn was du auf einer Petri sofort siehst und noch sauber überimpfen kannst oder einfach eine saubere Petri nehmen, das verteilt sich gleichmäßig in deiner ganzen Flasche Flüssigmycel.
Geschrieben von: Herr von Böde Sep 17 2015, 16:18
Die Überlegung ist halt das zum Beimpfen des Flüssignährmediums nur 1x annhäernd perfekte Bedingungen herrschen müssten und sämtliche Gläser die dann mit dem Flümy beimpft werden mit sehr wenig Aufwand einfach durch Impfports angesetzt werden könnten.
Trotzdem, ich verspreche: Weitere Experimente mit Flümy wirds erst mit Hepafilter geben. ![]()
Geschrieben von: Dioxis Sep 17 2015, 20:30
Du wohnst wohl im OP ?
Vielleicht schaffen es sehr gebüte Hände entsprechend schnell zu arbeiten und damit Kontis beim Beimpfen ohne Glovebox oder Hepa vor Fremdkeimen zu schützen, ich hab immernoch hohe Kontiraten (immer Hefe soweit ich das beurteilen kan) wenn ich in der Glovebox beimpfe, egal ob mit 70-80%igem Ethanol oder mit Klorix desinfiziert wird.
Wie das mit einem Bunsenbrenner funktionieren soll ist mir überhaupt nicht klar, der schafft ja erst zusätzliche Luftverwirbelungen und ich glaube nicht das ich damit Erfolg haben könnte.
Da scheint mit das Arbeiten im Wasserdampf noch einleuchtender, weil der Dampf ein größeres (auch noch gut sichtbares)Volumen einnehmen würde das Kontis fernhält.
Inkubatoren habe ich in ausreichender Menge und Größe (züchte auch noch Reptilien).
Mir gehts beim Hepa in erster Linie um die Bequemlichkeit, sobald werd ich mir aber wohl keinen zulegen.
Bin im Moment dabei Kontiqellen mittels Petries zu ermitteln, irgentwo ist nach wie vor der Wurm drin.
Morgen werd ich 9 Gläser mit bewachsenem Agar beimpfen und- wohl auf Kosten der Durchwachszeit, dafür muss der Glasdeckel aber kürzer angehoben werden- nur mit einem Stück (etwa 1/3 8cm Petrie) impfen.
Steriles umfeld ist unnötig wenn man sich nicht mega anstellt oder anfängerfehler macht (nie mit dem Arm über Medien greifen u.a.)
Schnell arbeiten muss man auch nicht, beim aussparteln von Infektionsflüssigkeit stehen Agarplatten auch mal mehrere Minuten lang offen (natürlich nicht komplett, aber halt ca. 2cm angehoben).
Ich hab das so in der Ausbildung gelernt (von ordentlichen Doktoren der Biologie mit langjähriger Berufserfahrung, das hat schon Hand und Fuß), wir haben Agarplatten mit Vollmedium für Bakterien oder Pilze nie unter einer Sterilbank gegossen oder bearbeitet und die Ausfallquote war bei 100 Platten vieleicht 4.
Auser für Pflanzliche und Tierische zellkulturen war es schlicht unnötig.
Wir hatten zwar (unsterile aus ner zupfbox) Handschuhe an, haben damit aber auch zwischendrin alles mögliche andere angefasst, z.B. bei erkältung geschneuzt und dann hatt sich niemand vor dem weiteren Arbeiten die Handschuhe desinfiziert.
Beim Aufbereiten wie z.B. Plasmide isolieren haben wir auf handschuhe sogar ganz verzichtet.
Speziell gefilterte Luft oder so hatten wir auch nicht, wenn alle am Bunsenbrenner standen haben wir einfach die Fenster aufgemacht, weil es schnell ziemlich warm im Labor geworden ist.
Ein Kollege von mir züchtet psilos im etwas größeren masstab Zuhause (im Wohnzimmer) ausschließlich mit Bunsenbrenner und Desinfektionsmittel zum Arbeiten.
Ob Platten, Flüssigkulturen oder Säcke mit Roggen, die Kontaminationsrate ist vernachlässigbar.
Er hatt zwar eine Grovebox, aber die nutzt er nur für Sporenabdrücke.
Hab auch schon selbst für ein parr Trips welche mit dem Bunsenbrenner, DDT, H2O2, Sterilum und Bacillol zum sterilen arbeiten rangezogen.
Nährmedium in nem sauberen (nichtmal steril nur mit H2O2 kurz gespült) Becherglas auf dem Herd in der Küche angerührt und einfach unter der Bunsenbrennerflamme in saubere Einmalpetris gegossen.
Nach dem auskühlen, festwerden und autoklavieren habe ich es (ebenfalls unter der Flamme) mit etwas sporenlösung von besagtem Kollegen beimpft, das ganze Gründlich ausgespartelt und 0 von 5 Platten waren nach dem inkubieren in meinem Kleiderschrank kontaminiert.
Anschließend (wenn wunderts, wieder nur unterm Bunsenbrenner), mit einem Abgeflammten Skalpell (Einmalteile sind Geldverschwendung, wir haben die im Labor auch nur gewechselt, wenn sie stumpf waren) die vielversprechendsten Kolonien ausgeschnitten und in Boxen mit Roggen und Vermiculit überführt (zusammen im DDT sterilisiert, die boxen waren billigteile von Azarius und gebraucht, sind nichtmal Formstabil im DDT, aber solange der deckel dicht schließt kein Problem).
Von 3 Boxen auch kein einziger Ausfall (als Fruchtungskammer diente ein Standartbeutel mit luftfilterpatch, wie man sie zum anzüchten großer Mengen kultur auf Roggen u.a. benutzt.)
Alles Besteck wie Skalpelle und Impfösen erst in Spiritus tunken und dann abflammen, die Behältnisse und Medien im DDT gut Autoklavieren, nicht unbedingt auf die Platten husten, mit dem Finger drauf tatschen oder mit dem Ärmel drüber langen und schon kann man stressfrei, extrem billig und sicher arbeiten.
Früher dachte ich auch ich brauche mindestens eine Grovebox um auch nur annährend annehmbare Ergebnisse zu bekommen, mittlerweile halte ich es für unnötig und umständlich, solange man nicht im Industiemasstab züchten will.
Die Chance sich mit einer zusammengeschusterten Grovebox oder einem gegebenenfalls schlecht gelagertem billigen Hepafilter eine Konti zu holen halte ich für höher.
Kann natürlich sein, das ich und vorallem mein Kollege einfach abartig viel Glück haben, aber das halte ich für sehr weit hergeholt.
Ps: Probier mal deine Box mit 30% H2O2 sauber zu machen, sag dem Apotheker einfach du willst damit im Bad schimmel aus den fugen entfernen, bis jetzt hat es mir noch jeder verkauft.
Und bring dich nicht mit dem Chlorzeugs um
Geschrieben von: Herr von Böde Sep 17 2015, 22:03
Dioxis, ich glaub Dir das alles gern, nur ich hab teilw. schon Hefekontaminationen in sterilisierten Petries die niemals geöffnet wurden,
einfach nur nicht im DDKT auskühklen konnten.
Ich denke vieles hängt auch sehr von der Umgebungsluft ab, ich wohne in einem Altbau und habe offenbar eine hohe Belastung mit Hefen in der Raumluft.
Seltsam finde ich halt das es immer diese Hefen sind, im Vergleich mit Schimmel sollten die doch recht leicht zu killen sein. Schimmlige Petries hatte ich bisher vielleicht 1 oder 2, Substratgläser gar keins, 1nen verschimmelten Mikrofilterbeutel...
H2O2 habe ich tatsächlich noch nicht getestet, werde ich machen wenns jetzt wieder so große Probleme gibt.
Ich würd das online bestellen, um Apotheken mache ich nen Bogen...
ps. natürlich nicht zu veressen die verschimmelten Pf-Cakes die mit frischem Roggen zu Casings verarbeitet wurden- aber da liegt der Fehler ja auf der Hand...
Geschrieben von: hogie Sep 18 2015, 01:39
wenn du endlich saubere Petris hast, kannst du das leicht testen
In Alufolie eingewickelte und darin autoklavierte Petris haben bei mir eigentlich ganz gut gehalten. Dass Partikel durch die Ritzen gezogen werden, ist eigentlich nur bei häufigen Druckänderungen denkbar. Häufige stärkere Temperaturänderungen haben natürlich den gleichen Effekt. Ansonsten sollen die Ritzen nicht feucht sein, denn sonst könnte auch etwas durch wachsen.
30% H2O2 verwendet man auch in der Lebensmittelindustrie beim Abpacken . Dass es schneller geht, wird es dort sogar meistens heiß angewandt. Du darfst es halt nicht auf die Haut bringen und mit sprühen musst du sehr vorsichtig sein. Eingeatmetes Aerosol birgt die Gefahr eine Lungenödems.
Ansonsten eignet sich noch Tyvek als ganz hervorragende Sterilverpackung. Es ist kontidicht, wasserdicht, im Schnellkochtopf noch locker temperaturbeständig, kann geschweißt und geklebt werden, ist hoch dampf- und gasdurchlässig und ganz einfach in kleinen Mengen in Form von Tyvek-Briefumschlägen zu beschaffen. Darin hatte ich auch häufig Petris.
Geschrieben von: Herr von Böde Sep 18 2015, 05:25
Ja, ich bin mir inzwischen klar das zumindest bei den Petries ein erheblich Teil der Kontis schon bei der Abkühlung ins Agar geraten (das spricht sicher schonmal für eine relativ hohe Hefebelastung in der Raumluft): Zuletzt (8.9.) 15 Petries nach erreichen des Normaldrucks in Alufolie belassen in die Glovebox überführt und auskühlen gelassen.
Nach 24h 11 Petries beimpft, aus 3 Ausgangspetries.
Ausgangspetrie 1: 4 beimpft, 3 Ausfälle durch Hefen
Ausgangspetrie 2: 4 beimpft 2 Ausfälle (Hefen)
Ausgangspetrie 3: 3 beimpft 1 Ausfall (Hefen)
(Box wurde zwischen Ausgangspetrie 2&3 1x kurz geöffnet, erneut desinfiziert und 15 min gewartet) Alle Ausgangspetries sahen (und sehen noch heute, Löcher teilw. wieder überwachsen) klasse aus, was mich stutzig macht ist das es bei der letzten Ausgangspetrie die wenigsten Ausfälle gab.
4 Petries wurden nach dem Impfvorgang der anderen unbeimpft herausgenommen und mit Frischhaltefolie umwickelt, in einen Inkubator bei 32 gestellt und gestern Abend gegen 22:00 Uhr ausgepackt, alle hatten Hefekontis.
Das war der Test
Petries von gestern sehen bei konstant 28 Grad C. noch sauber aus, wenns morgen um die Zeit noch so ist sind die hefemäßig über den Berg...
Edit:
Man kann aus obigem Ergebniss wohl einfach schliessen, das die Kontis nicht beim Beimpfen ins Agar geraten, denn die unbeimpften Gläser vielen total aus wärend es bei den Beimpften immerhin die eine oder andere kontifreie Petrie gab.
Die Infektion muss wohl in der kurzen Zeit des Überführens der heissen Gläser in die Glovebox stattgefunden haben oder eben wärend des 24stündigen Abkühlens bzw. der Lagerung in derselben, darum blieben die Petries von gestern bis zuletzt im DDKT.
Muss aber dazu sagen das die Unbeimpften zusammen in Frischaltefolie gewickelt und nicht einzeln verschlossen wurden. Aber nach dem Umwickeln dürfte da keine große Luftbewegung mehr stattgefunden haben.
Die Petries standen die ganze Zeit wärend des Beimpfens der anderen Petries in der Glovebox noch original eingepackt in Alufolie, so wie sie aus dem Topf kamen.
Geschrieben von: hogie Sep 18 2015, 13:42
Dann müsste die Lösung sein, wenn du Petris in einer Sterilverpackung aus Tyvek sterilisierst. Denn die Schnellkochtöpfe lassen auf jeden Fall Raumluft in Innere, sobald der Überdruck weg ist.
Wenn du Gelrite statt Agar nimmst, der wird einmal bei Gießen fest und ist dann mehrfach autoklavierbar ohne mehr zu schmelzen. Du kannst in diesem Fall die Petris heiß aus dem DDKT entnehmen. Hefen sollten eh nicht viel aushalten, eine einfache Pasteurisierung sollte da schon reichen. Bei z.B. 80°C kannst du sie mit einem Isolierhandschuh locker aus dem Wasserbad entnehmen. Viele Lebensmittel pasteurisiere ist gewöhnlich bei ca. 98° und entnehme die Gläser. Man muss aufpassen, dass man beim Öffnen des Deckels keine Dampfschwade abbekommt. Das Entnehmen geht prima mit einem Isolierhandschuh. Weil ich keinen wasserdichten habe, mache ich noch eine Plasiktüte dazwischen. Denn saugt er sich mit heißem Wasser voll oder man langt gar ins Wasserbad, dann wird es ziemlich heiß ![]()
Geschrieben von: Herr von Böde Sep 18 2015, 19:20
Ok, Tyvek hatte ich eh schon auf der Liste, wird auch mal getestet und mir nen Quatratmeterpreis von 1,40-E sicher kein rausgeworfenes Geld.
Die Petries sehen immer noch klasse aus, ich glaube fast Kontimässig passiert da nicht mehr viel. Teilw. wächst bereits Myzel vom Impfstück auf das Arar...
Werd demnächst aber wieder die empfohlen 25g Arar/1l benuten, hatte diesmal auf 20g reduziert und hab jetzt fast überall Restwasser (kein Kondenswasser) in den Gläsern.
Mal was hübsches, wer Langeweile hat darf Pins und junge FK zählen :

Geschrieben von: hogie Sep 18 2015, 22:49
Ich habe mal in meiner Doku nach geschaut, doch ca. 25g/l habe ich damals auch verwendet. Es war Agar aus dem Asialaden.
Geschrieben von: Herr von Böde Sep 19 2015, 11:05
Meins ist ausm Reformhaus, wird nicht das schlechteste sein für rund 6,-/50g.
Und wenn das jetzt mal besser klappt, sich herausstellt dass das Auskühlenlassen im DDKT schon ausreicht, sollte ich schon ne Weile auskommen mit 1-2l Arar.
Hab in den 8cm Petries immer 15 ml, mehr würd überkochen, weniger trocknet zu schnell ein.
9 Petries für 2 Ausgangsgläser mit PF.orig. Myzel sind grade von der Platte gestellt worden. Morgen Früh nochmal ein bissl Arbeit und dann mal abwarten, auch wie es sich in den Roggen/Hirse Gläseren entwickelt.
Hab die Gläser- und werd das auch morgen so machen- mit jeweils einem größeren bewachsenem Agarstück (1/8 einer Petrie) beimpft, mit der bewachsenen Seite nach unten einfach aufs Substrat gelegt, einfach der Geschwindigkeit wegen.
Wenn sich deutliches Wachstum zeigt wird mal geschüttelt.
Edit 08:52 Uhr:
So, nochmal 11 Substratgläser und 9 Petries fertig.
Werd den Inkubator jetzt mal 3 bange Tage unberührt lassen und dann entweder sehr froh oder ziemlich entteuscht sein ![]()
Petries von Vorgestern sehen nach wie vor gut aus, abgesehen vom freien Wasser.
Man sollte wirlich nicht zu viele Parameter pro Durchgang verändern wenn man sich an ein Ziel herantastet...
Aber das Myzel wächst bereits von allen Impfstücken auf das Agar, so das die Gläser kopfüber gedreht werden konnten.
Geschrieben von: Herr von Böde Sep 21 2015, 13:48
Weils so schön ist ![]()
AA+ Heimchendosencasing
AA+ Quarkdosencasing 1
AA+ Quarkdosencasing 2
AA+ Quarkdosencasing 3
Bin überrascht das im "Heimchendosencasing" die Fks doch größer werden als gedacht, die eigendliche Substratschicht ist max. 1-1,5 cm dick.
Wird sich dann wohl an der Anzahl der Flushes bemerkbar machen.
Gibts eine Faustregel für die Dicke der Substratschicht (also für das Substrat aus den Gläsern, zwischen Perliteboden und Abdeckschicht) ?
Wie dünn darf sie sein bzw. ab welcher Dicke wird eine Vergrößerung sinnlos oder gar kontraproduktiv?
Möchte ehr auf 2l Schalen umsteigen, sind darauf vier 430 ml Substargläser ein vernünftiger Richtungswert (Gläser sind ja nie 100%ig voll)?
Die beiden GT-Casings zeigen auch die ersten Myzelverdichtungen, wenn ich nicht irre. Die sind auch weiss aber sehr viel weniger von der Anzahl. Fotos wenn die ersten Pins spriessen ![]()
Geschrieben von: hogie Sep 21 2015, 15:44
Sieht super aus! Ich bekomme fast Lust, auch mal wieder ein Paar Wichtel zu growen. Vielleicht auch wieder den südlichen Schüppling. Die Getreideschicht empfehle ich nicht zu geizig zu machen. Denn das durchwachsene Getreide ist nahezu unkontaminierbar. Man kann auch einfach durchwachsene Gläser fruchten lassen. Allerdings ist das Getreideverschwendung, weil Pilze zu 90% aus Wasser bestehen. Deshalb ist das andere Optimum, wenn man Verluste durch Kontis außer Acht lässt, dass Wasser und Nährstoffe gemeinsam zur Neige gehen. Als Richtwert kannst du die Rezepturen der PF-Tek heran ziehen.
Geschrieben von: Herr von Böde Sep 21 2015, 16:12
Danke Hogie ![]()
Deine Aussagen bezüglich der Substratdicke verstehe ich leider grad gar nicht so richtig, bzw. gehen die etwas an meiner Frage vorbei :
Also bevor ich im Glas fruchten lasse würd ich ja ehr wider auf PF-Tek umstellen, die minimale freie Oberfläche eines Glases kann keine höheren Erträge liefern als die eines "freien" Pf-Cakes gleicher Größe ![]() ??
??
Ausserdem möchte ich die Gläser ja gern wider frei haben ![]()
Wie meinst Du das mit dem Richtwert von PF Rezepturen?
Dort arbeitet man ja mit trockenen Ausgangszutaten.
Etwa 2-1-1 (Vermi.-Reism.-Wasser)... ich würde also das Wasser bei der Übertragung der Verhältnisse auf ein Casing schonmal aussen vor lassen.
Der Rest hiesse dann in etwa 1Teil Boden, 1Teil Getreide, 1 Teil Deckschicht... ok so oder ähnlich hab ichs auch schon oft gelesen.
Worauf ich mit meiner Frage aber hinauswollte waren soetaws wie Minimal-bzw.- maximal - und schließlich -optimalwerte ![]() für die Schichten,
für die Schichten,
insbesondere für die Getreideschicht.
Könnte mir zB. vorstellen das 15cm Boden, 15 cm Roggen, 15 cm Deckschicht keinen wirklichen Sinn machen, weil (das ist die Frage) zB. die unteren 5-10 cm Roggen kaum noch Einfluss auf die Ernte haben?
Das andre Extrem : Schichten grad so dick wie ein durchwachsenes Getreidekorn, das ganze wird wohl sehr schnell vertrocknen und der Ertrag (wenn da überhaupt was wächst ![]() ) wäre die Mühe nicht wert.
) wäre die Mühe nicht wert.
Ich hab vor ca. 15 Jahren mal eine Growbox gehabt, hab es damals aber leider versäumt mir den Aufbau mal genauer anzusehen.
Kann mir vorstellen das die schon ziemlich sinnvoll zusammengestellt sind, hat das evtl. schonmal jemand nachgemessen?
Geschrieben von: hogie Sep 21 2015, 17:56
Die Angabe in cm ist natürlich auch so nicht extrem sinnvoll, weil das vom Gefäß abhängt. Die Growboxen haben gewöhnlich unten Perlit, dann eine eher geizige Schicht (die durchaus etwas dicker sein kann) durchwachsene Körner und oben Vermiculit.
Wir haben hier doch gerade jemand im Forum, dessen Großbox nach 5 Flushs am Ende ist. Er soll sie zerschnippeln und nach messen ![]()
edit: oben verschrieben, Deckschicht ist natürlich Vermiculit
Geschrieben von: Herr von Böde Sep 23 2015, 04:29
Alles klar, hab da mal nen Thread aufgemacht ![]()
Also meine zukünftigen Schalen sollen in etwa solche sein, 2-2,5l -
(innen) etwa 21cm(L) x 15 cm(T) x 9,5cm(H) :
Je 3cm pro Schicht dürfte also etwa passen.
Wobei mir eine 3cm Abdeckschicht ziemlich gewaltig vorkommt, erst recht ein 3cm Boden... oder passt das schon?![]()
Nur 1 Ausfall einer PF-orig Petrie!! Für mich die bisher mit Abstand beste Impfaktion (beim teilw. falschen Datum -Monat- nicht verwirren lassen,
hab mir da wohl eine Verlängerung des Sommers gewünscht) ![]() :
:
4vov4 AA+
4von4 GT
5von5 PF-o. aus Petrie I
3von4 PF-o. aus Petrie II
Des Wassers wegen großteils kopfüber geknipst.
Alles sauber !! ![]()
Zur Feier des Tages stelle ich mich auf eine hochdosierte Reise heute Abend ein, evtl. gibts an dieser Stelle nen Live-tripbericht (solange ich kann ![]() ):
):
Edit:
So, das Heimchendosencasing brachte im ersten Flush 73g. ![]()
--------------------------------------------------------------------------
Trippbericht 19:00 Uhr
Ich kaue grad diese exakt 2g trockenen Pf.orig, rechts danaben ein einzelner A+.
Die stammen noch von den Pf Cakes und werden qualitativ sicher nicht besser ![]() :
:
Dannach werd ich 15g dieser Frischpilze zu mir nehmen:
Normalerweise halte ich nicht so viel vom späteren Nachlegen aber 25 g werd ich wohl in ca 45min noch drauflegen.
Toleranz dürfte bei mir derzeit keine vorhanden sein und da es das erst mal ist das ich trockene und frische Pilze, auch noch unterschiedliche Strains kombiniere, fange ich mal "vorsichtig" an.
19:02 Uhr ich finds wirklich nicht ekelig, erste Portion ist runter ![]()
Kurz noch was zum Set und Setting, bin alleine in meiner (unfallgesicherten) Wohnung, werd mir zum Hochfahren diesen alten Schicken http://www.veoh.com/watch/v39012655mSj9JRmc?h1=Flucht+ins+23.Jahrhundert+%281976%29 antun, ich glaub wie gemacht fürn Trip, nüchtern nicht unbedingt jedermanns Sache (wahrscheinlich verlier ich aber irgendwann das interesse -oder den Faden ![]() )
)
Edit 19:34 Uhr
ziemlich schlagartig sind die ersten Wirkungen spürbar, hui, das Schreiben (tippen) wird kompliziert ![]()
Edit 19:52 Uhr
15g (frisch) nachgelegt. Das sollte erstmal reichen ![]()
Edit 20:40 Uhr
lol, ich weiss wieder genau warum ich kein Freund des "Nachlegens" bin...
natürlich ist die Wirkumng weitgehnd ausgeprägt, aber nicht "überwältigend" und dieses "Überwältigt werden" macht für mich nen guten Trip aus.
blöderweise kann ich auch nicht mehr vernüftig kalkulieren was zu diesem zeitpunkt eine sinnvolle Menge zum nachlegen wäre ![]()
also, lieberf kurzer Prozess und nochmal 30g Frischpilze am kauen bin...
Für Anfänger sicher nicht die empfehlenswertestete Vorgehnsweise ![]()
Edit 21:27 Uhr
Ok, der Trip spitzt sich jetzt eindeutig nochmal zu.
Weitere Edits wohl erst nach dem Peak ![]()
Edit 23.09 um 04:00 Uhr
Ich bin grade aufgewacht, völlig nüchtern, auch wenn ich mich grad nicht unbedingt hinters Steuer setzen würde ![]()
Ich muss zwischen 23:00 und 00:00 Uhr tatsächlich eingeschlafen sein^^.
Unterm Strich hätte ich mir die letzten 30g Frischpilze sparen können, der Trip gewann zwar tatsächlich nochmal deutlich an Intensität aber flachte dann unverhältnissschnell auch wieder ab.
Ein typischer "nicht genug" Trip, Gedanklich drehte sich ab 20:40 Uhr fast alles nur noch um die (für mich) unkorrekte Dosierung.
http://www.veoh.com/watch/v39012655mSj9JRmc?h1=Flucht+ins+23.Jahrhundert+%281976%29 ist angetrippt wirklich ein sehr interessanter Film ![]()
Geschrieben von: Herr von Böde Sep 24 2015, 11:38
Das erste Dosen A+ Casing ist heute soweit, mehr aber dafür etwas kleinere Fks als im "Heimchendosencasing":
Die GT- Casings haben deutlich länger gebraucht, erst heute die ertsen Pins:

Geschrieben von: Herr von Böde Sep 26 2015, 08:47
Alls A+ Casings sind abgeerntet, die Ergebnisse durchaus unterschiedlich:
Heichmchendose 76g
Qarkdose I :41 g
QD II : 72 g
QD III: 61 g
Durch den Feuchtigkeitsverlust war in den letzten Tagen der Flushes ein Zusammenziehen der Substratkuchen deutlich zu erkennen. Teilweise beträgt der Zwischenraum zwischen Substrat und Dosenrand 0,5 cm.
Wahrscheinlich wäre das bei einer rein mineralischen Abdeckschicht , also Vermiculite nicht der Fall weil dies im Ggs. zum Cocohum kein Volumen verliert wenn es trockener wird.
Meine Mischung besteht etwa hälftig (vol.) aus beidem.
Zwei Fragen dazu:
1. Sollte ich den Vermiculiteanteil in folgenden Deckschicht erhöhen um dieses Problem zu verringern?
2. Macht es Sinn die entstandennen Zwischeräume mit frischer Abdeckerde oder mit reinem Perlite aufzufüllen?
Geschrieben von: hogie Sep 26 2015, 15:41
Ich würde den Zwischenraum mit Vermiculit auffüllen, denn die Wichtel neigen dazu, beim nächsten Flush genau dort Fruchtkörper zu bilden. Es spricht auch nichts dagegen, die Abdeckung aus purem Vermiculit zu machen. Perlit ist ungeeignet, weil es nicht lebensmitteltauglich ist.
Geschrieben von: Herr von Böde Sep 28 2015, 09:43
Ok, ich habe das mal im Zuge des Dunkens versucht, ist aber eine ziemliche "Prökelei", denke das richtet mehr Schaden an als das es nutzt ![]()
Auch wenn das Cocohum Volumen beim Trocknen verliert kann es doch sicher auch im durchwachsenem Zustand mehr Feuchtigkeit beim Dunken absorbieren als reines Vermiculite, oder teusche ich mich da? Dachte das wäre der Vorteil daran ![]()
Aber gut, bin ja soweit schon recht zufrieden.
Nächster Schritt wird es sein isolierte Genetik zum fruchten zu bringen, dann kann ich ein wenig experimentieren und mir viele Fragen am Ende auch selbst beantworten ![]()
Edit 20:49
Ich lauere nicht täglich in die Inkubatoren (1x Petries, 1x Gläser) um dann ein gewisses Erfolgserlebniss zu haben, wenn sich gut was getan hat.
Eine Überraschung erlebe ich jetzt grade beim betrachten der Gläser vom 17. und 19.09.
Ein Glas mit GT-1 Myzel hat einen Schimmelkonti (irgendetwas blau-günes), sonst sieht alles gut aus(endlich mal wieder was anderes als Hefen ![]() ---wobei ich wette, wenn ich das Glas öffne-morgen an der Tonne- wird meine Nase um das Hefearoma nicht herumkommen
---wobei ich wette, wenn ich das Glas öffne-morgen an der Tonne- wird meine Nase um das Hefearoma nicht herumkommen ![]()
![]() ) .
) .
Was aber wirklich begeistert ist das dieses GT-1 Myzel, welches ich vor ein paar Tagen noch als "nicht das schnellste" bezeichnet habe, in 9 Tagen bei 28 Grad richtig Gas gegeben hat (wahrscheinlich wurds dem Pilz auf dem Agar einfach langweilig ![]() )
)
Alles andere ist nichtmal annäherd so weit.
Hier das Kontiglas, die 3 anderen Gt-1 Gläser sehen fast noch besser aus, haben auch keine Kontis:


Edit:
Mir ist inzwischen klar das ich dieses Hobby ein wenig ambitionierter verfolgen werde, es wird wohl bald die Ausweitung auf Speisepilze (die können einfach auch in kürzerer Zeit sinnvoll verwertet werden) folgen.
Insbesondere wird mich sicher die tatsächle Zucht beschäftigen, was hier passiert ist ja im Prinzip nur ein Weitervermehren und "am Leben halten" - wenn es um isolierte Genetik geht.
Ich bin also gedanklich schon ein bissl weiter.
Eine wichtige Frage dabei ist sicher die nach der Gewinnung von monokaryotischen Hyphen.
Wahrscheinlich werd ich nicht um das Wälzen von Fachliteratur herumkommen aber evtl. hat hier schon jemand ähnliche Versuche unternommen und hat ein paar Tips?
Ich gehe erstmal davon aus das man dabei nicht um das Isolieren einzelner Sporen herumkommt, was für eine Optik ist dafür wohl nötig
und welches Werkzeug?
Für Tipps (auch Hinweise auf gute Literatur) oder Links (hab nicht sehr viel gefunden) wäre ich dankbar ![]()
Edit 28.09. 09:43 Uhr
Nach dem insgesamt 2ten, diesmal sehr gründlichen Schütteln vorgestern sehen die 3 verbliebenen Gläser mit dem GT-1 Myzel heute morgen so aus:
Im mittleren Glas gut die Größe des Impfstückes (bei allen vergleichbar) zu erkennen, die werden beim Umfüllen wohl herausgefischt.
Ich denke Mittwoch oder Donnerstag sind die bereit zum Casen ![]()
Edit:
Noch ein Bild der Fruchtungsbox:
Vorn links und rechts die langsam spriessenden GT, in der Mitte setzt der zweite Flush des A+ "Heimchendosencasings" an (hatte eine neue sehr dünne Casingschicht aufgetragen, weil das Ernten die Deckschicht teilw. bis auf den Roggen aufgerissen hatte). Hinten die 3 anderen A+ Casings, die durch Flüssigkeitsentzug entstandenen Zwischenräume waren nicht gut aufzufüllen, so hab ich die Ränder etwas dicker mit Vermiculite bedeckt in der Hoffnung das kein idealer Gasaustausch in den Zwischenräumen entsteht, der CO2 Gehalt steigt und das Myzel so vom Fruchten abgehalten wird...natürlich erhöht stickige, feuchte Luft in den Hohlräumen auch die Schimmelgefahr. Naja, alles mal austesten ![]()
Wies aussieht muss (wenn in den vorhandenen Casings nichts Schimmelt) bald eine 2te Fruchtungsbox eingerichtet werden. ![]()
Geschrieben von: hogie Sep 28 2015, 13:41
Geschrieben von: Herr von Böde Sep 28 2015, 14:09
Das ist vielleicht ein wertvoller Tipp, danke !
Ich glaub aber ich hab chemisch weitgehend alles abgetötet was da im Glas war:
Ich hatte schlicht keine Lust auf irgendwelche fiesen Düfte beim Leeren des Glases, so hab ich 3x 25 ml Chlorix pur durch das Polyfil ins Glas gespritz und am Ende auch das Polyfil selbst damit durchtränkt, 1x kräftig geschüttelt und ne Stunde stehen lassen.
Das Chlorix bewirkt das es ersten gut aus dem Glas rutscht, nicht fies organisch stinkt und weitgehnd alles abtötet.
Ich hoffe mal die Maßnahme war ausreichend... ![]() .
.
Geschrieben von: Herr von Böde Sep 29 2015, 20:25
Die GT-1 Myzel Gläser heute:
Morgen wird gecased. Nur im mittleren Glas noch ein oder zwei freie Stellen, da das Bild heute Mittag gemacht wurde gehe ich sogar fast davon aus das auch diese inzwischen bewachsen sind.
Bin grad dabei noch 4 Substratgläser zu sterilisieren, werd dann morgen Vormittag vor dem Casen ein fertig durchwachsenes Glas in der Glovebox öffnen um mal die direkte Impfmethode (jeweils 1 Tl des durchwachsenen Substrates auf ein frisches Substratglas) zu testen. Werd dazu auch tatsächlich 4 Teelöffel, einzeln in Alufolie sterilisiert verwenden.
Ich möcht einfach wissen wie hoch die Kontirate ist, obs evtl sogar ohne Ausfälle klappt und ausserdem möchte ich dem Myzel noch etwas Zeit geben bevor einzelne Körne wider Zwecks Lagerung und Sicherung auf Agar landen.
Ausserdem habe ich beim Lüften der Fruchtungskammer grade bemerkt das meine vermeindlichen Golden Teacher bereits mit eingerissenem Velum Sporen verstreuen und habe deshalb diese 5,6 g Pilze abgeerntet:
![]()
Ich schliesse aus dem Aussehen und dem recht hohen Gewicht der mini Fk das mir mal wider etwas sehr typisches passiert ist: ein dämlicher Flüchtigkeitsfehler (beim Beschriften der Gläser).
Golden T. sollten deutlich größer werden bevor das Velum reisst, ziemlich sicher habe ich hier PF-orig Wichtel vor mir ![]()
Ein weiterer Teil kann wohl morgen geerntet werden, ich habe aber bei beiden Casings den Eindruck das einzelne Flushes evtl. nicht sehr stark zeitlich voneinander abgegrenzt sind, es erscheinen stetig neue Pins die auch zulegen.
Geschrieben von: Mister.T Sep 29 2015, 20:35
Die meisten Cubensis sehen ähnlich aus. Das Aussehen der Fruchtkörper hängt von weit mehr Faktoren ab. Dazu gehören Luftfeuchtigkeit, CO2 Gehalt, Licht und Substratgröße. Die Gene spielen auch noch eine große Rolle. Falls die FK aus Sporenspritzen entstanden sind, ist es gut möglich, dass dabei kleine Dicke rauskommen können
Geschrieben von: Herr von Böde Sep 29 2015, 21:25
Das stimmt natürlich aber das in 2 Casings (aus Sporenspitzen) ein Strain der in der Regel mehr als doppelt so große FKs hervorbringt solche Miniwichtel zu sporulieren anfangen halte ich für mehr als unwahrscheinlich, zumal "nebenan" gleich die A+ stehen die sich völlig normal entwickeln.
Also an Bedingungen in der Fruchtungskammer wirds nicht liegen, wenn dann an Bedingungen direkt in den Casings.
Immerhin sollten auch Pf.orig. Fks nicht so winzig bleiben, aber da die Sporen aus professioneller Quelle stammen denke ich mal das die seit Generationen kein Casing mehr durchwachsen haben.
Ich glaube jedenfalls kaum das das Golden Teacher sind, selbst auf PF-Cakes hatten die weit größere Fruchtkörper.
So wichtig ists aber nicht, aus diesen Casings gibt es kein weiterkultiviertes Myzel, das für mehr Irrtümer sorgen könnte und in spätestens 10 Tagen- schätze ich jetzt mal- hab ich den Vergleich. ![]()
Edit:
da fällt mir noch ein: ein sporulierender GT-Hut sollte wenigstens Ansatzweise die typische helle Farbe bekommen, das ist hier überhaupt nicht der Fall..
Edit II:
Aber vielleicht traut sich ja jemand eine Bestimmung anhand von Fotos der Casings zu:

Beim ersten Bild erkennt man ganz oben und rechts 2 Fruchtkörper die mit dem Hut nach unten und dem Stiel nach oben wachsen, das könnte evtl. auf nen Konti hindeuten? Oder ein typisches Merkmal einer der beiden fraglichen Strains?
Geschrieben von: Mister.T Sep 29 2015, 21:38
hmm sehen ein wenig nach Penis Envy aus ![]()
Ob es sich um eine Konti handelt weiß ich leider nicht ![]()
Geschrieben von: Herr von Böde Sep 29 2015, 21:54
![]()
Lol, ja. Nur die haben ihren Hut gewöhnlich auch oben und sollten ebenfalls deutlich größer werden- wobei die Kopfsteher wohl noch 2-3 Tage brauchen.
Ich selbst glaub nicht an einen Konti ehr das es etwas mit dem Strain zu tun hat, evtl. auch mit der Feuchtigkeit - meine sowas schonmal auf Fotos gesehen zu haben.
Geschrieben von: Herr von Böde Sep 30 2015, 09:02
Die 3 Gt-1 Gläser sind in der weiter oben schonmal abgebildeten 2,5l Eisdose gecased.
Als Boden wurden 2 430ml Gläser sterilisiertes Perlit eingebracht, auch die Deckschicht ist bestimmt nicht zu dünn, war da recht großzügig. Der Vermiculiteanteil in der Deckschicht wurde auf ca. 75vol % erhöt die restlichen 25% bestehn wie gehabt aus Cocoohum.
Auf das Beimpfen der 8 neuen Gläser habe ich erstmal verzichtet, denn das Myzel in allen andren Gläsern vom 17. und 19.09 wuchs nicht wirklich weiter, deutlich war in mindestens der Hälfte der Gläser grüner Schimmel bzw. gräuliches - nicht Psilomyzel zu erkennen .
Alle anderen Gläser wurden also entsorgt, die 8 neuen Gläser werde ich erstmal bei 35 Grad Inkubieren um auszuschliessen dass das Sterilisieren fehlgeschlagen ist (jedoch waren diese Gläser-630 ml- gefüllt mit jeweils genau 400 ml Substrat zu dritt bzw. zu zweit jeweils 150 min im DDKT auf Temperatur und unter Druck).
Am Wochenende nehme ich mal eine Geruchsprobe, werde dann erneut Sterilisieren und erst dann mit Agar beimpfen.
Ich habe die leise Vermutung dass das Sittichfutter stark mit Sporen belastet ist, werd testweise mal ein paar Petries mit unsterilisierten Körnen "beimpfen" um zu sehen ob da ähnlicher Schimmel wächst (wie gesagt gräuliches Myzel, das irgendwann ins Blasgüne umschlägt). Ggf. werd ich dann wohl auf reine Hirse bzw. Hirsemischung als Zusatz ausweichen.
Geschrieben von: hogie Sep 30 2015, 15:13
Irgendwo muss bei dir noch eine gewaltige Schwachstelle lauern. Bei 120° im Sattdampf muss die Dauer auch bei hoch kontaminiertem Substrat locker ausreichen. Vielleicht erreicht dein DDKT keine genügend hohe Temperatur. Bei z.B. 110° erwischst du Sporenbildner praktisch nie.
Geschrieben von: Herr von Böde Sep 30 2015, 16:19
Ok, die jetzt entsorgten Gläser waren - wenn ich mich recht erinnere auch nur 90 max. 120 min im Topf - bin mit der Zeit hochgegangen weil mit den größeren Gläsern natürlich auch mehr Substrat im Topf war.
Aber klar, darum jetzt das warme Bebrühten der unbeimpften Gläser.
Werd mir gleich ausserdem mal ein paar Gemüse oder wohl besser Hülsenfrüchte googeln und mir die Garzeiten anschauen.
Wenn der Topf bei 3 von 3 Gemüsen das Garen in angegebener Zeit schafft, kann ich wohl davon ausgehen das er die 120 Grad C schafft.
Evtl. gibts dann mal jahreszeitlich verfrüht Linsen und Erbseneintöpfe die nächsten 2 Wochen^^ immerhin nicht aus der Dose !! ![]()
Edtit:
Es besteht aber auch die Möglichkeit dass das Polyfil die Schimmelquelle ist:
ich hatte die Stopfen nämlich großzügig mit Silikon auf beiden Seiten (innen und aussen) zum Rand hin abgedichtet. Nach dem 2ten Sterilisieren setzte der Deckel dann schon Rost an wie ich nach dem Abnehmen der Alufolie feststellen musste.
Ausserdem ist es sicher besser den Polyfil nicht 2x zu Verwenden und besser nicht einzukleben. Hatte die Filter zwar mit Heisswasser und Chlorix ausgibig gespühlt aber organische Reste könnten natürlich trotzdem verblieben sein, so das Schimmel durchwachsen konnte, ich sehe allerdinks in keinem Filter ein Spur Schimmel...
Geschrieben von: hogie Sep 30 2015, 16:46
Ich glaube nicht, dass dich die Hülsefrüchte weiter bringen. Entweder hinreichend genau messen oder einen Sporentest machen.
https://glp-shop.de/sporentest-streifen.html
Geschrieben von: Herr von Böde Sep 30 2015, 17:03
![]()
Die Dinger hatte ich letzte Woche schon im GLP Warenkorb, hab sie dann aber wider entfernt weil ich die Notwendigkeit da noch nicht wirlich sah und festgestellt hatte das die Untersuchung nicht im Preis inbegriffen ist - wobei, kann man die nicht selbst einfach in eine Petrie packen bzw. Agar damit beimpfen?
(Für Reptilien gibts ähnlich Sets um vorzugsweise vor Überwinterungen oder Verpaarungen Kotproben zu nehmen, da ist die Untersuchung im Preis enthalten).
Da ich esrt Donnerstag eine Sendung in Auftrag gegeben habe und grade erwarte werd ich es erst nochmal so versuchen, ggf. sammel ich mal selbst eine bunte Schimmelsporenmischung zusammen, sterilesiere sie im Topf in einer Petrie und setze dann mal auf Agar an.
Sonst bei der nächsten Bestellung^^
Geschrieben von: hogie Sep 30 2015, 17:23
Eigentlich muss das Zeug nur in den Brutschrank. Am einfachsten dürften solche Ampullen zu verwenden sein:
https://www.uni-marburg.de/sicherheit/autoklavencheck.pdf
Geschrieben von: Herr von Böde Sep 30 2015, 17:39
Ah, danke ! Die werd ich mal testen. Allerdings schafft keiner meiner Inkubatoren 60 Grad C, ich glaub 42 Grad könnte ich in einem Eigenbau Gerät erreichen.
Aber wenn bei 35 Grad nach 10 Tagen eine Verfärbung stattfindet ist das Ergebniss wohl ebenso eindeutig.
Edit 21:05 Uhr:
Hab jetzt mal ne schöne Schimmelagarplatte gebastelt ^^
Hab mich dazu extra in fremde Räumlichkeiten begeben um hier nicht unnötig die Sporenbelastung in der Raumluft zu erhöhen oder gar noch versteckte Schimmelansiedlungen zu ermöglichen:
Habe aus 2 kontaminierten Gläsern diese "schönen" bestimmt schon sporulierenden Kontistellen entnömmen:

(kann jemand evtl. sagen um welchen Schimmel es sich handelt und wo der typischerweise gerne siedelt - mal abgesehen von meinen Substratgläsern ^^??)
und auf Agar in einer Petrie gepackt (und sehr gut verschlossen):
Das Ganze lasse ich jetzt fern irgentwelcher Inkubatoren oder Pilzkulturen stehen bis ich mir sicher bin das ordentlich Sporen freigesetzt werden.
Dann wird die Petrie zusammen mit wassergefüllten Gläsern auf ein solches gestellt (dorthin wo wohl im Betrieb die tiefsten Temperaturen herrschen) und für 15 min sterilisiert.
Anschliessend wird etws flüssiges Agar entnommen und auf eine frische Petrie übertragen.
Wenn da was wächst brauche ich einen neuen DDKT...
Ich glaub da bin ich nah dran:
http://www.google.de/imgres?imgurl=http%3A%2F%2Fshow.wnmu.edu%2Fmicrofungi%2Fgallery%2FAnamorphic%2FAspergillus%2FAspergillus-flavus-1059--1xdiss.jpg&imgrefurl=http%3A%2F%2Fshow.wnmu.edu%2Fmicrofungi%2FshowGallery.php%3Fdiv%3DAnamorphic%26gen%3DAspergillus%26spec%3Dflavus%26id%3D1059%26colonies%3D1&h=267&w=263&tbnid=QjEpuZ43mFls5M%3A&docid=5QbY9MiZaKycxM&ei=4UAMVpnMKYTJsQGo3bjoBQ&tbm=isch&iact=rc&uact=3&dur=2631&page=16&start=213&ndsp=15&ved=0CFIQrQMwGjjIAWoVChMI2cCOyMefyAIVhGQsCh2oLg5d
Geschrieben von: Herr von Böde Oct 1 2015, 03:16
huch
Ok, kann hoffentlich genausogut wohl Aspergillus fumigatus oder ganz etwas anderes sein...
Den riskantesten Teil der gesamten Aktion habe ich aber eh wohl hinter mir, werd das Experiment also zuende bringen...
Da dieses Zeit braucht hab ich mich entschlossen die vorbereiteten Gläser nun doch zu beimpfen (ich hoffe ich komme im Laufe des Tages dazu). Schlimmstenfalls gehen ein paar Körner verloren.
4 Gläser nochmals mit dem GT-1 Myzel, 4 Gläser mit AA+-1 Myzel.
Ich möchte das erst genannte Myzel, welches ich für sicher isoliert halte nur ungern wegen Überalterung durch das ausschliessliche Wachstum auf KDA verlieren (auch wenn ich noch keine Früchte diese Myzels zu Gesicht bekommen habe- höchstens unwissentlich auf einem der 3 Pf-Cakes aus denen es ja stammt).
Aus dem selben Grund werde ich das Agar jetzt mal wechseln, grade wird Bieragar sterilisiert:
Hab dazu 0,5l Pils (billig vom Aldi) mit 0,5l Wasser vermischt und das ganze wieder auf 0,5 l einkochen lassen (Zwecks Alk.-reduzierung), dazu kamen dann noch 2g Dextrose und 0,05g Kaliumhydrogenphosphat sowie 12g Agar Agar.
Bin sehr gespannt wie den Myzelien diese Abwechslung gefällt (und mindestens genauso ob mir ein ähnlich kontiarmes Beimpfen - jedenfalls der Petries- wieder gelingt)
Beim GT-1 Myzel und eigendlich auch beim AA+1 wird jedenfalls offensichtlich das sie Abwechslung brauchen, einfach wegen des im Vergleich rasanten Wachstums im Körnersubstrat.
Hier mal Bilder von den Petries, man bedenke das ein jeweils etwas kleiners Impfstück (als in den Petries jetzt bewachsenes Agar vorhanden ist) in derselben Zeit ein 430 ml Glas durwachsen hat...jedenfalls das GT-1 Myzel.

Auch bei den kaum selektierten Pf org. Myzelien die 4-6 Wochen später auf Agar gebracht wurden macht sich dieser KDA-Überdruss wohl schon bemerkbar:

Der 2te Flush des Heimchendosencasings könnte schon gepflückt werden.
Um ein paar Prints zu bekommen lass ich aber die Hüte sich noch ein wenig entfalten, hoffe ich verpasse nicht den richtigen Zeitpunkt, kann nur alle 5- 6h mal nachschauen


Geschrieben von: hogie Oct 1 2015, 13:25
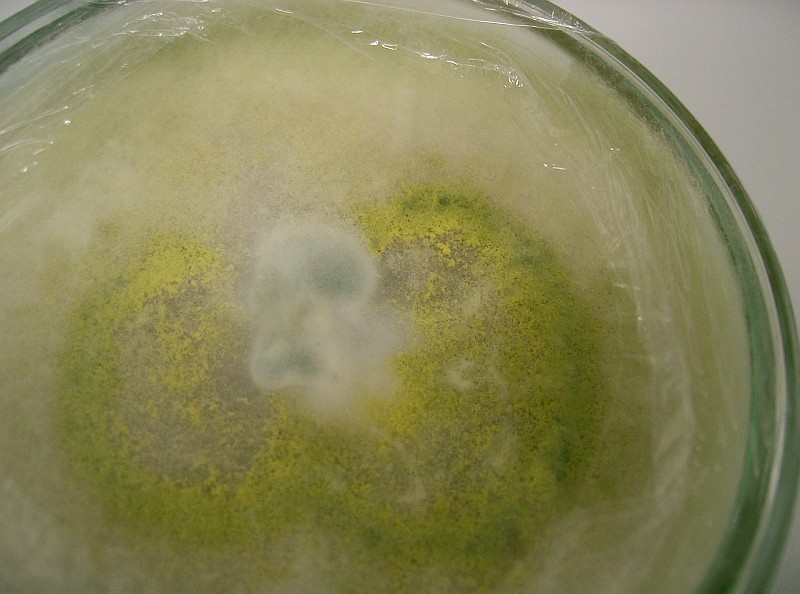
Das war mein Aspergillus flavus. ![]()
Geschrieben von: Herr von Böde Oct 1 2015, 16:54
Hm, also farblich könnte sich das tatsächlich schon ziemlich in die Richtung entwickeln...
Hatte gutes Timing, es wurden grade zwei weitgehend geöffnete A+ erwischt, ein paar Velumreste wurde noch vorsichtig entfernt.
Ein Bild der verbliebenen Stiele (als Massstab ein Q-Tip), die haben sich im Laufe des Tages nochmal gewaltig gestreckt, sind aber auch nicht sonderlich massiv, ich schätze mal ein 5-7 x kleinerer FK bzw. Stiel eines kleinen der PF.orig. Wichtel bringt das selbe auf die Waage :
Edit:
wobei, diese beiden Stile doch über 15 g Masse haben...
Edit II :
Das Casing brachte im 2ten Flush soziemlich das gleiche Ergebniss: 72 g (bin mir grad nicht sicher obs beim ersten 73 oder 76 waren, glaube aber 73g).
Das überrascht mich doch, dachte bei der dünnen Roggenschicht gehen die Erträge von Flush zu Flush deutlich um mindestens 1/3 zurück.
Da die "Schrumpfränder" nochmal deutlich größer wurden bis zu 1cm. hab ich direkt nach der Ernte trockenes Vermiculite hineingestreut und dann eingespühlt. Das ganze wird jetzt wohl bis morgen Mittag gedunkt.
An der Stelle mal eine Frage die mir schon länger immer wider in den Sinn kommt aber dann schnell auch vergessen ist:
Die PF-Cakes hatte ich wärend des Dunkens in den Kühlschrank gestellt, bei den Casings hab ich das bisher nicht so gemacht, aber sie stehen /standen in einem unbeheizten (Überwinterungs-)raum, da schwanken die Temperaturen derzeit zwischen 8 (gestern Nacht wurde es erstmalig so kühl) und 15 Grad.
Macht das Kühlen irgendeinen Sinn, oder verlangsamt das nur sinnlos alles?
Es wird ja manchmal empfohlen vor der erten Fruchtung nen Kälteschock zu geben, das habe ich auch bisher nur bei den Cakes so gemacht. Die Cakes bzw. Casings auch beim Dunken etwas bzw. sehr viel kühler zu stellen war nur so eine Idee, die sich gut anfühlte.
Evtl. gewinne ich aber nen ganzen Tag wenn ich das völlig unterlasse, bzw. nur aus der Fruchtungsbox
(schwankt zwischen 22 und 25 Grad) entnehme und bei normaler Raumtemperatur (schwankt wohl auch zwischen 17 und 22 Grad) das Dunken abwarte.
Was meint Ihr ?
Geschrieben von: Herr von Böde Oct 2 2015, 01:49
Ich musste grade im Inkubator handieren weil ich mit dem Beimpfen der Gläser begonnen habe.
Ohne wirklich zu glauben etwas zu sehen konnte ich es mir nicht verkneiffen in das "Rieseneisdosencasing" mit dem GT-1 Myzel zu lauern.
![]()
Unglaublich, Schock schwere Not - ein Konti?? -NEIN, eindeutig nicht: in nichtmal 48h hat das Myzel das (diesmal deutlich fester angedrückte) mindestens 2 ehr 2,5 cm dicke Casing an einer Stelle bewältigt :

Wenn das so weitergeht und an der Stelle nicht nur einfach ein Körnchen nach oben gerutscht war, gehts Samstag Abend evtl. sogar noch früher in die (dann schnell neu eingerichtete) Fruchtungsbox ![]()
Hier nochmal ein Bild der beiden, für mich jetzt sicher als PF-orig. identifizierten, Quarkdosen:
dabei liegt die gestrige Ernte des linken Casings an dem Rechten habe ich mich erst nach dem Foto vergriffen, insgesamt 8,5g.
Ich frage mich wie man aus diesen Hüten Sporen gewinnen kann, wird sicher nur ein Abdruck mit dünnem Rand.
Meine schon erwähnte Vermutung das einzelne Flushes in einander übergehen scheint zuzutreffen, kann täglich etwa die gleiche Menge ernten wärend es kontinurlich nachspriesst.
Evtl. werd ich bei einem größeren Exemplar nochmal versuchen zu klonen, davon isolierte Genetik fruchten zu sehen fände ich schon interessant.
Weiterhin bleibt die Größe der Wichtel ein interessantes Phänomen, ob das wirklich am Substrat liegt? ob professionell erzeugte PF.orig. Sporen tatsächlich ausschliesslich aus FKs auf PF-Cakes gewonnen werden?
Edit 22:18 Uhr:
Heute vielen bei den Pfs 13 g an... (übrigens vom Volumen etwa 1/2 des auf dem Bild weiter oben-mit dem Q-Tip- größeren A+ Stiels, beide zusammen wogen nicht ganz 16g) Kleinvieh macht auch Mist ![]()
Ein Hütchen ist einzeln zum Sporenwerfen auf Alu unter einem Glas, 3 weitere zusammen unter einem Glas.
Beim großen Casing doch nur ein einzeles Korn? Hatte heute Mittag jedenfalls keinen weitern Fortschritt festgestell.
Geschrieben von: Herr von Böde Oct 3 2015, 23:33
Auf 15 neuen Petris (10x GT-1, 5x A+-I) aus der Nacht vom 01.10 auf den 02.10
(zusammen mit bei der Beimpfung der 8 Gläser entstanden) sind bisher keine Kontis zu erkennen, das sich noch Hefen breit machen ist damit schon fast ausgeschlossen.
Wie gut das Bieragar angenommen wird ist noch nicht raus, die meisten Impfstücke sind grade mal angewachsen.
Ich habe bei meiner Glovebox bei dieser Impfaktion die Gloves entfernt, so das ich mit 1x Handschuhen durch die als Stutzen dienenden Konservendosen (die Handschulöcher) arbeiten konnte.
Das hat enorm die Geschwindikeit steigern können, sowohl bei den einzelen Beimpfungen als auch insgesamt: Die Löcher können gut als Schleuse für Petris, ausgeglühte Scalpelle etc. dienen.
Wärend der Einwikzeit des Desinfekts wurden die Löcher einfach mit Frischhaltefolie verschlossen.
Vorteil ist nicht nur die erhöte Arbeitsgeschwindikeit, auch das wirklich extrem frustrierende Einführen der Hände in die engen Putzhanschuhe (alles rutscht dauernd hin un her, gestapelte Petris fallen um, wahrscheinlich wir dabei auch Luft angesaugt) fällt komplett weg- beim ausziehen der Handschuhe gibt es die selben Probleme natürlich nochmal^^
Das "Rieseneisdosencasing" zeigt jetzt an 3-4 Stellen Myzelwachstum an der Oberfläche, bin gespannt wie es morgen Abend aussieht, dann ,lohnt evtl. auch ein Foto.
Das nächte A+ Casing wird morgen mit dem 2ten Flush fertig. Leider kann ich die Dosen nicht mehr zuordnen, sie hatten anfangs einen, zwei, bzw. drei rote Filzstiftpunkte, nach dem ersten Flush, bzw. dem Dunken hatte ich die Dosen mit Ethanol 70-80%ig aussen abgewischt, damit verschwanden auch die Markierungspunkte, hab das erst einige Tage später bemerkt.
Edit 05:30 Uhr:
Hier nochmal 2 Klonversuche aus einem dickeren PF-o. Stiel.
Immerhin ist an allen 3 Impfstücken frisches Myzelwachstum zu erkennen, trotzdem kann die erste Petrie komplett entsorgt werden, auch am weiter unten liegenden Impfstück meine ich verdächtiges Wachstum ausmachen zu können, das am Oberen Stück ein Konti wächst ist sehr deutlich:
In der zweiten Petrie mit nur einem Impfstück könnte die Klonung tatsächlich gelingen, eindeutig frisches Myzel und von Kontis noch keine Spur:
Edit 21:15 Uhr:
An den gegenüberliegenden Rändern ist das Myzel inzwisch an mehreren Stellen sehr gut zu sehen aber auch mitten drauf gibts (für die Kamera leider noch nicht festzuhalten) ein paar Stellen mit durchbrechendem Myzel, das 2500ml "Rieseneisdosencasing" mit Gt-1 Myzel:
Das beits abgeerntete A+ Quardosencasing brachte nur 30 g im zweiten Flush, das nächste wohl noch weniger. Das Casing mit den vielen Pilzen sieht dagegen wieder so aus wie im ersten Flush - auch wenn ich die Dosen nicht mehr 100%ig zuordnen kann- ich vermute das die Casings die schon im ersen Flush weniger Ertrag brachten im zweiten Flush deutlicher an Ertrag verlieren und die onehin ertragreicheren Casings sich von der Erntemenge im 2ten Flush nicht groß unterscheiden (sind ja aus Sporenspitze).
Wie man sieht habe ich ein Pf-o. casing weitgehend abgepflückt, einfach um zu sehen was passiert ![]()
Geschrieben von: Herr von Böde Oct 5 2015, 19:08
Jetzt geht es schnell :
Die beiden lezten A+ Casings brachten 39,5 und 78 g. Beim 78g Casing also auf jedenfall mehr als im ersten Flush.
Man muss natürlich bedenken dass das Erntegewicht stark vom Erntezeitpunkt abhängt, wenn ich es nicht auf Prints abgesehen habe pflücke ich solbald der erste Riss im Velum erscheint, das wäre bei den beiden Casings wohl irgendwann in der Nacht der Fall gewesen.
Diesmal wurde erst heute Mittag gepflückt und die Hüte hatten sich schon weitgehend geöffnet, wenn auch nicht voll entfaltet.
Darüber dass das erreichte Mehrgewicht nicht unbedingt auf wirkstoffhaltiges Myzel sonder großteils auf aufgesogenes Wasser zurückgeht ist man sich in der Pilzgemeinde ja relativ einig...
Geschrieben von: Herr von Böde Oct 6 2015, 06:04
Es geht jetzt wirklich schnell, überall Myzel.
Morgen früh kann sicher umgezogen werden ![]()

Das Bieragar wird super angenommen, in der Mitte zum Vergleich eine Petrie vom 17.09 (hatte die lieber mal noch behalten ![]() )rechts und links sowie unten links das selbe Myzel vom 02.10 (wird das vom 17.09 sicher morgen oder übermogen überholen).
)rechts und links sowie unten links das selbe Myzel vom 02.10 (wird das vom 17.09 sicher morgen oder übermogen überholen).
Unten in der Mitte die GT-1 Petrie aus der die Impfstücke entnommen wurden (um mal zu sehen wie es mit Kontis nach dem mehrmaligen Öffnen und Zerschnippeln in der Box aussieht - noch siehts gut aus ![]() )
)
Rechts oben eine Petrie mit zwei Impfstücken (beides GT-1) , will einfach sehen wie die beim "Zusammenprall" reagieren.
Das gleiche Experiment gibts bei der nächsten Impfaktion mal mit 2 sicher unterschiedlichen Myzelien, zB. A+ & GT , einfach um zu sehen was passiert ![]()
Das A+ Myzel mag das Bieragar offenbar noch lieber: Oben in der Mitte ein Impfstück das mit der bewachsenen Seite aufs Agar gefallen war, wollte nicht rumfummeln und hoffte einfach dass das Myzel nicht erstickt, belies es also so - das unten liegende Myzel hat sich offensichtlich so aufgebläht das die unbewachsene Seite jetzt an den Deckel der Petrie gedrückt wird, Myzel versucht den wohl weitgehend nährstoffreien Deckel zu besiedeln ![]()
Oben links und unten rechts nochmal A+ :
Das an die Decke gegangene A+ Myzel nochmal nahe :

Edit
Beim Auffüllen mit Vermiculite eines frisch gedunkten A+ Casings fällt mir ein, die gewaltigen Spalten nach dem 2ten Flush könnte man auch mal zeigen, wirklich ansehnlich ist keines der A+ Casings mehr:
Das geht wirklich bis unten durch, schwer zu fotografieren...
Edit 22:49 Uhr:
Da ich annehme hier das zu erkennen was man als "Neigung zum Overlay" bezeichnen könnte und ich glaube mich entsinnen zu können bei Waaagh die Empfehlung gelesen zu haben in einem solchen Fall mit dem Umstellen auf Fruchtungsbedingungen nicht zu warten bis die Deckschicht komplett bewachsen ist, steht das 2500 ml Casing seit einigen Minuten in der Fruchtungsbox.
Um Kontis mache ich mir keine großen Sorgen.
Sogar passt die Eisdose in die noch einzige Fruchtungsbox, auch wenn das A+ Heimchendosencasing grade versuchsweise nochmal in die Inkumbation gewandert ist ( hatte wohl etwas viel Vermiculite aufgetragen und das Myzel hat begonnen dieses wieder zu überwachsen- dachte da sind Inkubationbedingungen für 24-48 h evtl. nochmal sinnvoll).

Geschrieben von: Herr von Böde Oct 7 2015, 05:20
So, hab mich entschlossen den Tag mit nem ausgewachsenen Piztrip zu starten ![]()
Hab um 05:02 Uhr 6,3g knusprig trockene - dann aber gründlich und nicht völlig ohne Genuß durchgekaute - A+ verschluckt.
Die nächsten Wochen bin ich beruflich etwas unvorhersehbar eingespannt (auf Abruf), so das heute evtl. die letzte Gelegenheit bis Mitte November für mich ist die Früchte meiner Bemühungen auch zu geniessen.
Ich gestalte den Trip bzw. das Hochfahren diesmal so wie ich es eigentlich sonst auch immer gemacht habe, etwas Bier ist am Start (4 Halbe) die eh nicht getrunken werden und mich als jemanden der Alkohol sonst tatsächlich nur mal auf dem Weihnachtsmarkt zu sich nimmt auch völlig betrunken machen würden.
Bei einem Trip habe ich meisten 4 Bier da, von denen 2 recht zügig getrunken werden (innerhalb der ersten 45 min - ![]() - ich weiss andere hätten in der Zeit schon alle 4 weg), normal schlägt dann der Trip auch gut ein so das der rest schlicht vergessen oder nur noch angenippt wird.
- ich weiss andere hätten in der Zeit schon alle 4 weg), normal schlägt dann der Trip auch gut ein so das der rest schlicht vergessen oder nur noch angenippt wird.
Mein Magen ist seit gestern Mittag leer.
Die Wohnung ist gesichert (scharfe Kanten etc.).
Mir ist grad nach Doku, so läuft https://www.youtube.com/watch?v=_03a3OpKt5k nebenher.
Mal schauen wies wird, die Dosierung dürfte diesmal passen.
05:29 Uhr
Es ist nicht so das ich tatsächlich schon etwas merke aber ich kann mich grad nicht von diesem Beitrag lösen... hab jetzt wohl 20x gelesen was ich grad geschrieben habe. Also Wirkung ist unterschwellig auf jedenfall schon da...
Und ich weiss das da gleich ne gewaltige Welle einschlägt ![]()
05:39 Uhr
deutliche Veränderungen der Sinne (wie viele Damen sprechen da aus dem Off bei der Doku ![]() ??, laiern die ?? ) alles völlig anders..
??, laiern die ?? ) alles völlig anders..
Denke sinnvolles jetzt hier zusammenzubekommen wird schwer.
Gedanken springen...die Well ist da ...
bis später ![]()
die Hände schwitzen, oder zerfliessen ??
06:06 Uhr:
also die Stäke passt soweit, Dosierung ok.
Aber schon allein weil es Momente gibt in denen ich solche Pläne überhaubt schmieden kann... werds im Novemmber wohl auch mal mit 8 g und mehr.
Puhh, es ist schon schwer eine n Gedankengang zuende, geschweige denn auch aufzuschreiben...dazu kommt noch die Zeilen verschieben sich gegeneinander..
ohhh..das wird gebrabbel...
06:27 Uhr:
mein Magen dreht sich grad um... aber nicht wegen den pilzen sonder wegen dem pils ![]() ka warum aber ich hab grad offenbar innerhalb von rd 10min die 3te fl getrunken...aus versehen irgendwie
ka warum aber ich hab grad offenbar innerhalb von rd 10min die 3te fl getrunken...aus versehen irgendwie ![]() , evtl hatte ich durst...
, evtl hatte ich durst...
boahh...gebrabbel, wollte auf irgedertwas hinaus..dachte ich..
so..nächste meldung erst wieder wenns tatsächlich auch wieder geht
![]()
06:43 Uhr:
kanns mir nicht verkneiffen ![]()
für die anmerkung reichts auch noch:
bin von den dokus, derem inhalt ich eh nichtmehr folgen kann umgestiegen, und dabei bleibts dann wohl vorerst auch mal ![]()
https://www.youtube.com/watch?v=4va9DduFwIQ
07:06 Uhr:
wo sind die Zeiten hin ??
https://www.youtube.com/watch?v=w8aSwUWev8Q
https://www.youtube.com/watch?v=c8-kj1GkbfU ![]()
07:18 Uhr
Scence change ![]()
https://www.youtube.com/watch?v=evssZWsdsqc
zwischendurch, beim Betrachten meines zwischenzeitlich sehr erstaunt dreinblickenden ![]() schäferhundes, sich ankündigende, nur mühsam abzuwürgende Lachfläschs
schäferhundes, sich ankündigende, nur mühsam abzuwürgende Lachfläschs ![]()
wirklich ein total unerwateter tripverlauf...das ganze geschreibsel hier...die längst vergessenen patys irgendwo... der erwartungsvoll dreinbilckende "zwerckschäfie" auf der couch...
![]()
07:40 Uhr :
es fällt auf:
I die ersten (unangenehmen) gedanken an das herunterkommen setzen ein.
(ein bier wäre auch nicht schlecht... ![]() )
)
II ich rauche seit mindestens 90 min kette (in der tat ,eine nach der anderen)... so auch noch nicht erlebt.
07:50 Uhr :
rückfall in partyzeiten, noch irgendetwas nachzuholen ??
tatsächlich zuwenig sex ![]() ??
??
ganz instiktiv auch musiktechnisch irgendwie wieder auf die anfänge zurückgekommen:
https://www.youtube.com/watch?v=R795KiMD4zs
(kommt grad auch richtig gut !!!)
klar, der trip flacht ab.
(zunehmend erfolgreiche)Bemühungen um struktur in den gedankengängen...
08:13 Uhr:
zum runterkommen erscheint dies wirklich nett ![]()
https://www.youtube.com/watch?v=-e7x8BhiAQ4
ansonsten in den letzten minuten nur viele sehr private Gedanken, was will/kann der Trip mir sagen ??
evtl. noch ein resume wenn ich tatsächlich wider vollends auf erden angekommen bin.
lehne mich jetzt zurück und grüble noch etwas bei der tollen musik.
Geschrieben von: Herr von Böde Oct 7 2015, 08:52
08:45 Uhr:
bei einem zwingent notwendig gewordenen Gang durch die halbe Wohnung schlug mir grad ein typisches Erleben im Peak eines Trips ins bewusstsein:
von einem paar schuhen (sorgfältig Vor ![]() dem Schuschrank abgestellt) kann man sich tatsächlich erheblich in seiner bewegungsfreiheit eingeschränkt fühlen, man hängt daran fest, die nächste ecke im raum klebt an einem wie eine klebefliegenfalle
dem Schuschrank abgestellt) kann man sich tatsächlich erheblich in seiner bewegungsfreiheit eingeschränkt fühlen, man hängt daran fest, die nächste ecke im raum klebt an einem wie eine klebefliegenfalle ![]()
will sagen, sowas kann schon angst machen wenn man es nicht kennt und irgendwie auch mag ![]() , soein bizzarres erleben ist komplett unvereinbar mit dem "otto-normal-wachbewusstsein". es kommen dabei räumliche und zeitliche verzerrungen plötzlich flashartig ins bewusstsein.
, soein bizzarres erleben ist komplett unvereinbar mit dem "otto-normal-wachbewusstsein". es kommen dabei räumliche und zeitliche verzerrungen plötzlich flashartig ins bewusstsein.
als hätte die verwirrung keine ausreichende größe (keine ahnung gard, wo ich welche löschen soll) :
also eine antwort auf die antwort...
![]()
Geschrieben von: Herr von Böde Oct 7 2015, 09:17
bei einem zwingent notwendig gewordenen Gang durch die halbe Wohnung schlug mir grad ein typisches Erleben im Peak eines Trips ins bewusstsein:
von einem paar schuhen (sorgfältig Vor
will sagen, sowas kann schon angst machen wenn man es nicht kennt und irgendwie auch mag
kann mich auch gut daran erinnern das ich als junger twen schon dosen intus hatte auf denen solches erleben gar nicht mehr so "flashartig" war sondern im prinzip den gesamten peak ausgemacht hat.
würde da auch gern wieder hin, darum die weiter oben schon ewähnten gedanken die dosis gen 8g+ zu erhöhen.
09:47 Uhr:
nun sind bald 5h seit dem verzehr vergangen.
ich bin immer noch alles andere als nüchtern (abgesehen von meinem magen, der deutlich nach einer aufgabe verlangt - immerhin bald 24 h keine feste mahlzeit mehr, die wichtel fallen in der beziehung wohl kaum ins gewicht), bei der hunderunde war das deutlich zu spüren, selbst die schäbigste ecke : ein prachtvolles panorama
aber sehr praktische - alltagsgedanken nehmen wieder den gewohnten raum ein.
essen gehen ? gerne aber ich glaub heute nicht die beste idee
essen bestellen ? 2h wartezeit bis zum frühest möglichen lieferzeitpunkt...(ey, bin ich hier aufn dorf oder was??)
essen kochen ? geht grad mit an sicherheit grenzender wahrscheinlichkeit gründlich in die hose... schon nudeln kochen könnte etwas zu anspruchsvoll sein (wegen der vergessenen nudeln auf dem herd
guter rat ist teuer.
hab mich wohl grad für das bestellen entschieden, macht mein magen die 24h halt voll.
aber auch gedanken an die weitere gestaltung des tages nehmen platz ein.
den eltern absagen? den raum für mich beanspruchen, mich satt essen und wahrscheinlich- schlicht schlafen?
kompromiss möglich ??
blablub...
fühlbar ist der rausch noch an einer gewissen gedanklichen zerstereutheit, einem leichtem gefühl des getrieben seins (komme ja dauernd auf diesen tripbericht zurück - der nächste trip ganz sicher fern des forums) was etwas nervt und einem ruhebedürfniss, gähnen und mühdikeit blitzen immer häufiger durch.
sehr ausgeprägt auch noch optische verzerrungen und sensationen beim blick aus dem fenster (triester bauplatz).
ich denke das war es hier jetzt wirklich. melde mich ab.
geniesse ne pekingente (glutamatfrei
Geschrieben von: hogie Oct 7 2015, 10:29
Haha, Glutamatfreie Pekingente gibt es nicht 😂
Geschrieben von: Acinonyx Oct 7 2015, 10:34
Koch was, das Dich so in den Bann zieht, dass Du den Herd nicht verlässt
Ich hab mal am Ende eines gewaltigen Trichterwinde-Trips eine Tomatensuppe gekocht und war so fasziniert von diesen roten sprudelnden Massen in dem Topf vor mir - unvorstellbar, dass so riesige Fluten in meinen Magen passen sollten
Geschrieben von: Herr von Böde Oct 7 2015, 11:40
Hm,es gibt hier nen Chinesen da kann man Glutamat abwählen, ob die sich daran halten ist die Frage, müsste man 2 Enten zum Vergleich ordern...
Aber der Chinese dauert mir eh zu lang, hab inzwischen echtes Magenknurren...
Thunfischpizza gibts mit Knofi und Oliven und als Zwischenhappen zur "Geschmacksneutralisierung" ne schlichte Salamipizza (mini) mit Paprika...
Ausserdem nen Liter Orangenlimo...
Freu mich drauf, wirklich ^^
Ansonsten denke ich bin ich sanft gelandet, die optischen Verzerrungen sind so gut wie weg, der Anblick der Baustelle nebenan bleibt aber noch super geil
Nach dem Essen wird tatsächlich nicht mehr viel spührbar sein.
Geschrieben von: hogie Oct 7 2015, 12:02
Die Angst vor Glutamat ist unbegründet. Wenn jemand keine nachgewiesene Unverträglichkeit hat, kann man damit Speisen wesentlich schmackhafter bekommen. Man sollte aber Konzentration und pH-Wert im Auge behalten, um es sinnvoll und effizient einzusetzen. Die Chinamänner machen das jedenfalls nicht.
Geschrieben von: hillage Oct 7 2015, 22:17
war das der trip, wo du es bereut hast dir die zähne geputzt zu haben?
Geschrieben von: Acinonyx Oct 8 2015, 10:02
war das der trip, wo du es bereut hast dir die zähne geputzt zu haben?
Haha, ja, daran erinnerst Du Dich? Stimmt, so schrecklich hat Zahnpasta noch nie geschmeckt....
Pizza könnte ich übrigens nach einem Trip auch nie essen - bzw. hab das nach meinem allerersten LSD-Trip sogar versucht und hab kaum was davon runter gebracht, weil es wie Karton ausgesehen und geschmeckt hat
Mit LSD vertragen sich bei mir eigentlich nur Orangen, und die scheinen dafür DAS Lebenselixier schlechthin zu enthalten - einfach nur göttlich
Bei Pilzen bekomme ich oft Lust auf Bananen, Datteln und schwarze Schokolade. Naturjoghurt und Trauben gehen auch noch.
Geschrieben von: Herr von Böde Oct 8 2015, 10:22
Pizza könnte ich übrigens nach einem Trip auch nie essen - bzw. hab das nach meinem allerersten LSD-Trip sogar versucht und hab kaum was davon runter gebracht, weil es wie Karton ausgesehen und geschmeckt hat
Mit LSD vertragen sich bei mir eigentlich nur Orangen, und die scheinen dafür DAS Lebenselixier schlechthin zu enthalten - einfach nur göttlich
Bei Pilzen bekomme ich oft Lust auf Bananen, Datteln und schwarze Schokolade. Naturjoghurt und Trauben gehen auch noch.
Joa, so groß der Hunger anfänglich war, es ging nichtmal die halbe Pizza runter, hatte sofort ein extremes Übersättigungsgefühl, so gut wie es auch geschmeckt hat.
Abends, aufgewärmt war der Rest dann aber wirklich klasse
Die Orangenlimo allerdings, da hätten es auch gern 2l sein dürfen, ein absolutes Erlebnis obwohl ich mich schon wieder sehr nüchtern gefühlt hatte.
So, eine aktueller Blick in die Fruchtungsbox:

Das GT-1 Myzel wächst wirklich sehr agressiv, denke ich hätt das große Casing auch gut 24h früher aus der Inkubation holen können.
Die am 2ten beimpften Gläser scheinen bisher kontifrei, nach 1xigem Schütteln viele Stellen an denen Myzel wächst. Ich dene Montag spätestens lohnen Bilder
Geschrieben von: Herr von Böde Oct 8 2015, 20:18
Beim abendlichen Substratköcheln viel mir grade dieses in die Hände:
beim durchsuchen des Sittichfutters war kein weiteres solches Korn auzuspühren.
Mir ist schon klar das Für Tierfutter strenge Richtlinien herrschen aber wenn man an die Lebensmittelskandele denkt die bei für den menschlichen Verzehr gedachten Lebensmitteln alltäglich geworden sind will ja man ja erst recht nicht wissen was beim Tierfutter so abgeht^^
Kennt jemand dies Saat oder hab ich da tatsächlich ein Mutterkorn entdeckt ??
Geschrieben von: hogie Oct 8 2015, 20:33
Das ist schon Mutterkorn. Selbst im Biogetreide, das für menschlichen Verzehr gedacht ist, waren immer wieder einzelne Körner zu finden. Ich habe jetzt nicht nach geschaut, wie die genauen Vorschriften sind. Aber für echte Vergiftungserscheinungen brauchst du schon einen Anteil von ungefähr 1%. Der Anteil ist um Größenordnungen niedriger.
Geschrieben von: Herr von Böde Oct 8 2015, 20:43
Gut, harmlos fürn 88kg Menschen wie mich.
Aber was wiegt son Wellensittich 30g die überzüchteten Tiere? oder 15 g ein Zebrafink, für die das Futter auch sein soll ![]()
Geschrieben von: hogie Oct 8 2015, 22:24
Da habe ich mir jetzt noch nie Gedanken gemacht. Ich könnte mir aber vorstellen, dass der das Mutterkorn erst gar nicht frißt und das Problem deshalb keine bedeutsame Rolle spielt. Als Mutterkorn ein massives Problem war, hat die Körner auch niemand vorsätzlich gegessen, sondern der verbackene Anteil im Brot war einfach zu hoch.
Geschrieben von: Herr von Böde Oct 8 2015, 22:52
Ja stimmt, wenn der Pilz sich schon die Mühe macht solch toxische Alkaloide zu produzieren um nicht gefressen zu werden sind ein paar nette Bitterstoffe oder Ähnliches vielleicht auch parat, so dass es gleich wieder ausgespukt wird.
Werde das jetzt aber mal nicht testen ![]()
Hm, ich frage mich ob ich das Casing doch noch patche oder nicht, Myzel ist schon sehr dicht ![]() bin hin und her gerissen...
bin hin und her gerissen...
Einfach nochmal ne locke -nicht als solche zu bezeichnende- Schicht Vermi aufstreuen?? Hm..
Geschrieben von: hogie Oct 8 2015, 23:14
Ich habe die Dinger auch nie probiert, sondern immer gleich weg geworfen. So geht es uns halt, wenn Blinde von Farben reden
Geschrieben von: Herr von Böde Oct 8 2015, 23:28
Auch dazu ists ja ganz nützlich isoliertes Myzel zu haben, man kann vergleichen.
Werd dieses Casing wohl einfach so lassen, das nächste genauso basteln und in der selben Situation dünn Vermi aufstreuen um zu schauen obs wesentliche Unterschiede gibt.
Schön zu sehen, am Dosenrand Rhizome, das Myzel sucht offenbar neue Besiedlungsmöglichkeiten:

Geschrieben von: hillage Oct 9 2015, 00:57
noch bevor ich das erste mal LSD genommen hatte, hatte ich 2 trips
nun, ich würde es heute sogar für möglich halten, dass man dies dem vogel nicht mal ansehen würde!
Geschrieben von: Herr von Böde Oct 9 2015, 03:57
![]() joa, ne 250er Mikro würd ich zwar nicht unbedingt für die allerbeste Piepmatzernährung halten aber das der von der Stange kippt würd ich auch nicht unbedingt erwarten...wenn auch Freiflug für die nächsten Stunden gestrichen wäre...
joa, ne 250er Mikro würd ich zwar nicht unbedingt für die allerbeste Piepmatzernährung halten aber das der von der Stange kippt würd ich auch nicht unbedingt erwarten...wenn auch Freiflug für die nächsten Stunden gestrichen wäre...![]()
Aber son Mutterkorn enthält ja nun doch noch ganze Menge anderes übles Zeug ![]()
Edit 06:42 Uhr:
Bevor ich mich tagelang herumärgere und zweifle nun doch trockenes Vermiculite locker aufgestreut (lässt sich einfach gleichmäßiger ohne dickere Bröckchen verteilen, sozusagen pudern) und sofort reichlich eingesprüht.
Hatte einfach das dringende Gefühl es sei besser so.
Lieber jezt als zu warten bis es schon zu Pinnen anfängt ![]()

Geschrieben von: fluchsDirMaus Oct 9 2015, 10:44
Herr von Böde, schöner Bericht.
Geschrieben von: Herr von Böde Oct 9 2015, 13:28
Danke fluchsDirMaus ![]()
Wie schon angedeutet eine Erweiterung auf Speisepilze wird bald kommen.
Hab einen Raum der bisher nur für Terrarien im Winter (Überwinterungsraum im Keller) genutzt wird und auch im Sommer selten über 17Grad hat.
Der lässt sich gut und sicher Lüften, so werd ich zB. mal Indoorversuche mit Seitlingen (aber evtl. auch mit psychoaktiven Holzbewohnern) anstellen.
Bei bestehendem Interesse wird hier evtl. in einem neuen Fred berichtet...
Geschrieben von: hogie Oct 9 2015, 17:02
Ich kann dir den südlichen Schüppling empfehlen. Obwohl er leicht zu züchten ist und super schmeckt, kann man ihn praktisch nirgends kaufen. Denn für die Logistikkette von der Pilzfarm bis zum Teller ist er nicht robust genug. Für den Homegrow ideal.
Geschrieben von: Herr von Böde Oct 9 2015, 17:44
Ja, den hattest schonmal erwähnt, war auch schon auf der Liste .
Danke für den Tipp ![]()
Denke Mitte-Ende Nov. wirds losgehen.
Edit:
ein PFO Casing musste entsorgt werden, weisse Pünktchen auf 3 mini Wichteln, wird Schimmel gewesen sein.
Trotzdem nicht verschwendet, Blaptica dubia (Futtertier) freut sich offenbar über die Abwechslung: trotz Licht ein enormer Ansturm. ![]()

Geschrieben von: Herr von Böde Oct 12 2015, 15:17
Gibt nicht viel Neues, das große Casing macht noch keine Anstalten Myzelverdichtungen zu bilden aber der Strain soll ja eh ein paar Tage länger brauchen, die Spannung steigt ![]() .
.
Eins der A+ Quarkdosencasings hatte im 3ten Flush einen einzelnen sehr großen FK (19 g), das selbe Casing setzt aber tasächlich nochmal diesmal mit mehrern Fks einen Flush an aber ich denke die verhungern unterwegs.
Das Heimchendosencasing produziert grad den 3ten Flush mit 4 oder 5 Fks.
Habe aber leider etwas Probleme mit der Temperatur in der Fruchtungsbox, gehen teilw. sehr hoch 26/27 Grad was mit dem Start der Raumbeheizung zu tun hat.
Das ganze steht jetzt erstmal auf dem Boden (da sollte es etwas kühler sein als auf Hüfthöhe).
Natürlich beheize ich mein Wohnzimmer (alle anderen Räume wären für die Box zu kühl, teilw. keine 18 Grad) nicht auf solche Temperaturen, mir ist noch nicht ganz klar welcher Effekt die Temperaturen in der Box wirklich so stark ansteigen lässt.
Morgen, Übermorgen mal wieder mehr. ![]()
Edit:
Bietet sich grad doch noch die Möglichkeit ein paar Bilder einzuschieben:
Die Fruchtungsbox:
Das A+ Heimchendosencasing:
Das A+ Quarkdosencasing 4 Flush:
Ein A+ Quarkdosencasing 2 oder 3 vor dem 3ten Flush:
Ein weiteres A+ Quarkdosencasing 2 oder 3 vor dem 3ten Flush:
Das verbliebene PFO Casing, die FK werden jetzt etwas größer:
Das Rieseneisdosencasing mit dem GT-1 Myzel, gefällt mir nach dem Aufstreuen der Vermiculiteschicht weit besser:
Geschrieben von: Herr von Böde Oct 14 2015, 17:29
So, das PFO Casing wurde gestern abgeerntet (komplett)= 32g,

mal schauen wie sich das noch so weiterentwickelt, schön ist was anderes.
Zb: der 3te Flush des A+ Heimchendosencasings entbehrt nicht einer gewissen
Ästhetik:
dazu kommt praktischerweise das der Strain sich bisher wirklich als sehr ertragbringend erwiesen hat.
Das Quarkdosencasing im 4ten Flush:
Die beiden anderen Quarkdosencasings (3 Flush):

Nichts Neues im Rieseeisdosencasing:
Die Box:
Da heute Morgen geschüttelt wurde und somit erstmal nichts zu sehen ist, noch keine Bilder der Gläser.
Kontis gibts bisher scheinbar keine.
Das A+ Myzel scheint diesmal deutlich schneller zu sein (das kann an der Füllmenge und der Größe der Impfstücke liegen), denke 3 A+ Gläser und 1 GT-1 Glas sind in 3-5 Tagen bereit zu Casen. ![]()
Geschrieben von: Herr von Böde Oct 15 2015, 06:26
Das Heimchendosencasing wurde grade abgeerntet, hätte man es mir beim ersten Anblick der 5-6 Wichtel gesagt - als als sie grad zu spiessen begannen- hätte ich es nicht geglaubt: Nochmal satte 60 g im 3ten Flush !! Der größe FK hat 20 g !!
Ich hab das Gefühl das die FK größer sind als beim ersten Flush, evtl. hatte ich auch etwas zu früh geerntet.
Bei diese Pilzen gibts noch keinen Riss in einem Velum ( ![]() wer kennt den Plural von Velum ??
wer kennt den Plural von Velum ?? ![]() ) , bin aber die nächsten h nicht da, darum jetzt die Ernte.
) , bin aber die nächsten h nicht da, darum jetzt die Ernte.
Vorher:
Nachher:
mit Feuerzeug als Maßstab:
Geschrieben von: Herr von Böde Oct 15 2015, 10:17
Ich vergess es immer wieder:
Ich brauch mal nen Tipp zur Herstellung eines angesäuerten, auf Ethanol (vergällt, Brennspiritus) basierten Desinfekts:
Der Spiritus hat 94 %, dh. um 125 ml Desinfekt anzumischen fülle ich derzeit 98,4 ml Brennspiritus mit 26,6 ml (Leitungs-)wasser auf (in der Praxis wird gerundet, also 98,5 ml Spiritus mit 26,5 ml Wasser.
Dies sollte (wenn ich mich nicht grob verhauen haben ![]() ) eine 74% ige
) eine 74% ige
Desinfektionslösung ergeben.
Da ich nun ein recht hartes Leitungswasser nutze und ein ansäuern oft empfohlen wird Frage ich mich wieviele Tropfen Essigessenz dürfen es sein ? 2 oder 3 ??
Habe im Netz leider nichts wirklich hilfreiches gefunden...
Hier weiss doch gewiss jemand Rat ![]()
Danke schonmal !!
Geschrieben von: hogie Oct 15 2015, 15:18
Für ca. 125ml komme ich auf
93ml Brennspiritus
31ml demin. H2O
ca. 1ml Essigessenz 25% sollte noch vertretbar sein.
Kein Leitungswasser nehmen. Zwischen 70 und 80% (Vol) sind ok. Exakte Konzentrationen könnte man eh nur durch Wiegen herstellen. Auch Umrechnen mit der Dichte klappt bei Wasser/Ethanol-Gemischen nicht.
Geschrieben von: Herr von Böde Oct 15 2015, 15:54
Danke, wobei bei der Rechnung dürfte ich ehr im weit unteren 70%igem Bereich liegen ?
Wegen der Schwierigkeit der exakten Berechnung (Volumenkontraktion) habe ich immer Konzentrationen von ehr über 73 % angestrebt um im sicher Bereich zu bleiben.
Gerechnet habe ich folgendermaßen:
Zielmenge X Zielkonzentration / Ausgangkonzentartion = nötige Menge des Brennspiritus in Ausgangskonzentration.
Ich würde nun also schlicht 1ml des Auffüllwassers durch E.essenz ersetzten, passt das so?
Und wegen des Auffüllwassers, kann ich nicht einfach 20-30 ml (die sind beim Kochen ja rasch zusammen) Wasser aus kondensiertem Dampf abfangen (an einer schräg stehenden Scheibe abperlen lassen und auffangen) oder ist das zu stark durch Staub etc. verunreinigt?
Ich meine wozu kaufen wenn es doch fast tgl. als ungenuztes Abfallprodukt in weit ausreichenden Menge anfällt ![]()
Edit:
![]() Im GT-1 Casing tut sich langsam was:
Im GT-1 Casing tut sich langsam was:



Edit II
In den (tatsächlich kontifreien) Gläsern ist heute auch wieder gut der Fortschritt auszumachen.
Was das steriele Arbeiten angeht scheint es inzwischen ziemlich reibungslos zu laufen ![]()
A+1 Myzel

GT-1 Myzel

Geschrieben von: hogie Oct 15 2015, 22:21
Wegen der Schwierigkeit der exakten Berechnung (Volumenkontraktion) habe ich immer Konzentrationen von ehr über 73 % angestrebt um im sicher Bereich zu bleiben.
Ja das passt scho
Ich habe für eine Zielkonzentration von 70% gerechnet. So wichtig ist es für Desinfektionszwecke ja nicht. Kondensiertes Wasser sollte schon gehen, doch solltest du den 7x% verdünnten EtOH einige Zeit stehen lassen, dass er sich möglichst selbst desinfiziert.
Allerdings halte ich es für am falschen Fleck gespart, denn das demin Wasser bei den Discountern ist so billig und sehr hoher Qualität. Man braucht es immer wieder.
Geschrieben von: Herr von Böde Oct 15 2015, 23:00
Ok, wird mal nen Kanister angeschafft ![]()
Alledings würde ich ja onehin die Mischung anrühren nicht wenn ich sie grade brauche, sondern wenn grad das Kondenswasser zur Verfühgung steht, so dass bis zur Benutzung dann sicher mal 2-3 Tage vergehen können. ![]()
Geschrieben von: Herr von Böde Oct 16 2015, 13:10
Ich war grad mal einkaufen, Herr ALDI hat tatsächlich keine E.essenz, hab dann mal einfach 5%igen Wein (25%) - / Branntwein (75%) - essig mitgebracht.
Dachte die Umrechnung - eben 5 statt 1 ml- ist nun wirklich kein Problem, zu spät viel mir dieser Beitrag ein:
Ich verwende einfach 70% Isopropanol. Du kannst sogar einfachen Brennspiritus mit destilliertem Wasser auf 70% herunter verdünnen. Der ist genauso wirksam, stinkt bloß unangenehm. Am besten noch etwas mit synthetischer Essigsäure (kein Weinessig) ansäuern.
Ok, was ist das Problem beim Weinessig ? Kann ich meinen nehmen ?

Edit :
Wenn das Problem die Essigsäurebakterien sind die meinen Alkohl abbauen dürfte das in eine so kleinen Charge (125 ml) ja nicht ins Gewicht fallen wenn die Lösung nun doch mit gekauftem demin. Wasser hergestellt und direkt verbraucht wird ?
Überleben die überhaupt solche Alkoholkonzentrationen?
Geschrieben von: hogie Oct 16 2015, 16:11
Ok, was ist das Problem beim Weinessig ?
Diesen Weinessigverschnitt verwende ich auch in der Küche schon lange nicht mehr, weil er alles versaut.
Ich gehe davon aus, dass die das nicht überleben. Sonst würde sich der Einsatz von Essigsäure hier verbieten. Hatte aber noch nie Probleme damit und Essigsäure gewählt, weil sie rückstandslos verdunstet und nicht so fies wie HCL ist. Vielleicht ist Essigsäure aber doch nicht so gut, weil sie durchaus geringste Mengen an Nährstoffen enthält. Weinessig ganz bestimmt noch sehr viel mehr als die synthetische Essigsäure, die man liebevoll als Branntweinessig bezeichnet.
Geschrieben von: Herr von Böde Oct 16 2015, 17:08
Ok, sollte also gehen, Versuch macht kluch...
Kann natürlich eine typische Verschlimmbesserung werden wenn das Vorteil bringende Ansäuern des Desinfekts dieses plötzlich zur Kontischleuder macht ![]() .
.
Aber vorhandenes oranisches Material welches enthalten ist wird in der Praxis wahrscheinlich nur Probleme mit den Düsen von Sprühköpfen machen.
Solange nichts lebt auf dem organischen Material sollte man halt beachten keinen Hepa damit anzusprühen oder Polifylstopfen damit zu spühlen.
Edit :
Ich selbst vermeide übrigens in aller Regel jedes säuerliche Essen, gibt sofort Sotbrennen. Salat nie im Leben mit Essig !!
Noch ein paar Bilder:
Die Box, unten Rechts das Casing im 4ten Flush, da verhungert offenbar gar nichts unterwegs ![]() ich denke mal der einzelne Fk war wohl tatsächlich nur ein Nachzügler des 2ten Flushes
ich denke mal der einzelne Fk war wohl tatsächlich nur ein Nachzügler des 2ten Flushes
Im GT-1 Casing wichtelt es nun wirklich, offenbar bildet das Myzel faule Fk, die meisten wachsen fast liegend ![]()





Edit II :
Ein-zwei Fragen zum Einlagern von Myzel.
Als Agar würd ich wohl Haferflocken als Nährstoffliefernat wählen, der Abwechslung wegen und irgendwo stand zu lesen das dieses Agar sich wegen der relativ geringen Nährstoffkonzentration besonders zum Einlagern eignet.
Macht es Sinn dafür vorgesehenes Myzel vorher nochmal über ein völlig anderes Substrat (ich dachte an süßen Dosenmais) zu schicken (würde diesen dann direkt aus den jetzt bewachsenen Gläsern beimpfen) oder besser erst nach der Pause auf dem Haferflockenagar (würde dann eben einzele Körner aus den jetzt bewachsenen Gläsern auf das Agar legen)?
Ausserdem- die Temperatur kann wahrscheinlich direkt verringert werden, sobald zu erkennen ist das Myzel das Agar besiedelt oder besser länger warten bis die Petrie stärker bewachsen ist?
Alle Tips zum Einlagern von Myzel sind natürlich sehr willkommen ![]()
Geschrieben von: Herr von Böde Oct 17 2015, 23:06
Ein paar neue Casings:
die Gläser stehen hinter den Schalen auf die sie verteilt wurden.
Ganz links 2 große A+-1 Gläser hinter einer XXL-Heimchendose, die Dose hat die selbe Grundfläche ist aber 1/3 höher als die normalen XL Heimchendosen.
Ich möchte einfach wissen was eine höhre bzw. doppelt Substratschicht auf gleicher Grundfläche bringt, mit isolierter Genetik sollten solche Experimente halbwegs aussagekräftig sein ![]()

Rechts davon ein A+I Glas für die kleinere Vergleichsschale, und noch weiter rechts 2 GT-1 Gläser mit ihren Schalen.
Step by step (der A+-1 Vergleichscasings), um evtl. ne Vorstellung vom Aufbau zu haben, genaus Nachmessen scheint doch etwas unpraktisch:
Bodenschicht
+Brut, 1= hohe Schale; 2= "normale" Schale
(etwas spät ans Foto gedacht ![]() )
)
+Deckschicht


Beim Aussprühen der Schalen mit dem angesäuerten Ethanol-Desinfekt konnte ich übrigens einen angenehmen Effekt festellen:
Es stinkt nicht mehr wie in einer Fuselbude sondern wie im Schminckkämmerlein mancher Frauen, es richt ehr nach Aceton ![]()
Noch 2 Bilder der aktuell fruchtenden Casings:
Die GT-1 Wichtel beginnen sich doch noch aufzurichten ![]()

Das lezte noch nicht abgeerntete A+ Casing.
Das Casing welches ich schon dem Hungertod nahe sah brachte im vermeindlich 4ten Fluch 60 g!!
Das andere knapp 41.
Da mir das verbliebende PFO-Casing gar nicht gefallen hat (über/auf der Casingschicht befand sich eine massive -im Sinne des Wortes- Schicht Aborts und Myzel), man konnte das wohl nur als extremstes Overlay bezeichnen, habe ich eine Radikalkur vorgenommen:
Mit Scalpell wurde die Casingschicht dicht über der Körnerbrut abgeschnitten, also eine dicke Scheibe der Oberfläche komplett entfernt.
Im Anschluss daran - nach dem gründlichen Entfernene sich verirrter Fks, die teilw. sogar aus der unteren Perliteschicht wuchsen - wurden die eingeschrumpften Seiten und die dünne Restcasingschicht erneut Eingecased.
Auf erneute Inkubation wird verzichtet.
Ist ein Experiment ... will mal sehen was son Casing mit sich machen lässt ![]() . Hab natürlich trotzdem möglichst steriel gearbeitet.
. Hab natürlich trotzdem möglichst steriel gearbeitet.
Edit 18.10. 09:05 Uhr:
Falls noch jemandem etwas zun lezten Teil meines vorherigen Beitrages einfällt, immer gerne !
Das lezte A+ Casing vor der Ernte, spaßeshalber mal ein Maßbrand an die Box gehängt, die Fk sind bindestens 12, ehr 15 cm lang ![]()

Ergebniss : 73,5 g...
Geschrieben von: Herr von Böde Oct 19 2015, 01:16
Die beiden Gt-1 Heimchendosencasings stehen jetzt (noch verschlossen) auf
dem Inkubator, in die Fruchtungsbox gehts sobald sich Myzel zeigt.
Hoffe dem Overlay so ohne zusätzlichem Patchen entgegewirken zu können.
Das schon weiter fortgeschrittene Casing mit dem Myzel, inzwischen sind "richtige" Fks entwickelt ![]()



Geschrieben von: hogie Oct 19 2015, 01:25
wunderschön!
Geschrieben von: Herr von Böde Oct 20 2015, 14:39
Beide A+1 Casings zeigen Myzelwachstum an der Oberfläche - morgen, übermorgen gehts in die Fruchtung ![]()
Das PFO Casing dankt die Rosskur immerhin schonmal mit einem , gar nicht mehr zwergenartig wachsendem FK :
Das große GT-1 Casing:
Geschrieben von: hogie Oct 20 2015, 19:06
Irgendwie finde ich die viel schöner als die blassen Heinopimmel ![]()
Geschrieben von: Herr von Böde Oct 20 2015, 19:21
![]() Was für ein Gedanke !!
Was für ein Gedanke !! ![]()
Damit ists dann vorbei mit dem Genuss frischer Pilze ![]()
Geschrieben von: Herr von Böde Oct 21 2015, 14:22
Ist dieser PFO nun doch ein Golden Teacher ![]()
Nach der Radikalmaßnahme sehe ich keinen großen Unterschied mehr:
und ein 2ter FK drückt sich nach oben:
Der erste Flush des sicheren Gt-Casings ist morgen wohl soweit, evtl. kann in 2 Schritten geerntet werden:
Die alten A+ Casings sind erstmal umgezogen.
Die neuen, erstes Bild die XXl Heimchendose, 2tes Bild die XL Heimchendose:

Die "Haupt"-box:
Geschrieben von: Herr von Böde Oct 21 2015, 20:54
Nun war es doch schon heute abend soweit, der erste Teil des ersten Flushes konnte geerntet werden.
Man sieht, es ist so weit:

Der erste Teil brachte 56g:
Der Rest kann sicher noch gut eine Nacht vertragen:
Geschrieben von: Herr von Böde Oct 22 2015, 08:51
In der Nacht bzw. grade eben wurde noch 2x gepflückt, 1x 33g und 1x 36 g.
Noch immer steht dieses und wird wohl bis zum Mittag noch zulegen dürfen:

Das durch Feuchtigkeitsverlust verursachte Zusammenziehen des Casings ist im oberen Bild an den sich bildenden Spalten an den Schalenrändern schon wieder gut zu sehen.
Wird wohl von heute Mittag bis morgen Früh gedunkt.
Edit 14:39 Uhr
Das 4te und lezte Pflücken des ersten GT-1 Flushes brachte nochmal satte 74g, insgesamt im ersten Flush 198g ![]()
Geschrieben von: Herr von Böde Oct 23 2015, 04:51
Bei dem PFO oder GT Casing bin ich mir inzwischen tatsächlich überhapt nicht mehr sicher um welchen Strain es sich nun wirklich handelt.
Wenn man diesen FK mit den Bildern weiter Oben vergleicht haben sich seit dem Entfernen der alten Casingschicht die Eigenschaften umgedreht, der Fk hat eine normale Größe, ist nicht mehr massiv sondern fühlt sich (darum auch kein Klonkanditat) ehr ziemlich hohl an (hab das brutale Antouchen mal gewagt, heut Abend wird wahrscheinlich eh gepflückt).
Der Hut allerdings scheint dunkel zu bleiben:
Der 2te sichtbar gewordene Fk ist wohl ein Abort, kein Zuwachs festzustellen.
Die Fruchtungsbox, oben die A+, unten die Gt Casings, das große GT Casing wird gleich abgegossen und gesellt sich dann wieder dazu:
Edit 16:14 Uhr
Der FK hat jetzt eine Stiellänge von 10 cm un der Hut bei unbeschädigtem Velum ist 4,5 cm breit. Kann das überhaupt noch ein PFO sein ??

EDIT II
Mit Abstand der größte und schwerste von mir hochgezogene Fk, es kann wohl kein PFO sein oder?
Kann das jemand erklären?
![]() ja, die Schale unter dem Fk wurde austariert ...
ja, die Schale unter dem Fk wurde austariert ...
![]()
Geschrieben von: hogie Oct 24 2015, 01:19
Das mit den Strains bei Cubensis ist eh völlig Quatsch. Die Zuordnung ist völlig willkürlich. Teilweise bezieht sich ein bestimmer "Strain" nur auf einen angeblichen Fundort in der Vergangenheit und es ist kein Wunder, dass sich ein und die selbe Genetik unter verschiedenen Aufzuchtbedingungen oft verschiedener verhält, als unterschiedliche Strains.
Geschrieben von: Herr von Böde Oct 24 2015, 03:51
Schade das man den nicht in der Größe fest bekommt, sonst würd ich den glatt konservieren und eingerahmt an die Wand hängen oder als Deko in ein Terrarium stellen ![]()
Geschrieben von: Herr von Böde Oct 25 2015, 00:05
Wollte grad eine Petrie zum Beimpfen hernehmen und mir kommen Verfärbungen ins Bewusstsein, ich hab das zwar schon längst gesehen, aber irgentwie drüber weg gesehen, nicht beachtet.
Ging wohl einfach davon aus es käme bspw. von der Feuchtigkeit in der Petrie...
Aber jetzt wo es ernst wird... frag ich lieber doch nochmal.
Das Myzel scheint unbeeinträchtigt. Irre ich wenn ich von einer natürlichen Myzelferfärbung ausgehe und es ist doch ein Konti ? ![]()




Es geht um das leicht Gelbliche.
Evtl. kann man es noch erahnen: es handelt sich um eine der Petris in denen ich testen wollte wie identisches Myzel sich verhält wenn es von 2 Impfstücken aus zusammenwächst.
Da schliesst sich dann gleich die 2te Frage an.
Das Myzel von den Impfstücken ist wohl identisch oder sieht ein Zusammenschmelzen bei identischem Myzel noch anders aus?
Geschrieben von: Herr von Böde Oct 25 2015, 20:51
Na, niemand eine Meinung zu den Verfärbungen ??
Beeimpfung damit hat aber stattgefunden ![]()
Das lezte Bild des ersten A+ (mulitsporen) Heimchendosencasings:
Hab die beiden größeren Fk mal abgenommen, der Rest bleibt bis morgen noch stehen.
Der 4 Flush zeigt nun deutlich Mangel (obwohl ich muss zugeben, diese Casings standen jetzt wenig optimal, in - klarsicht- Plastiktüten). Rechts der Fk knickte direkt um nachdem die stützende Folie weg war.
Der andere FK auch ehr hohl und dünn.
Die 3 andern Quarkdosencasings sehen nicht viel anders aus, ist halt das (wenig spektakuläre) Finale.
Die Box:
Wie man sieht, trotz Inkubationsverzicht (quasie nur 24 h) sind die GT-1 Schalen, unten stehend, vollständig bewachsen.
Das isolierte A+1 Myzel (oben klinks und rechts) ebenfalls nicht schwächlich.
Das Eisdosencasing sezt (auf der Aufnahme höchstens zu erahnen) zum 2ten Flush an.
Geschrieben von: Herr von Böde Oct 30 2015, 00:23
Ich glaube ich habe mit ziemlichem Overlay zu kämpfen, beim GT-1 wars klar aber auch das A+-1 Myzel bewächst fleissig jede neu aufgestreute Schicht Vermiculite und plant offenbar noch keine Fruchtkörperbildung.
Im großen Eisdosencasing mit dem GT-1 Myzel gut zu sehen das die größeren Cluster auch nur dort wachsen wo relativ wenig weiss (also Myzel) in der Deckschicht ist, der Ertrag ist also meiner Meinung nach- offensichtlich massiv eingeschränkt.
Leider ist zu der Thematik kaum etwas im Netz zu finden, falls also niemand an dieser Stelle noch brauchbare Tipps dazu hat tut sich ein wirklich weites Feld von möglichen Experimenten auf ![]()
Das kleine vermeintliche PFO Casing fruchtet trotz der Radikalbehandlung langsam und stetig vor sich hin, wenn es diesmal wieder so riesenhafte FKs gibt wird doch nochmal das Klonen in der Glovebox versucht.
Bin also für jeden Tipp dankbar der es mir erspart Blödsinniges auszuprobieren ![]()
Die Box
GT-1 Eisdose , 2ter Flush:
Geschrieben von: Herr von Böde Oct 31 2015, 02:55
So der lezte Teil des 2ten Flushes vom großen Eisdosencasing wurde grade abgepflückt. Der 2te Flush brachte insgesamt 219 g.
In einem der beiden andern GT-1 Casings scheint es langsam loszugehen mit der Fruchtung.
Geschrieben von: angel of death Oct 31 2015, 19:01
Das sieht echt verdammt gut aus!!
Aber wass machst du mit all den pilzen? Ich hatte glaube ich vor 5 Jahren ein paar Flushs gezüchtet und hab immer noch nicht alle verputzt^^
Sendest du Sporen an FSRE??
Geschrieben von: Herr von Böde Nov 1 2015, 03:44
Bisher sind noch keine Sporen an FRSE gegangen, ich traue der Quali meiner Abdrücke noch nicht genug.
Hab bis jetzt (war einfach kein Bedarf) nur testweise 2 A+ Abdrücke verwendet die leider auch komplett ausvielen.
Vernünftige Abdrücke zu bekommen wird ein nächstes Ziel, schon allein um die ganze Zucht ein wenig runterfahren können und sichere Sporen als Backup zu haben.
Im Moment werden die Fruchtkörper gewogen und entsorgt (Schabenfütter, die stürzen sich darauf) ich hab nämlich fürs nächste Jahr (wenn ich von einer monatlichen Reise ausgehe) ebenfalls genug.
Abgeben oder gar verkaufen möchte und werd ich nicht und Pfundweise Pilze zu lagern macht diese weder besser noch meinen Schlaf ruhiger ![]()
Geschrieben von: Herr von Böde Nov 2 2015, 07:55

Solche "Knubbel" liessen mich vorgestern annehmen die Fruchtung ginge bei den GT-1 Casings los.
Ganz falsch ist es wohl nicht aber bisher ist in beiden Casings insgesamt nur 1 wirklicher Pin zu entdecken :
Die beiden zu vergleichenden (400ml und 800 ml Brut auf gleicher Fläche) A+_1 Casings wollen jetzt aber eindeutig:

Edit:
Joa, auf dem ersten Bild oben sieht man - habs erst auf dem Foto entdeckt - unterhalb des "Knubbels" am unteren Bildrand zwei weitere Pins, einen deutlich mit Hut und einen noch völlig weissen ![]()
Geschrieben von: Herr von Böde Nov 3 2015, 10:54
Nun tut sich richtig was, in diese Phase kann man echt fast zuschauen ![]()
Die Box
Bei den A+1 Casings zeigt sich mir zum ersten mal deutlich was selektiertes Myzel für einen Unterschied machen kann, es brauchte etwas länger bis zum Fruchtungsbeginn dafür sieht es aber nach einer Menge brauchbarer Fruchtkörper aus.
A+1 /400 ml
A+1/800ml
Die beiden GT-1

Geschrieben von: Herr von Böde Nov 5 2015, 22:34
Im ersten Flush sicher keine bedeutenden Unterschiede zwischen den 400 und 800 ml A+1 Casings auf gleicher Grundfläche.
A+1 (400 ml)
A+1 (800 ml)
Beim GT-1 Myzel bin ich mir inzwischen nicht mehr sicher wie gut die Myzelselektion tatsächlich war.
1
2
Die Box
Geschrieben von: Herr von Böde Nov 7 2015, 20:22
Das erste der kleineren GT-1 Casings wurde in 5 Etappen abgeerntet und brachte 94,5g.
Das zweite ist noch nicht so weit:
Jedoch waren 2 Fruchtkörper etwas vorraus und sind schon gepflückt (11,3 g).
Das die Myzelisolation sehr erfolgreich war steht also nochmehr in Frage.
Das große Gt-1 Casing entwickelt zum 3ten mal Fruchtkörper:
Auch bei den beiden A+1 Vergleichscasings sieht es - nicht so dramatisch- unterschiedlich aus.
Das 400ml Casing ist etwas weiter und auf den ersten Blick ist evtl. sogar ein höher Ertarg als im 800 ml Casing zu erwarten:
400 ml
800 ml
So und nun nochmal eine Frage an die echten Experten ![]()
Ich hoffe die Bildquali reicht zumindest für eine Einschätzung, es geht nochmal um die zwei Impfstücke auf der selben Agarplatte. Identisch oder nicht, das ist die Frage.
Ich habe leider noch keine Vergleichsmöglichkeit mit definitiv unterschiedlicher Genetik, evtl. wärs schlau gewesen dieses Experiment zuerst durchzuführen ![]()
Also, traut sich jemand zu etwas zu sagen:

nochmal im Gegenlicht:
Geschrieben von: angel of death Nov 7 2015, 21:36
ob die identlisch sind lässt sich wohl nur mit Mikroskop bzw Gentest ermitteln, ein paar verschwommene Handyfotos bringen da gar nichts :D
Ich schätze du meinst diesen "Canyon" in der Mitte. Wenn du dir unsicher bist dann benutz doch jeweils nur eine Hälfte zum beimpfen von Substrat, oder selektier weiter auf Petrischalen
Geschrieben von: Herr von Böde Nov 7 2015, 21:57
Nein, ich habe ja mit absicht die Petri mit zwei Impfstücken beimpft die von vermeintlich identischem Myzel stammen.
Es ist ein Experiment, die Petri ist nicht gedacht um damit weiter zu beimpfen, ichdenke das Myzel ist inzwischen auch zu alt um noch lange damit zu arbeiten.
Ich bin davon ausgegangen das isolierte Myzelien sich relativ deutlich von einander abgrenzen wenn sie beim Wachstum aufeinandertreffen und nicht identisch sind.
Um in Zukunft abschätzen zu können wie deutlich das ist (zB. um nicht unnötig viele Petris mit unerkannt identischem Myzel zu besetzen und als Backup einzulagern) diese Versuche (Petris mit identischem Myzel und sicher differentem Myzel zu beimpfen).
Das GT-1 Myzel hielt ich für gut isoliert, sicher 7-8x überimpft, das Ursprungsstück aus einem PF-Cake war kein halber mm groß und Teil einens Rhizoms (dachte ich ![]() ).
).
Da ich inzwischen an der sichern Isolation des genannten Myzels Zweifel habe und auch auf der Agarplatte durchaus soetwas wie Abgrenzungen zu erkennen sind von denen ich nicht abschätzen kann ob es echte Abgrenzungen sind oder einfach nur Überbleibsel der an 2 Stellen durchgeführten Beimpfung, zudem das Gegenexperimet (die Beimpfung mit sicher unterschiedlicher Genetik) noch nicht so weit ist hoffe ich das jemand mit Ahnung mir weiterhelfen kann.
Wenn es generell unmöglich ist durch diese Methode einen halbwegs zuverlässigen "Identitätscheck" durchzuführen wäre ich mit der Info auch zufrieden, allerdings meine ich anderes gelesen zu haben ![]()
Geschrieben von: Herr von Böde Nov 8 2015, 07:38
Edit 09.11. 18:35 Uhr
Das 400 ml A+1 Casing ist abgeerntet und brachte 97g.
Das 800 ml A+1 Casingasing brachte 108,5g. Und ergab etwas massivere Fk.
Boden und Deckschicht waren gleich, auf gleicher Grundfläche war also im größeren Casing nur die Brutschicht doppelt mächtig.
Geschrieben von: angel of death Nov 8 2015, 19:01
Okay, dazu kann ich leider gar nichts sagen.
Schade das Waaagh nicht mehr aktiv ist, der hatte davon wirklich Ahnung.
Zu alt dürfte das Mycel aber nicht sein. Ich bin gerade dabei Mycel zu ziehen das zwei Jahre ohne mein zutun unter meinem Bett lag. (Ein Jahr war ich überhaupt nicht zu Hause, und in dem anderen Jahr hab ich es nur hin und wieder zum nachschauen raus geholt). Es hatte seine Anlaufschwierigkeiten und wächst etwas langsam, aber es lebt definitiv noch ![]()
![]()
![]()
Geschrieben von: Herr von Böde Nov 8 2015, 21:09
Joa, bis es tatsächlich den Geist aufgiebt ist es bestimmt noch hin, obs schlau ist das abzuwarten, ehr nicht...
Sicher das es zu alt ist bin ich aber auch nicht aber es gab auf KDA schon deutlich verlangsamtes Wachstum. Auf Bieragar wuchs es wider besser.
Ich kann ander Umstände als das Alter (exakte Nährstoffzusammensetzung) die für unterschiedlich schnelles Wachstum verantwortlich sind aber nicht wirklich ausschliessen.
Ich beimpfe heute - eben um das etwas besser einschätzen zu können, nochmal 3 Gläser und 3 Petreies, mal schauen wie es wird.
Ein unter dem Bett liegende, unbebrühte Agarplatte, bzw. das Myzel darauf das nicht zerschnippelt und zum ständigen Neubeimpfen hergenommen wird altert sicher in 2 Jahren langsame als "hochbeanspruchtes" 4 Monate altes Myzel das rd alle 14 Tage auf neue Ararplatten und in Substratgläser wandert.
Mir ist darum auch noch nicht ganz klar wie man bei gründlicher Selektion das Überaltern verhindert, es sei denn ich bin völlig auf dem falschen Dampfer und 4 Monate sind - egal wie beansprucht- für Cubensismyzel gar nichts....
Geschrieben von: Herr von Böde Nov 10 2015, 07:31
So rein optisch ist der 3te Flush des großen GT-1 Eisdosencasings bisher der schönste:


Geschrieben von: Acinonyx Nov 10 2015, 11:06
Oh, hübsches Fliegenpilz-Muster!
Geschrieben von: hogie Nov 10 2015, 13:26
Geschrieben von: Herr von Böde Nov 10 2015, 17:38
Die Punkte blieben bis zulezt ![]()


195g in wirklich schön handlichen (der Spitzenreiter hatte 22g) Fruchtkörpern :
Kaum Aborts, ausserdem war dies bei dem Casing der erste Flush der wirlich an einem Stück geerntet werden konnte.
Geschrieben von: Herr von Böde Nov 16 2015, 11:38
Das 800 ml A+1 Vergleichscasing ist einer bläulichen Schimmelkonti zum Opfer gefallen... darum leider kein weiterer Vergleich möglich.
Wenn Gläser wieder bereit sind geht der Vergleich mit GT-1 weiter.
Die beiden kleineren GT-1 Schalen sind im 2ten Flush sehr unterschiedlich gereift, das erste konnte vorgestern mit 93g in einem Schritt abgeerntet werden, beim 2ten habe ich soeben 50g gepflückt es steht aber noch was, der zweite Ernteschritt wohl erst morgen.
Evtl. unterschätze ich die Wirkung des Lichtes, insgesamt steht die Box recht Dunkel, die schnell gereiften Fruchtkörper wuchsen bisher immer dichter an der Lichtquelle. Das das Zufall ist ist immer noch wahrscheinlich, wird aber bei den nächsten Casings mal genauer ausgetestet.
Geschrieben von: Herr von Böde Nov 20 2015, 19:30
Möchte zwischendurch für Interessierte nochmal festhalten das ich mit
Natriumhypochlorit (Klorix) als Sprühdesinfekt in der Impfbox annähernd ohne Ausfälle arbeiten kann, mit 70-80%igem Ethanol, egal ob angesäuert oder nicht habe ich noch immer Ausfallraten von über 50% (dem Geruch nach fast ausschliesslich Hefen).
Das gilt für Petris wie auch für Roggensubstrat.
Propanol wurde noch nicht getestet.
Werde zunächst auch beim Natriumhypochlorit 2,8-3 %ig bleiben, eine besondere Giftikkeit oder Schädlichkeit sehe ich einfach nicht, Chlorgas entsteht praktisch keines, ansonsten bleiben Sauerstoff und - zugegeben lästige- Kochsalzrückstände (verstopfende Sprühdüsen können aber leicht wieder freigespühlt werden).
Für Klonversuche ist Alkohl wahrscheinlich trotz hoher Ausfälle vorzuziehen, selbst der FK kann aussen mit Alkoholdesinfekt abgetupft werden, mit Klorix würde ich das gar nicht erst versuchen...
Geschrieben von: hogie Nov 20 2015, 20:05
Ethanol und Propanol sind vom mikrobiellen Wirkungsspektrum sehr ähnlich..
Achtung! Konzentrationsfalle!
Ich kann mir nicht vorstellen, dass du DanKlorix unverdünnt nimmst. Denn dieser enthält pro 100ml: 2.8g Natriumhypochlorit und ca. 5g Natriumcarbonat. Macht also unverdünnt 2.8% Hypochlorit. Ich habe 15% herum stehen mit Natriumhydroxid stabilisiert. Das ist nochmals eine ganz andere Liga und vom Umgang nicht mehr hausfrauentauglich
Verdünntes Hypochlorit verwendet man sogar in Pilzfarmen von Speisepilzen und besprüht die Casings damit.
Geschrieben von: Herr von Böde Nov 20 2015, 20:20
Doch, so wie es aus der Flasche kommt, direkt in die Sprühflasche umgefüllt.
Wie geschrieben: 2,8-3%ig (Konzentration schwank von Hersteller zu Hersteller offenbar leicht).
Auf die Idee ein Casing damit einzusprühen käme ich allerdings nicht ![]()
Die 13-15%ige "Chorbleiche" zu verwenden macht sicher keinen Sinn.
Geschrieben von: hogie Nov 20 2015, 20:25
Wie geschrieben: 2,8-3%ig.
Geschrieben von: Herr von Böde Nov 20 2015, 20:33
Warum nicht mehr versprühen? Meine Wohnung nebel ich ja nicht damit ein ![]()
Wenn ich da jetzt wirklich Unmengen von bräuchte wäre das hochkonzentrierte Zeugs bestimmt günstiger. Ich komm aber mit 1,5l /mtl locker aus (davon max.400 ml für diesen Zweck), spar mir das Verdünnen und es ist überall zu bekommen.
Geschrieben von: Herr von Böde Nov 21 2015, 15:23
Es gibt einen neuen Spitzenreiter unter den größten Fruchtkörperen,
aus dem 4ten Flush (ingesamt 116g) des GT-1 Eisdosencasings:
![]()
Geschrieben von: hogie Nov 21 2015, 17:16
Geschrieben von: Herr von Böde Nov 22 2015, 00:57
Trotzdem habe ich keinen Plan, wo der Rotz bei dir herkommen soll, der deine Kulturen so zuverlässig kontaminiert.
Ja, das wäre ganz sicher die interessanteste Frage.
Es scheint tatsächlich überall zu sein:
Lasse ich gefüllte Petris im (geschlossenen)DDKT abkühlen bleiben sie rein, öffne ich den Deckel
und lasse sie in Alu eingepackt abkühlen habe ich auf über 90 % Hefewachstum nach 1-3 Tagen...
Geschrieben von: Dioxis Nov 24 2015, 21:00
Trotzdem habe ich keinen Plan, wo der Rotz bei dir herkommen soll, der deine Kulturen so zuverlässig kontaminiert.
Ja, das wäre ganz sicher die interessanteste Frage.
Es scheint tatsächlich überall zu sein:
Lasse ich gefüllte Petris im (geschlossenen)DDKT abkühlen bleiben sie rein, öffne ich den Deckel
und lasse sie in Alu eingepackt abkühlen habe ich auf über 90 % Hefewachstum nach 1-3 Tagen...
Eine möglichkeit wäre vieleicht die Hefekonzentration im Raum durch Ionisatoren (zur Ozonerzeugung), UV-Licht (in einem Luftfilter) oder einer kombination daraus allgemein zu senken.
Von Chlorhaltigen mitteln kann ich immernoch nur abraten.
Wenn du einen richtigen Hammer brauchst, der auch zuverlässig sporizid ist, nimm Peroxyessigsäure (nur dann keine Ionisatoren im Raum anlassen).
Es ist selbst in niedrigen Mengen derart Wirksam, das man es benutzt um Parasiten aus Fischzuchtgewässern zu entfernen (http://www.google.de/patents/EP0944305B1?cl=de)
Lässt sich auch kostengünstig selbst herstellen.
Geschrieben von: Herr von Böde Nov 25 2015, 17:47
Ich sehe ehrlich gesagt wenig Sinn darin mit weiteren Mittelen oder gar für den gesamten Raum arbeitenden Luftfiltern oder UV-Licht zu experimentieren.
Auch weil ich ehrlich gesagt nicht sehe was am Natriumhypochlorit so böse sein soll.
Frei werdendes Chlorgas sollte weit weit unter jeder möglichen Wirkung oder Nebenwirkung erzeugenden Menge bleiben, als Rückstand bleibt Kochsalz und Sauerstoff, das stört mitunter, machst mir aber keine Angst.
Nächster Schritt wird wohl tatsächlich der Hepa sein, ob ich den aber für meine Zwecke wirklich brauche ??
Ich werds sehen wenn ich endlich an Speispilze komme (muss zugeben die letzten 2 Wochen war ich nicht mehr wirklich hinterher...).
Geschrieben von: Herr von Böde Nov 29 2015, 06:10
Testweise wurde auch der 5te Flush des großen (2500 ml-gesamt) GT-1 Eisdosencasings abgewartet, nicht mehr wirklich lohnenswert:
Der 3te Flush des verbliebenen 400 ml (Brut) A+1 Casings :
Als nächstes stehen nun tatsächlich mal ein paar PF-orig Casings (wurden in der letzten Woche nach und nach gebastelt) an, bin sehr gespannt auf die FK ![]()
Ausserdem gibt es (dem netten Spender sei nochmals gedankt !! ) unselektiertes B+ Myzel, von dem einiges in den nächsten Tagen auf Substrat überimpft wird.
Geschrieben von: Herr von Böde Nov 30 2015, 21:16
Das große (ca. 1200ml Brut+ 300 ml Boden und 700 ml Deckschicht) GT-1 Eisdosencasing brachte im 5ten Flush doch nochmal 79 g (insgesamt brachte das Casing also gute 800g Frischpilze) ohne das am Ende deutliche Mangelerscheinungen an den FK zu sehen waren- nur die Erträge brachen ein (3ter=195g, 4ter=116g, 5ter=79g)- zwei Hüte waren stark eingerissen und nicht sehr symetrisch.
Das 400 ml (Brut) A+1 Casing im 3ten Flush brachte 73 g, hier schwächelten die FK deutlicher.
Interessant dürften wohl die Schwankungen im Wirkstoffgehalt sein, ohne Labor aber nicht zu testen, unmöglich kann alles verkonsumiert werden ![]()
Noch 2 Bilder der verbliebenen kleineren (400 ml -Brut) GT-1 Casings (3ter Flush):

Geschrieben von: Herr von Böde Dec 1 2015, 04:38
![]()
Bei Mäusen wirken Pilze.
Wohl etwas unbedacht (bei den Schaben gab es gar keine Probleme, die lieben die Fk und alte Casings ![]() - wobei mir natürlich schon klar ist das Mäuse als Säuger selbsteverständlich ein relativ entwickeltes Gehirn haben - im Vergl. zu Schaben) habe ich die letzte Ernte im Stall verteilt, alte Casings haben die schon problemlos vertragen.
- wobei mir natürlich schon klar ist das Mäuse als Säuger selbsteverständlich ein relativ entwickeltes Gehirn haben - im Vergl. zu Schaben) habe ich die letzte Ernte im Stall verteilt, alte Casings haben die schon problemlos vertragen.
Jedenfalls gibt es jetzt ne ziemliche Aufrgegung, alles rennt komplett plan- und ruhelos hin und her...
Da hatte ich nicht mit gerechnet, hoffe das geht gut aus, mein schöner inzuchtfreier mit Wildmäusen rückgekreuzter Futtermausstamm ![]()
Geschrieben von: Acinonyx Dec 1 2015, 10:46
Bei Mäusen wirken Pilze.
Ich kenne jemanden, der mal einen getrockneten SKKK mit einem Stück Pizza zusammen an eine Katze verfüttert hat, die hatte angeblich danach zwei verschieden große Pupillen und war dann erst mal zwei Wochen lang weg.....
Aber theoretisch müsste es bei Kühen und Schafen dann ja auch wirken, wenn auf deren Wiese SKKK wachsen und sie die mit dem Gras zusammen fressen?
Geschrieben von: Herr von Böde Dec 1 2015, 11:09
Bei Wiedkäuern kann ich mir vorstellen das die Wirkstoffe irgendwo zwischendurch verloren gehen bzw. einfach so langsam resorbiert werden das es zu einem Wirkungseintritt gar nicht erst kommt.
Dazu kommt das die Wichtel ja vorzugsweise auf nüchternen Magen eingenommen werden, sagen wir mal 30-100 g SKK verteilt in Unmengen Zellulose dürfte einen Wirkungseintritt wohl auch nicht verbessern, aber würden man nen Kuhstall nicht mit Stroh sondern trockenen Pilzen ausstreuen, dann könnte sich auch da was tun ![]()
Vielleicht doch nicht ganz nüchtern ??
https://de.wikipedia.org/wiki/Wiederk%C3%A4uer#/media/File:Wiederk%C3%A4uendes_Schaf.jpg
Edit
Übrigens scheinen alle Mäuse wider gelandet, derzeit ist Ruhe.
Verluste gibt es keine ![]()
Geschrieben von: Acinonyx Dec 2 2015, 09:51
Ja das hab ich mir nach dem Schreiben auch gedacht, dass es bei Wiederkäuern wohl nicht so leicht wirken kann.
Schön, dass Deine Mäuse wieder wohlauf sind, wäre interessant zu sehen, ob sich irgendwelche Langzeitfolgen zeigen, beobachte doch mal die Nachkommen genau, ob da irgendwelche Verhaltensauffälligkeiten sind.
Ja, so unbedachte Sachen hab ich auch schon gemacht, ich habe mal einem Kaninchen den Stengel einer abgeernteten Hanfpflanze gegeben - ich hab gedacht, eh ich den wegwerfe, verfütter ich den doch lieber - und erstaunlicherweise war da offenbar eine Menge Wirkstoff dran. Das Kaninchen hat sich danach im Zeitlupentempo geputzt, alles gaaaaanz langsam, und saß mit einer eigenartig vibrierenden Körperspannung da.
Aber nach einer Stunde war der Spuk dann auch wieder vorbei ![]()
Ich glaube aber, dass die Tiere richtig toxische Dinge gar nicht erst fressen würden, von dem her ist die Gefahr, aus Unbedachtheit etwas anzurichten, vermutlich nicht sehr groß.
Geschrieben von: Herr von Böde Dec 2 2015, 10:23
![]() Naja, der Nachwuchs - ausgenommen auserwählte stammhaltende Damen-
Naja, der Nachwuchs - ausgenommen auserwählte stammhaltende Damen-
hatt nicht allzuviel Zeit Auffälligkeiten zu entwickeln, mit 25-30g dh. mit 8-12 Wochen müssen sie ihr Leben für das meiner Schlangen hergeben.
Zum Winter hin ist die Zeit noch viel kürzer, weil schon Neonaten oder 10-20 Tage alte Mäuschen für die Schlüpflinge des nächsten Jahres ihr Leben lassen müssen.
Ich glaub aber kaum das solche Nachwirkungen zu erwarten wären.
Dachte aber beim Lesen Deines Beitrages eben daran was mit Wildmäusen ist die soetwas fressen.
Mag natürlich sein dass das unbedenkliche Fressen der Pilze (die gerne genommen wurden) eine degenerative Erscheinung ist die auf die extreme Inzucht der Farb/Futter/Labormausstämme von Mus musculus zurückzuführen ist.
Ich bemühe mich zwar immer Männchen aus allen möglichen Teilen der Welt zu bekommen die dann jeweils mit einem Wildfangweibchen die männliche Linie meines Stammes zeugt aber der Wildmausanteil bleibt klein, ausserdem können schon aus praktischen Gründen nur solche mix-Männchen Väter werden wenn sie schon gewisse degenerative Erscheinungen vom domestizierten Vater mitbekommen (wenig Scheu, sehr kleine Fluchtdistanz, verringerter Nagetrieb etc.) .
Naja....bin hier ja nicht im Terrarienforum ![]()
Geschrieben von: Herr von Böde Dec 3 2015, 05:29
Nun zeigen auch die PF-orig Casings Anzeichen von Overlay, viele in die Luft ragende Rhizome die leider keine FK bilden werden.
Hab das zunächst bei den A+ und Gt noch auf den Zufall zurückgeführt, einfach Genetik erwischt zu haben die dazu neigt.
Einzige Casings die das so nicht zeigten waren die ersten A+ Casings mit Multimyzel :


Ein Patchen (mit reinem groben Vermi) ist inzwischen die Regel, das tut dem Gesamtertrag wahrscheinlich aber ehr gut und scheint bisher die Wichtel auch ganz gut davon abzuhalten - selbst in weissen, etwas lichtdurchlässigen Schalen vermehrt an den Rändern bzw. den Zwischenräumen dort zu wachsen, trotzdem wundern mich die in die Luft ragenden Rhizome doch sehr.
Die Deckschicht ist meist deutlich dicker wie meist empfohlen, 3-4cm ohne die zusätzliche Vermiaufstreu.
Woran mag das liegen ? Temperaturen liege in der Box ziemlich konstant bei 23 Grad, die Luftfeuchte ist teilw. aber sehr hoch, meist ü 95 %.
Auch wird nicht beleuchte, Oma hätte es schwer zu lesen bei den Lichtverhältnissen.
Geschrieben von: Herr von Böde Dec 5 2015, 08:50
Ich beginne grade mit der Myzelselektion des B+ Strains (warte die Desinfektionzeit der Box ab).
Es ist die 2te Überimpfung nach der Sporenkeimung.
Auch wenn die Petris überfällig sind entnehme ich bei diesem Durchgang aus nur einer Myzel, einfach aus Sicherheitsgünden, sollte mir die Schale so wie die "Tochterpetris" wegen irgendeines Fehlers doch mal wider verkeimen ist noch was da.
Mit den Resten der Agarplatte wird anschliessend Roggen/SiFu Substrat beimpft.
Den ersten Feheler hab ich auch schon gleich gemacht... mal schnell Fotos fürs Forum, und die Petri des Lichtes wegen auf das "olle" Pflanzenbrett gestellt.
Sowas kann man sich einfach sparen... wenn man vorher überlegt ![]()
Wie gesagt die Petris sind "überreif", Myzelstränge gut überdeckt mit flauschigem Myzel.
Also aus der Not eine Tugend machen und die einzigen erkennbaren nicht überdeckten Myzelstränge hernehem die - natürlich- nicht mehr auf dem Agar wachsen sondern bereits versuchen aus der Petri zu entkommen.
Die auf dem untern Bild erkennbaren Stränge haben den obern Rand der max. 1,5mm hoch ausgegossenen Petri bereits überwunden und wachsen stramm auf die letzte Hürde, die PET - Folie zu.
Sicher spricht das nicht für schwächliches Myzel.
Aber obs gut geht und die Stränge noch ausreichend steriel sind ??
Aber wenns gut geht sparts vielleicht 1nen oder gar 2 weitere Isolationsschritte.
Schaun wir mal ![]()


Edit
Scheint soweit gutgegangen, weniger Friemelei als erwartet.
In 3 Tagen weiss ich mehr ![]()
Geschrieben von: Herr von Böde Dec 8 2015, 15:58
So, ich habe grade mal im Inkubator gelauert und stelle erstaunt und erfreut fest, das 5 von 6 B+ Petris die mit winzigen Myzelstückcken (mit Kanüle mühsam abgekrazt und ebenso mühsam von dieser auf Agar übertragen) des oben gezeigten über den Petrirand gekrochenen Myzels beimpft wurden - zumindest schonmal hefemäßig, die sehe ich nach der Zeit- kontifrei sind und was genauso erfreut, schon deutlich Fläche einnehmen ![]()
Evtl. sogar zu erkennen: das Myzel wächst tatsächlich rhizomporph weiter, das Impfstück passte so grade in die Spitze einer großen Kanüle ![]()

(Die dunklen Stellen im Agar sind abgesetzte Partikel aus dem zur Herstellung verwendetet Hefeweizenbier)
Weiter irritiert das Fruchtungsverhalten, es handelt sich sowohl um isolierte Genetik wie auch um Multimyzelcasings:

Die Boxen stehen nun zwecks Hellikeitserhöhung unschönerweis vor einem großen Tropenterrarium welches im Winter (die Bewohner mögen keine Überwinterung) in Betrieb bleibt. In einer Box wurde die Luftfeuchte abgesenkt.
Aber noch immer nirgendwo Pins zu sehen.
Bei den "weissen" Casings (hab absichtlich nach der Vermiculiteschichtextraschit =Patchschicht nichts mehr weiter aufgestreut oder gepatched um zu sehen was passiert) kann man doch wohl deutlich von Overlay sprechen oder ?
Geschrieben von: Herr von Böde Dec 9 2015, 20:00
Nun also doch, die ersten beiden A+ Pins lassen sich Blicken, (ganz links kommt auch einer ![]() )
)
(Im Beirag über diesem das Casing im untern Bild unten links)
Geschrieben von: Herr von Böde Dec 12 2015, 00:36
Die A+ wachsen, sieht aber nicht nach einem überwältigendem Ergebnis aus:
In der selben Fruchtungsbox auch endlich die ersetn 2 "sicheren" PF- original Fruchtkörper zu sehen:

Weils so selten ist (hab mit Schimmel einfach kaum Probleme) und einer gewissen Schönheit ja nicht entbehrt, grün-blauer Schimmel auf GT-"Sporenkeimschale":
Geschrieben von: hogie Dec 12 2015, 00:50

Diese Petri ist damit wohl raus. Ich weiß spontan aber auch nicht, was es genau ist. Viellicht ist es ja der Superschimmel, um den nächsten Käse damit zu beimpfen
Geschrieben von: Herr von Böde Dec 12 2015, 01:20
Die wäre raus, zum Glück eh nur ein Testlauf um meine Prints mal zu testen, könnte besser sein aber 2 von 3 Petris enthalten isolierbares Myzel, wie kontifrei die sind, vor allem in der oberen Petri weiss ich nicht was die gräulichen Buckelchen sind (spät keimendes Myzel oder monokariotes Myzel oder doch Hefen) werd noch abwarten.
Aber daraus wir nichts weiter, meine Kapazitäten sind ausgeschöpft, wollte ich jedes Myzel auf Substrat bringen--oh-oh ![]()


Hier nochmal der Test wie deutlich sich genetisch differente Myzelien abgrenzen, sind 3 Strains auf der Schale, auch mit dem Auge ehr entteuschend,zwischen den ersten beiden sich berührenden Myzelien keine klare Abgrenzung was bedeutet um zu checken ob Myzelien genetisch identisch sind taugt die Methode wohl nicht.
Aber mal noch 1-2 Wochen abwarten:
Geschrieben von: Herr von Böde Dec 13 2015, 02:35
Hatte heute alle Casings mal in der Hand, auch das Älteste, am 19.11. aus PF-original Substart gebastelt legt nun endlich mit der Fruchtung los.
Kein Casing das zwischen dem 23 und 29.11 (das Letzte)gebastelt wurde zeigt Anzeichen von Fruchtkörperbildung.
Seltsam irgendwie ![]()
Werd wohl zumEnde dieser Casings ein paar Substratgläser (B+ und GT1"Reste") zwischkühlen müssen, mir geht der Fruchtungsboxplatz aus ![]()
Beheizt wir der Inkubator seit 7 Tagen nicht mehr...
Geschrieben von: Herr von Böde Dec 14 2015, 00:03
Oben auf der Sporenkeimschale gezeigten grauen Buckelchen sind tatsächlich Myzel, war fast davon überzeugt es müsse sich um Kontis handeln:
Damit sollten meine Prints - zumindest für meine Zwecke- ausreichend gute Qualität haben ![]()
Dazu aber mal eine Frage: man kann kann doch wohl davon ausgehen das in den sichtbaren "Keimclustern" mehre Sporen die aneinander hafteten gekeimt sind und bereits großteils aus vereinigten dikarioten Myzelien bestehen oder?
Zur Isolation wäre also jetzt der beste Zeitpunkt, bevor die Cluster übereinanderwachsen?
Oder sind wahrscheinlich doch nur einzelne Sporen gekeimt?
Das würde Kreuzungsversuche natürlich viel einfacher machen als gedacht...
Edit 03:30
Soziemlich in allen Casings tut sich nun etwas, 3 vom 27 und 29.11 werden hoffentlich bis Mittwoch oder Donnerstag nachziehen:

Die PF-o Fruchtkörper unterscheiden sich morphologisch in diesem Stadium tatsächlich kaum von den GT. Die Hüte sind - so meine ich- etwas dunkler und haben auch den leicht rötlichen Stich auf den in manchen Beschreibungen des Strains hingewiesen wird:

Auch in diesen beiden Casings geht es los, wer Suchen möchte wird etwas finden ![]()


Geschrieben von: MarcusX Dec 14 2015, 15:48
Also ich seh einen :D
Geschrieben von: Herr von Böde Dec 14 2015, 16:38
Lol:

Geschrieben von: angel of death Dec 14 2015, 23:21
Finde es übrigens super dass du so ausführlich hier berichtest!
Meistens lese ich nur stumm mit, aber es ist immer cool zu sehen wie es voran geht, und es gibt nicht viele Leute die das so ausdauernd dokumentieren! :)
Geschrieben von: Herr von Böde Dec 15 2015, 01:04
Ich sollte hier vielleicht mal anmerken dass das alles natürlich ein Fake, eine schöne Geschichte ist.
Nicht das jemand ernsthaft meint ich betreibe evtl. illegale Hobbys ![]()
Geschrieben von: hogie Dec 15 2015, 02:08
Nicht das jemand ernsthaft meint ich betreibe evtl. illegale Hobbys
Geschrieben von: Herr von Böde Dec 15 2015, 03:32
Du magst keine Schlangen oder nicht die Haltung der selben?
Wenn Du das zweite meinst sei mal gesagt das fast nur noch Nachzuchten gehandelt werden. Verantwortungslose und unnötige Wildfänge lehne auch ich ab.
Grade die Nachzucht der Tiere - auch solcher die in freier Natur rar sind- ist Sinn meines Hobbys .
Berichte über böse Tierfänger und üble Importe sind ähnlich reisserisch wie Drogenreportagen, soetwas kommt vor aber kaum ein ernsthafter Terrarianer möchte geschwächte, parasitengeplagte Tiere die unbekannte Erreger in den Bestand einschleppen ![]()
Eine private tiergerchte Haltung der meisten Arten ist gut möglich. ![]()
Das ein 8m Python reticulatus nicht ins Kinderzimmer oder eine Studentenbude gehört ist klar, das auch soetwas vorkommt natürlich auch.
Das liegt dann aber nicht daran das die Tiergruppe zur Haltung prinzipiell ungeeignet ist sondern am Menschen der kein geeigneter Halter ist.
Hunde, Katzen und Fische - nicht zu vergessen die Millionen armen Goldhamster, vereinsamter und verhaltensgestörter Sittiche und andere Vögel in Minikäfigen !! werden ebenso schlecht von den entsprechenden Arschlöchern behandelt und gehalten.
Da pssieren eine Menge absoluter Wiederlichkeiten, oft auch aus mangeldem Wissen die darum nichtmal erkannt oder wahrgenommen oder vermutet werden. Der Terrarianer ist meist sehr gut über seine Pflegling informiert, mangelndes Wissen scheidet da schon mal aus.
Vor stumpfer Ignoranz ist natürlich kein Tier sicher.
Geschrieben von: Herr von Böde Dec 15 2015, 07:53
Abgesehen von all dem kann ich seit heute Morgen glaube ich deutlich erkennen das die PF-o Fruchtkörper um einiges zarter bleiben als die Golden Teacher es waren, die Hüte bleiben offenbar recht dunkel.
Ich denke morgen sind die ersten schon fertig:

Geschrieben von: MarcusX Dec 15 2015, 16:14
Ich kann angel of death nur recht geben. Wirklich ne super geschichte.
Hoff du machst weiter...
Vielleicht kommen ja noch n paar andere hauptdarsteller dazu :-)
Geschrieben von: Herr von Böde Dec 15 2015, 19:49
Lieben Dank für das Lob von Euch !!
Ich sehe keinen Grund das nicht zu tun (solange unliebsame Besucher, grüne oder blaue Männchen ![]() sich entfernt halten), einiges möchte ich ja schon noch testen.
sich entfernt halten), einiges möchte ich ja schon noch testen.
Zunchäst wird wohl mit reichlich vorahndenem Restmyzel ein wenig experimentiert, zB. das Stürzen perlit-bzw. bodenfreier Casings zum Cake und solche Dinge, wärend nebenher die Selektion jeweils einer neuen A+ und B+ Genetik läuft (diesmal noch ein wenig sorgfältiger, im Nachhinein bin ich von der Selektionsqualität meiner GT-1 und A+1 Genetik nicht mehr so überzeugt) um dann wieder auf das Thema "Schichtdicke" bzw. "Schichtverhältniss" im Casing zurückzukommen, dazu brauchts schon gut isolierte Genetik wenn man vergleichen will.
Sicher auch mal neue Cube-Strains, aber ausgeweitet werden soll zunächst mal in erster Linie auf Speisepilze (immer noch kein biologisches Material vorhanden, hatte die Suche zwischenzeitlich kurz mal verdrängt) und auf holzbewohnende Psilos .
Übrigens, der dickste A+ und 3 oder 4 PF-o wurden bereits heute Mittag mit eingerissenem Velum abgeerntet - und wenn ich mir das aus der Entfernung so anschaue sind gleich die nächsten PF-o (diese werden auch erstmal nur als Sporen eingelagert, die Kapazitäten x Strains gleichzeitig in Kultur zu haben sind nicht gegeben) dran.
Geschrieben von: MarcusX Dec 15 2015, 20:11
Mit gestürzten cakes hatt ich noch nie erfolg, bei mir können die über nen monat rumstehen ohne n ansatz von fk.
Ich hab noch nie ne bodenschicht bei casings gemacht, ich werds mal versuchen:-)
Auf nen bericht mit speisepilze bin ich gespannt:-)
Grüne männlein??? Akufolie soll helfen ![]()
Ist ja eh nur ne geschichte...
Off topic:
Wie läufts mit dem kampf gegen den nikotin?
Geschrieben von: Herr von Böde Dec 15 2015, 20:18
Der scheint- im Nachhinein überraschen einfach- bereits beendet
Stürzen würde ich die frühestens nach dem ersten Flush, damit das ganze fest genug ist und die Fruchtung ausreichend stabiel schon läuft.
Ich hatte vor einigen Wochen- als es noch deutlich wärmer war-mal ein altes Casing
(ohne Schale) in die Tonne geworfen, ca. 5 Tage später war es noch zu sehen und midestens 4 fröhlich vor sich hin sporuliernde FK erfreuten sich des Daseins (ja, in der sicher nicht sterielen Restmülltonne)
Geschrieben von: MarcusX Dec 15 2015, 20:54
Ja dann herzlichen glückwunsch ![]()
Ich werd im urlaub das thema jetzt richtig in angriff nehmen.
Ach, ich dacht du willst sturzgläßer nehmen und den inhalt stürzen.
Ja, das kenn ich.
Ich entsorg meine experimente im garten auf dem kompost. Da ist schon so viel gewachsen wo ich nie gedacht hätt das da überhaupt was passiert ![]()
Auch überall schnecken, vogelkacke und und und.
Interessant wie die natur das regelr...
Geschrieben von: Herr von Böde Dec 15 2015, 21:06
Nein, fertige Casings will ich stürzen, auf klassische PF-Cakes komm ich so schnell nicht wieder zurück ![]()
Geschrieben von: Herr von Böde Dec 15 2015, 22:41
So, tatsächlich waren die viel kleiner gebliebenden PF-o fertig, aus beiden - schon weiter Oben gezeigten - Casings ergaben sich zusammen 84 g.
Der zum Printen enthauptet goße Stiel rechts oben gehört zu einem A+

Die Huthaut sieht etwas samtig aus.
Starkes Blauen an einer "Amputationstelle", (hier wurde schon heut Morgen ein FK entfern) deutet darauf hin das Psilocybin/Psilocy da ist ![]()


Die A+ brauchen länger, werden aber deutlich größer:
Hier erkennt nun jeder die Pins:
Geschrieben von: Herr von Böde Dec 16 2015, 23:11
Beim Abschütten der gedunkten A+ und PF-o Heimchendosencasings drang mir grad ein verdächtig süß saurer Hefeduft in die Nase ![]()
Vielleicht erklärt das schon die lange Zeit bis zur Fruchtung und den für A+ recht geringen Ertrag im ersten Flush (55 ).
Hab sie mal noch nicht entsorgt.
Evtl. hab ich doch schneller wieder Platz in den Boxen als gedacht ![]()
Geschrieben von: Herr von Böde Dec 17 2015, 14:15
Auf jedenfall, das deutete sich bei den GT schon an, kann man sagen dass das Substratvolumen Auswirkung auf Anzahl und va. Größe der Fruchtkörper hat:
ca.1500ml Brut:
ca.760ml Brut:
ca.380ml Brut, nur 2 FK die aber groß werden:
Geschrieben von: Herr von Böde Dec 19 2015, 01:30
Viele PF-o. Fruchtkörper sind optisch vom Golden T. bestimmt nicht sicher zu unterscheiden.
In diesen beiden PF-o. Casings sehe ich keine Unterschiede zum Teacher:

Bestünd eigendlich Interesse an einer Zusammenfassung meiner bisherigen Vorghensweise?
Wäre aber evtl. etwas Arbeit und vieles ist überall nachzulesen.
Aber kein Problem wenn Interesse besteht.
Geschrieben von: MarcusX Dec 19 2015, 02:02
Ich hätt interesse:-)
Es ist bestimmt für anfänger nich eine bereicherung zu den schon bestehenden geschichten.
Hast du eigentlich kondenswasser in deinen petris?
Mich würd dein kda rezept interessieren wenn du es preisgeben willst:-)
Wie hast du das 1,5 liter casing gebadtelt?
Sind das mehrere gläßer zussmmen?
Hast du es sxhon mal mit nem bulk vesucht?
Grüße
Geschrieben von: Herr von Böde Dec 19 2015, 02:48
Ok, irgendwelche Rezepte geheim zu halten käme mir sicher nicht in den Sinn, heisse ich Coca-Cola ![]() ?
?
Rezepte gehörten natürlich zu der Zusammenfassung dazu, mit ein paar Erleuterungen. Ist aber kein Problem die schonmal hier -weitgehend unkommentiert- hineinzukopiern:
(Ich rühre immer 500 ml Agar, das dann auch sofort verwertet werden kann, an)
Kleine Anmerkung: die Rezepte zu verbessern steht noch nicht an, mir geht und ging es erstmaöl um andere Dinge, hier ist also nichts groß optimiert sondern blind übernommen, es funktioniert und das reicht erstmal- mehr Erklärungen dann in der Zusammenfassung)
Kartoffel-Dextrose-Agar (KDA)
---------------------------
300 g Kartoffeln (1 Stunde kochen in 2-3 L Wasser, nur die Brühe verwenden)
25 g Agar-Agar
12 g Dextrose (Traubenzucker)
0,1g Kalk = ca.2,5 Messerspitzen bzw. Mikrolöffel
0,1g Kaliumhydrogenphosphat (K 2 HP0 4 ) = ca.2,5 Messerspitzen bzw. Mikrolöffel
das Gemisch sollte 1 L Nährmedium ergeben
Kleinzerschnippelte Kartoffeln 1 h sprudeld kochen, ggf. mehr Wasser hinzuführen (angebranter Kartoffelmatsch im Topf verpesstet Dir für den Abend die Wohnung und das Topfschrubben ist eine wahre Freude ![]() - mit Waschpulver ggf. wiederholt einweichen kann Wunder bewirken
- mit Waschpulver ggf. wiederholt einweichen kann Wunder bewirken ![]() ).
).
Sud filtrieren und auf ca 900ml einkochen lassen.
Menge abmessen, und auf ca 1020 ml auffüllen (inzwischen nehm ich dafür destilliertes Wasser), aufkochen, restliche Zutaten einrühren, kochen bis alles gelöst, fertig.
Bier Agar
..........
500 ml Bier + 500 ml Wasser zum kochen bringen, auf ca. 400 ml reduzieren (zwecks Alkoholreduzierung), abmessen, auf 520ml auffüllen, aufkochen und die Zutaten:
2g Dextrose,
0,05 g Kaliumhydrogenphosphat
einrühren
12g Agar Agar einrühren
einrühren, deren Lösung abwarten, fertig
Ja, die großen Casings werden aus mehreren Gläsern mit selektiertem also identischem Myzel gebastelt.
Bulkversuche stehen weit hinten in der Liste.
Edit
ja Kondenswasser in den Petris kommt vor, wenn man die ideale Füllhöhe in den Petris findet kann man das etwas reduziern.
Aber auch wenn nicht, stört das gar nicht so sehr, die Schälchen werden onhein mit dem Deckel nach unten gelagert, ausserdem verschwindet es eigendlich immer nach spätestens 1 Woche.
Bildet sich sehr viel freies Wasser gibts beim Beimpfen die Möglichkeit schnell was abzukippen.
Geschrieben von: MarcusX Dec 19 2015, 03:00
Supe danke.
Ja topf schrubben ist scheiße.
Hab letztens milch snbrennen lassen und meine frau hat getobt:-)
Ich hsb neuerdings ein haufen kondenswaser in meinen petris und weiß nicht wsrum.
Hast du da keine probleme?
Läst du das medium komplett auskühlen bevor du die petrischale zumachst und sterilisierst?
Geschrieben von: Herr von Böde Dec 19 2015, 03:13
Hab dazu oben nochmal edetiert.
Temperaturschwankungen (Heizperiode ??), verändrte Füllhöhe der Petries, abgelagertes Agar oder zu wenig Agar fallen mir da bei plötzlichen Veränderungen bei dem Phänomen ein.
Manchmal ja, manchmal nein. Zu mach ich sie auf jedenfall sofort, im Sinne von Deckel drauf. Mir sind da noch keine Unterschiede bezüglich des Kondenswasser aufgefallen.
Ich würd wohl einfach 1g/500ml mehr Agar nehmen.
Bei Milch hast ja den ganzen Herd noch mitversaut,
da kommt Freude auf...
Geschrieben von: MarcusX Dec 19 2015, 12:35
Ok, hab bei wikibook gelesen das es das kondenswasser reduziert wenn man das medium erst vollständig auskühlen lässt.
Hat bei mir such super funktioniert bis aus die letzten 38 petris??!
Wickelst du alufolie um deine schalen und gläßer zum steriliesieren?
Was benutzt du für nen ddkt?
, oh ja, topf und hed haben ausgeschaut:D
Geschrieben von: Herr von Böde Dec 19 2015, 13:10
Ja klar Alufolie muss da schon drum rum, sonst hätte ich 99% Ausfälle durch Kontis.
Immer 6 Petris umwickelt, so kann ich gut 3x6 Petris pro Durchgang fertig machen.
Die Petris kühlen bei mir immer vollständig (über Nacht) im geschlossenem Topf aus.
Das ist ein einfacher Bratoni Schnellkochtopf 16,5 X 22(Dm) cm, ich glaub der kostete zwischen 30 und 35 ,-
Wie gesagt, Kondenswasser kommt schon vor aber in der Praxis stellt es kein Problem dar, was nicht beim Beimpfen abgekippt (so viel ist es allerdings selten) werden kann wird innerhalb einiger Tage vom Nährboden oder wachsenden Myzel absorbiert.
Temperaturschwankungen könnten das evtl. erschweren, die Temperatur in meinen Inkubatoren (eigentlich wird nur noch 1ner benuzt) schwankt um max 0,3 Grad C, sie liegt bei 28,3-28,6 Grad (wenn er eingeschaltet ist).
Edit
Ich hab übrigens gestern Abend noch welche sterelisiert, morgen erst komm ich zum Beimpfen. Solange bleiben die auch schön im Topf.
Kann gern mal Bilder machen, direkt nach dem Rausnehmen, nach dem Beimpfen und jeweils nach 3,6,9 Tagen da sollte ganz gut die Kondenswasserentwicklung zu erkennen sein.
Geschrieben von: hogie Dec 19 2015, 20:14
Periodische Temperaturänderungen sind die Ursache des Kondenswassers beim Lagern. Deshalb ist auch der Kühlschrank extrem schlecht für die Kondenswasserbildung. Denn beim Lagern stellt sich in der Petri eine RF von nahezu 100% ein. Sinkt die Temperatur dann nur geringfügig, erreicht man den Taupunkt und es fällt Wasser aus. Kondenswasser bildet sich immer zuerst an der kältesten Stelle und das ist beim Abkühlen naturgemäß der der Deckel der Petri, weil die Wärmekapazität am Boden größer ist. Schafft man es, dass der Deckel möglichst nicht die kälteste Stelle ist, dann ist das Kondenswasserproblem gelöst.
Geschrieben von: MarcusX Dec 20 2015, 00:10
@ herr von böde
Ja, bilder sind immer gu:-)
Ich vesichs mal mit mehr agar.
Ich hab dieses problem erst sit ich mein arbeitsbereich in ein zimmer im og verlegt hab. Ist mir noch nie so krass passiert mit dem ko denswasser.
@hogie
Dann dürftn js theoretisch nur die oberen petris das problem haben weil ja die deckel von den schalen darunter von dem medium darüber warm gehalten werden und somit gleichmäßig abkühlen oder hab ich ds jetzt n wurm drinn?
Geschrieben von: hogie Dec 20 2015, 01:52
Innerhalb der Petri hast du das Problem immer, dass der Nährboden mit viel Wasser eine extrem hohe Wärmekapazität hat und deshalb meist langsamer abkühlt, als der Rest.
Die Physik kann man nicht bescheißen. Aber es gibt mind. 1000 Möglichkeiten, das zumindest annähernd zu tun. Witzig sind auch Nährböden mit Gelrite statt Agar. Das ist ein Polysaccharid, das einmal ein Gel bildet und beim nächsten Erhitzen sich nicht wieder verflüssigt. Solche Petris kannst du z.B. auch auf dem Kopf autoklavieren.
Ich hatte jedenfalls niemals Probleme mit Kondenswasser in Petris.
Geschrieben von: Herr von Böde Dec 21 2015, 14:05
Die Kondenswasserentwicklung bei der jetzigen Charge zu dokumentieren fällt wohl flach, beim Beimpfen kein Wasser in Sicht ![]()
Mag auch daran liegen das die Petris 2 Tage im Topf bei 15 Grad standen und sich vor dem Beimpfen und Auspacken erst wieder aufwärmen durften.
Gut möglich das in 3 Tagen bei der ersten Kontrolle Kondenswasser zu sehen ist.
Geschrieben von: Herr von Böde Dec 22 2015, 14:23
So, 2 Petris mit Kondeswasser fanden sich heute:

Ich hab die mal zusammen gestellt und mach in Abständen von 3 Tagen nochmal Bilder.
Ausserdem, beimpfte und überlagerte Petris scheinen auch wieder zu Kondeswasserbildung zu neigen, diese Petri mit meinem Myzeltest war zwischenzeitlich frei von Kondenswasser.
Inzwischen zeigen sich halbwegs deutliche Abrgenzungen zwischen den 3 Myzelien, um aber ein Gefühl dafür zu bekommen was eine Abgrenzung ist und was nicht sind sicher mehrere Test von nöten, so eindeutig ist die Sache nicht.
Auf dem letzten Bild hab ich mal einen Bereich markiert auf dem Myzel wächst das ich keinem Impfpunkt zuordnen kann, vielleicht wärs interessant das zu isoliern und mal fruchten zu lassen ![]()



Geschrieben von: Herr von Böde Dec 25 2015, 18:21
Kurze dicke Fruchtkörper, so hatte ich die PF-o ursprünglich auch im Kopf:
Geschrieben von: Herr von Böde Dec 26 2015, 20:34
Wie ist denn soetwas zu erklären, keimfähige Hirse im Casing nach ca. 30 min köcheln + 100 min DDKT ??
Natürlich wird Hirse auch beim selbst zusammengemischten Mäusefutter verwendet aber ich wüsste keinen Weg wie die ins Casing hätte kommen sollen:
Es handelt sich um A+ Casing dessen 2ter Flush morgen fertig ist. Darum auch die beim ertsen Dunken vom Boden hochgespühlten Perlit"kügelchen" in der Deckschicht...
Edit:
Bevor ich es vergesse, schnell noch die Kondenswasserentwicklung.
Die selben Petris wie Oben mit Blitz und ohne Blitz.
Noch gibts keine Reduzierung des Wassers:



Geschrieben von: MarcusX Dec 27 2015, 11:30
Die pf o sehen richtig geil aus ![]()
Vielleicht hat die den Schäferhund geholfen wegen mikroklima ![]()
Bei meinen Petrus ist wesentlichmehr kKondenswasser, werden nächste Woche mal mit der agarmenge spielen.
Was bedeutet is?
Geschrieben von: Herr von Böde Dec 27 2015, 12:14
Die Sätze musst Du mir erklären
Also seit dem ersten PF-Cakediebstahl (siehe 1-3 Seite dieses Freds) stehen Inkubator und Casings für den Hund unerreibar. Sollte der also nicht nachts heimlich und unbemerkt Stühle rücken
Was bedeutet was??
Geschrieben von: MarcusX Dec 27 2015, 13:28
OK, dann kann man den Hund nicht fürs hirsesähen verantwortlich machen ![]()
Sorry, stand heut morgen etwas neben der kappe ![]()
![]()
Beim den Petris steht b+-iwas bedeutet is?
Geschrieben von: Herr von Böde Dec 27 2015, 15:09
lol, das ist nur ne Anmekrung für mich, die sinnvollerweise auf den Petris direkt vermerkt ist "is" für isoliert iGgs. zu - natürlich nach und nach, sobald die erste Fruchtung einsetzt, völlig wegfallenden - unmarkierten multi (Backup)Schalen.
Die Isolationsschritte an sich brauch ich ja nicht als Info auf der Petri.
Die selbe Info ist natürlich (bei kleiner Vorgehnsweise) auch im Impfdatum festgehalten aber "is" ist fürs Hirn ein schneller zu verarbeitender optischer Input , dessen Erstellung nur etwas Papier und Schwärze kostet
Geschrieben von: Herr von Böde Dec 29 2015, 17:25
Juchuh, endlich. Der die ersten Kräuterseitlinge (Pleurotus eryngi) konnten ergattert werden:
Sicher nicht der einfachste Speisepilz, zunächst will ich auch mal nur die Gentik auf Agar sichern, gleichzeitig eine gute Übung fürs Klonen (bei den Psilos ist mir bei den wenigen Versuchen noch keine Klonierung kontifrei gelungen) betimmt wandern auch ein paar Stücke testweise auf eingeweichte Buchenspäne.
Besteht Interesse an einem Thread oder zu unpassend fürs "Zauberpilzforum" ??
Geschrieben von: MarcusX Dec 30 2015, 00:16
Glückwunsch:-)
Von meiner seite aus besteht interesse:)
Ich hab meine zuerst auf pappe herangezogen, bin gespannt wie es läuft.
Geschrieben von: chronic Dec 30 2015, 00:31
Pleurotus eryngi ist wie alle Seitlinge total easy zu ziehen.
Geschrieben von: Herr von Böde Dec 30 2015, 00:35
Ok, guter Tip. Hab grad auch schon gelesendas dies (Pappe) wohl auch möglich ist.
Um die Gentik zu sichern wird auch das versucht, Impfstücke sollten da ja schpon ein paar rauskommen ![]()
Die Buchenpellets hab ich mal mit nem Beutel Reis und etwas Kleintierstreu vermischt (3 430ml Gläser Späne, 1 Beutel gekochter Reis, ne gute Handvoll Streu). dh. wegen dem Reis muss schon recht steriel gearbeitet werden und die Gläser werden ertst mit Agarmyzel beimpft.
Hoffe ich bekomm das Klonen kontifrei oder zumindest so kontiarm hin das sauberes Myzel überimpft werden kann. Hab mich für Bieragar entschieden, gegen 00:00 Uhr slollten die 10 Petries abgekühlt und bereit sein. ![]()
Geschrieben von: Herr von Böde Jan 5 2016, 12:33
Es sieht so aus als hätte ich wachsendes KS-Myzel ![]() , warum das Bieragar diesmal so dunkel wurde ist mir noch etwas schleierhaft:
, warum das Bieragar diesmal so dunkel wurde ist mir noch etwas schleierhaft:
Geschrieben von: hogie Jan 5 2016, 18:46
Geschrieben von: MarcusX Jan 5 2016, 19:31
Das wird schon, wenn ich so deine bisherigen erfolge anschau:-)
Hast du jetzt nur auf pwtri geforscht oder so auch ne kultur angelegt?
Hogie, macht es da dann sinn langsam die temperatur zu erhöhen?
Geschrieben von: hogie Jan 5 2016, 20:56
Geschrieben von: Herr von Böde Jan 6 2016, 03:00
Das Karamellisieren wirds wohl sein, beim Einkochen des mit Wasser aufgefüllten Bieres war ich mit der Temperatur nicht grad sachte.
Ich hab nur diese insgesamt 10 Klonkulturen auf Petrie und ein bissl was auf Pappe ( in 10 Ziptütchen-da zeigt sich aber noch nichts).
Die Tage kommt onehin ne größre Arbeit mit der glovelosen Glovebox, dann geht auch etwas auf das oben beschriebene Subsrat in Gläsern (das vorehr -wenn es gut riecht- nochmal in den DDKT wandert).
Geschrieben von: Herr von Böde Jan 9 2016, 13:00
Heute mal wieder gelauert und tatsächlich, sogar die völlig unsterile Pappe (nur zum Einweichen mit kochendem Wasser überspühlt) wird vom Seitlingmyzel überwuchert, damit allerdings getreide- (Reis) haltiges Subtrat zu beimpfen traue ich mich aber nicht ![]() Es gibt ja auch ausreichend steriles Agar aber entsorgt wird noch nichts, als Backup bleiben die Tütchen erstmal
Es gibt ja auch ausreichend steriles Agar aber entsorgt wird noch nichts, als Backup bleiben die Tütchen erstmal ![]()
Erstaunlich auf jedenfall das es 0 Ausfälle durch Kontis gibt, auf Agar ebensowenig wie auf Pappe - und das beim Klonen !! ![]()


Das macht Mut auf "Mykobags" komplett zu verzichten und eine größere Menge Holzschnipsel zB. im (frischen ![]() )Müllsack zu beimpfen wenn ein paar Brutgläser soweit sind...
)Müllsack zu beimpfen wenn ein paar Brutgläser soweit sind...
Geschrieben von: hogie Jan 9 2016, 17:42
So etwas gelingt schon hin und wieder. Doch gerade als Backup taugen die nicht viel. Denn klar ist, es sind genügend Kontaminanten am Start und wurden nur durch das aggressiv wachsende Mycel überwachsen. Wenn du es überimpfst, sind alle am Start und ob dein Mycel wieder gewinnt, wird immer unwahrscheinlicher. Unbedingt steril arbeiten so gut es nur geht. Denn die Rückschläge durch schludrige Arbeit lassen gewöhnlich nicht lange auf sich warten (in allen Bereichen) ![]()
Geschrieben von: Herr von Böde Jan 9 2016, 17:52
Naja mit "Backup" meine ich wirklich die letzte Reissleine.
Hab von den 10 Petris heute 8 -eigendlich gute- entsorgt (bzw. deren Inhalt), eine dient noch als bessers Backup, eine weitere wurde nochmal auf 6 Petris "verteilt" von denen dann endlich mal Brutsubstart beimpft wird.
Wenn diese 6 brauchbar sind werden die Pappen entsorgt.
Hab nur keine Lust nochmal wochenlang aus Seitlingsuche gehen zu müssen ![]()
Ne "schnöde" Auster konnte ich übrigens noch immer nicht auftreiben ![]()
Geschrieben von: hogie Jan 9 2016, 18:02
Geschrieben von: Herr von Böde Jan 9 2016, 21:22
Ja, ich finds fast schon unheimlich ![]() ich wohn nun echt nicht irgendwo im nirgendwo, 3 Supermärkte+2 Gemüsehändler und 1 Wochenmarkt in ähnlicher Reichweite wie bei Dir .
ich wohn nun echt nicht irgendwo im nirgendwo, 3 Supermärkte+2 Gemüsehändler und 1 Wochenmarkt in ähnlicher Reichweite wie bei Dir .
Statistischen Aussreiser erwischt... Nen Lottogewinn (ohne zu spielen ![]() ) wäre mir allerdings lieber.
) wäre mir allerdings lieber.
Aber natürlich klappere ich nicht täglich alles ab.
Wird schon noch klappen ![]()
Geschrieben von: Herr von Böde Jan 11 2016, 00:34
Schabenschmaus (Blaptica Dubia):
aufgebrochene Casings mit viel Myzel entsprechen wahrscheinlich viel mehr dem natürlichen Feuchtfutter als Apfel, Gurke, Spinat etc. der südamerikanischen Urwaldbewohner.
Solche Ansammlungen sind wirlich sonst nur bei Dunkelheit an anderem Feuchtfutter zu beobachten, hier stört nichtmal der Blitz ![]()


Geschrieben von: hogie Jan 11 2016, 00:50
Diese Viecher fressen einfach alles!
Geschrieben von: Herr von Böde Jan 11 2016, 02:45
Was wirklich nicht gern genommen wird sind Citrusfrüchte, die schaffen es als einzige Schimmel anzusetzen wenn es Alternativen gibt. Saures wird wohl nur genommen wenn der Wasserhaushalt nicht mehr optimal ist.
Ansonsten hast Du recht: von allem anderen bleibt nichts übrig ![]()
Die Casings werden aber eindeutig stark bevorzugt, nur (gepellte)Pellkartoffeln (die ohne Schale gekochten werden ohne eindeutige Begeisterung genommen) kommen da in etwa ran ![]()
Geschrieben von: Herr von Böde Jan 14 2016, 19:06
Spaßeshalber habe ich das schon lange vorbereitete Substat für die KS mal ohne Glovebox mit Myzelpappstücken beimpft. Das Substrat wird eh nicht besser und gegen ein paar Experimente spricht doch nichts. Es waren 4 Gläser, in einem zeigt sich grüner Schimmel (natürlich genau an den Reiskörneren) und wird nicht geöffnet bevor nicht ein paar ccm Klorix durchs Polyfil gedrückt wurden.
Bei 2 weiteren Gläsern ist ein bischen sich ausbreitendes Myzel zu erkenn, in einem Glas wächste es rapide schnell und deutlich erkennbar.
Sicher wird davon nichts ernsthaft verwendet aber das Myzel scheint deutlich aggressiver und wiederstandsfähiger, ausserdem (bei Zimmerteperatur 20-21 Grad) viel schneller wachsend als das der Cubensis.


Wohl auch zu sehen: Für dieses Substrat fehlt noch das Fingerspitzengefühl, es ist wohl sehr feucht geraten.
Noch ein Bild der frisch gereinigten und neu bestückten Fruchtungsbox, 2 A+ und 2 B+ Casings (vom 07.01).
Ich habe diesmal die Brut sehr lange durchwachsen lassen so das sich viel Myzel schon in den Gläsern entwickeln konnte, könnte mir Vorstellen dass das die Fruchtung etwas schneller in Gang kommen lässt.
Die "Schichtungsexperimente" gehen erst weiter wenn ich gut isolierte Genetik habe, bei den B+ dürfte das inzwischen der Fall sein, so das in 1-2 Wochen einiges an Roggen damit beimpft wird.
Geschrieben von: Herr von Böde Jan 15 2016, 20:21
Ich hab ja schon einiges über extreme Wartezeiten bei FSRE gelesen und möchte hier mal eine positive Rückmeldung geben, bin selbst ganz überrascht:
Hatte am 03. oder 04.01 3x3 Prints +5,- im Rückumschlag nach Eindhoven gesand, grade fand ich im Briefkasten den Rückumschlag mit 3 Prints, also 3 neu zu testen Strains (Amazonian, Equadore und RedBoy) über deren Qualität ich natürlich noch nichts sagen kann und für die FSRE natürlich auch nicht verantwortlich ist.
Also an dieser Stelle mal ein dickes DANKE an FSRE !!!
Geschrieben von: Herr von Böde Jan 18 2016, 11:29
Interessanterweise sehen die B+ Casings genauso so aus wie die allerersten A+ Casings, viele viel weisse Punkte die bald Fk werden wollen und das 11 Tage nach dem Casen. Wer genau schaut findet auf dem ersten Bild auch schon den ersten B+ Pin ![]()
Jenachdem wie schnell die A+ nun nachziehen scheint meine Vermutung das Brut die mehr Zeit hatte Myzel noch im Glas zu entwickeln (hier bestimmt 7 Tage länger als sonst, durchwachsen aussehnde Gläser wurden noch 1x geschüttelt und standen nach der Myzelerholung und erneuten "Durchweissung" nochmal 3-4 Tage) etwas schneller fruchtet, erstmal bestätigt.
Ob das über die gesamte Zeit ein Gewinn ist ist aber unklar, die Vermutung scheint aber berechtigt.
Oben die B+ Casings, unten die A+ :



In den unsteril beimpften KS-Gläsern war übrigens fast überall Schimmel zu erkennen, alle wurden entsorgt.
In 7-10 Tagen gibts eine größe Gloveboxaktion, dann gehts mit den Ks etwas ersthafter weiter. ![]()
Geschrieben von: Pachanoi Jan 18 2016, 13:28
Hey, falls du benötigst habe ich noch Körnerbrut und durchgewachsene Petrischalen mit Kräuterseitlingen.
Falls du Interesse hast kannst du mir da ja mal eine PN schreiben :)
Geschrieben von: Pachanoi Jan 18 2016, 13:28
-doppelpost dank IPad-
Geschrieben von: Pachanoi Jan 18 2016, 13:29
-dreifachpost, wo kann ich Beiträge löschen?-
Geschrieben von: Herr von Böde Jan 18 2016, 14:38
Danke für das Angebot, ich denke vom Ks hab ich jetzt aber genug brauchbares Myzel auf Agar.
Ich überleg grad nur ob ich tatsächlich erst Körnerbrut beimpfe oder direkt mit dem Agar auf Buchenholz+ etwas Kleintierstreu (ohne Getreide) gehe..
Geschrieben von: Waaagh Jan 18 2016, 14:44
Ich empfehle immer Flümy.
Scherbe mit reinpacken , durchschütteln und dann mit 50ml animpfen.
So sind selbst 1L Weckgläser oder große Bags über das Wochenende besiedelt
(man kann natürlich auch viel mehr zum animpfen nehmen, sollte nur sein Substrat nicht fluten).
Geschrieben von: Pachanoi Jan 18 2016, 15:29
Flümy habe ich bisher noch nicht benutzt, werde ich aber mal in Erwägung ziehen.
Hast du ein Link dazu für mich?
Btw Alles Gute dir waagh :)
Geschrieben von: Herr von Böde Jan 18 2016, 16:08
Stimmt Flümy wär hier tatsächlich einen Versuch wert. Und wird im Laufe des Abends angeszt ![]()
@Pachanoi: Für Flümy musst nur das Agar das ja nur dem Andicken dient weglassen, die flüssig bleibenden Nährlösungen sollten durchweg geignet sein.
Um möglichst klare Sicht zu haben würde ich aber Dextrose+H2O oder evtl. Malzextraktlösung oder Bier hernehmen.
Geschrieben von: Pachanoi Jan 18 2016, 17:30
Mein Nährmedium ist sowieso ein Malzextrakt.
Gut dann werde ich gleich mal zwei Glasflaschen mit der Lösung befüllen und etwas Mycel hinzufügen.
Ich hatte mit den Unicorn Bags bisher keine guten Ergebnisse, vielleicht ändert sich das dadurch ja.
Danke ![]()
Geschrieben von: Pachanoi Jan 18 2016, 18:42
Ich hoffe meine Glasflaschen kochen nicht über, sie sind in einem etwa 45' Winkel aufgestellt und sind mit 250ml gefüllt (750ml Gläser).
Da Malzextrakt mit Wasser gerne aufschäumt und mir deswegen schon einige Petrischalen versiegelt hat.
Habt ihr mit anderen Nährboden auch dasselbe Problem, oder gibt es bessere Alternativen?
Ich fülle meine Petrischalen z.b. mit nur 10ml MAE da es sonst zu sehr hochkocht beim autoklavieren.
Geschrieben von: Herr von Böde Jan 19 2016, 01:08
Ja, Bier muss eine Zeit gekocht werden bis es aufhört zu Schäumen.
Am einfachsten ist sicher eine etwa 3 %ige Dextroselösung.
Ausserdem wichtig : Vor dem Öffnen von Ventilen oder Deckel erst die Raumtemperatur erreichen zu lassen ![]()
Dann sollte nichts hochkochen .
Geschrieben von: Herr von Böde Jan 19 2016, 06:30
Viele viele B+ Pins, vielen Dank nochmal an den Sporenspender ![]()




Geschrieben von: Waaagh Jan 19 2016, 11:35
Also mein Standard Pilz Medium ist MEP
Für 1Liter dest. Wasser:
30g Malzextrakt
3g Sojapepton
pH auf 5.6 mit zb. HCL 3N einstellen
Für Platten noch 15g Agar hinzu.
Geschrieben von: Herr von Böde Jan 19 2016, 12:44
Oh oh, ich sehe schon das wird echt ne never ending story, nach den Schichtiungsexperimenten mit 3-4 Strains müssen dann wohl oder über mal Rezepte getestet werden.
Naja - zumindes die Agar- bzw. geriterezepte können wohl auch nebenher laufen da werden die Auswirkungen auf die Enderträge wohl so groß nicht sein und die Schichtungsexperimente nicht verfälschen.
Rezept dankend in die Liste aufgenommen ![]()
Mit Reformhaus-oder asiaagar braucht man übrigens gut die doppelte Menge, ich bekomm mit 13g 500ml fest.
Geschrieben von: Pachanoi Jan 19 2016, 13:12
Auf 1,1 Liter nehme ich 20gr Malzextrakt und 25gr Agar, ist das leichteste und günstigste in meinen Augen und MEA bietet ja alles an Nährstoffen für Bakterien, Hefen und Pilzen.
Geschrieben von: Herr von Böde Jan 19 2016, 13:15
Ich wechsel derzeit von Durchgang zu Durchgang zwischen KDA und Bieragar .
Beides funktioniert gut aber ohne Frage gibt es Optimierungspotenzial ![]()
Geschrieben von: Waaagh Jan 19 2016, 18:52
Also ich kann dir gern ein paar komplexere Nährmedien geben wenn du magst.
Dann musst du mir aber sagen für welchen Pilz , und was du dir unter Optimierung vorstellst.
Für mich ist zb ein Verzicht auf das Komplexmedium , und ein Rezept mit getrennter Zugabe der benötigten Salze ; Spurenelemente und Vitamine eine Verbesserung.
Da weißt du auf jeden Fall was du hast.
Nehme ich praktisch im Labor allerhöchstens für ganz anspruchsvolle Mykorrhiza Pilze, bei benötigten definierten Experimenten wie zb Fütterungsexperimenten.
Oder um schlecht auskeimende Sporen zu pushen, gesammelte Fruchtkörper aus dem Wald anzusetzen etc.
Eine Zugabe von Antibiotika die Bakterienwachstum hemmen wäre auch eine schöne Optimierung ![]()
Geschrieben von: hogie Jan 19 2016, 23:13
Ich habe dafür noch etwas Gentamicinsulfat im Kühlschrank. Das bietet sich für Nährböden geradezu an, um bakteriell kontaminierte Kulturen sauber zu bekommen, weil es im Gegensatz zu dein meisten übrigen Antibiotika problemlos autoklavierbar ist.
Geschrieben von: Herr von Böde Jan 20 2016, 01:23
Also Optimierungen würden für mich in erste Linie die Besiedelungszeit betreffen (in beide Richtungen, schnelle Besiedlung für direkt weiterzuverwendende Myzelien soweiee langsame Besiedlungszeit für Myzelien die evtl. als Backup eingelagert werden), ebenso wichtig ist die kontiunabhängige allgemeine Vitalität die auch eine schnelle Umgewhönung bzw. Erholung nach der Brutbeimpfung ans neue Substrat und einen gewissen "Überalterungsschutz" oder zumindest eine nicht geförderte Überalterung, bedeuten könnte.
Ausserdem ist gute Sichtbarkeit bzw. Entdeckbarkeit von Kontis keine schlechte Eigenschaft (da wäre Hogies Gelrite sicher optimal).
Auf Antibiose kann ich evtl. komplett verzichten, es geht allein um die Optimierung der Cubensiskultur, also so immens wertvolles Myzel habe ich nicht.
Evtl. macht es natürlich trotzdem Sinn isolierte Genetik von Zeit zu Zeit über ein solches Medium zu reinigen aber nur wenn sie onehin ehr langfristig gebraucht werden kann.
Ich habe noch Golden Teacher (GT-1) und A+ (A+1) Genetik die wenig jünger sind als dieser Thread, bei den letzten Casings hatte ich bereits das Gefühl das es schon deutlich nachliess- was natürlich auch ganz andere Ursachen haben kann -zB. bakterielle Kontis.
Reinigung würde sich evtl. lohnen wenn solche Genetik über 1-2 Jahre stabiel bleiben würde, kann ich aber onehin nur 2-4 "Casinggenerationen" mit Cubemyzel durchziehen bevor neue Genetik her muss lohnt das Reingen ehr nicht.
Darum hier nochmal die Frage: Wie lange -so etwa- kann eine isolierte, saubere Cubegentik verwendet werden ?
Edit
Und bei der Gelegenheit fällt mir noch eine Frage -für Waaagh bestimmt beantwortbar- ein:
Wie wahrscheinlich ist es mit der Klonierung eines FK aus einer Multikultur schon isolierte Genetik zu bekommen wenn ich aus dem Hut klone (also mit viel Abstand zur Casingoberfläche) ? Es soll ja Fks geben die sich aus unterschiedlichen Myzelien zusammensetzen. Ist das ehr die Regel oder eine seltene Ausnahme?
Geschrieben von: Pachanoi Jan 20 2016, 07:49
Wenn du das Wachstum von dem Mycel eindämmen oder "stoppen" möchtest und es als Backup dienen soll, dann Lager die Petris oder die Körnerbrut etc. doch einfach im Kühlschrank, so ist das Wachstum stark eingedämmt.
Ich habe so seit 3 Monaten 15 Petrischalen eingelagert und keine von denen zeigt bemerkbaren Wachstum des mycels.
Geschrieben von: Herr von Böde Jan 20 2016, 08:12
Jo, das ist klar das solches Myzel nicht im laufenden Inkubator gelagert wird ![]() aber ein dazu passendes Agar das nicht auf Powerwuchs sonderen auf Erhaltung abgestimmt ist wäre natürlich trozdem eine Optimierung, schon allein der durch die verstreichende Einlagerungszeit erhöten Kontigefahr wegen die durch nährstoffärmeres Agar evtl. ein wenig eingedämmt werden könnte
aber ein dazu passendes Agar das nicht auf Powerwuchs sonderen auf Erhaltung abgestimmt ist wäre natürlich trozdem eine Optimierung, schon allein der durch die verstreichende Einlagerungszeit erhöten Kontigefahr wegen die durch nährstoffärmeres Agar evtl. ein wenig eingedämmt werden könnte ![]()
Bei anstehnden Tests hätte ich die Nährlösungen einfach mal auf 1/2 - 1/4 verdünnt oder aus dem KDA mal KA gemacht aber wenns spezielle Rezepte gibt : her damit ![]()
Geschrieben von: Pachanoi Jan 20 2016, 10:11
Naja du musst dabei beachten das die Bakterien dann zwar nicht sich in dem Maße vermehren werden, aber genausowenig wird dein Mycel wachsen.
Bakterien können sich auch auf den nährstoffärmsten Substraten vermehren, da wo dein Mycel schon garnicht mehr wachsen würde.
Daher halte ich die Idee für etwas sinnlos, nicht böse gemeint.
Wenn du eine Petrischale die gut gewachsen ist und vor allem ohne sichtbare Kontis ist, einfach in den Kühlschrank stellst, sollte nach einem Jahr dort auch nichts anderes gewachsen sein, ich glaube vorher würde das Agar austrocknen.
Meine Petrischalen die ich nicht beimpft habe und als Test normal verschlossen habe, hatten alle keine Konti und auch nach 4 Monaten bei 20 grad noch immer keine.
Die waren alle mit Parafilm verschlossen und meine, die ich im Kühlschrank einlager, sind zusätzlich mit Alufolie umwickelt, hat auch den Grund, das kein Licht auf das Mycel trifft.
Geschrieben von: Herr von Böde Jan 20 2016, 10:16
...
Geanau das will ich ja darum versteh ich nun nicht warum dir das sinnlos erscheint
Geschrieben von: Pachanoi Jan 20 2016, 10:23
Oh okay, naja die Bakterien wachsen bei nährstoffreichen Substrat sehr gut genauso wie das Mycel.
Bei nährstoffärmeren Substrat wächst es weniger gut, genauso wie das Mycel.
Man kann es in etwa im Verhältnis sehen, als großes Manko kommt hinzu, das Bakterien auf jedem Substrat wächst wo auch nur ansatzweise Nährstoffe sind.
Ich bin nicht so sehr in der Bakterien-Materie drinne, aber vllt weiß jemand etwas anderes.
In Meinen Augen ist es egal welches Substrat du hast, es sei denn es ist mit Antibiotika versetzt, es wachsen kontis, sobald du eine hast, wie weit diese wachsen ist natürlich abhängig von der Konkurrenz Vorort also dem Mycel (oder evtl andere Kontis) und sie wachsen solange weiter bis die Nährstoffe aufgebraucht sind oder die maximal Masse entstanden ist, d.h. Es entstehen genausoviele Bakterien wie welche sterben.
Geschrieben von: Pachanoi Jan 20 2016, 10:26
Wenn du ein Backup hast solltest du also einfach nur drauf achten, das keine Konti dabei ist, denn Bakterien wachsen erst dann nicht mehr, wenn die Nährstoffe verbraucht sind oder wenn die Umgebung das nicht zulässt (Temperatur oder Stoffe wie Antibiotika)
Gehst du dabei davon aus eine Konti zu haben, sollte dies nicht mehr als Backup eingelagert werden.
Geschrieben von: Herr von Böde Jan 20 2016, 10:40
Du hast immer den einen oder andern Fremdkeim absolute Sterilität gibts vielleicht auf dem Mond aber bestimmt in keinem Nähragar, schon gar nicht in mit Haushalttechnik hergestelltem und dann noch mehr oder weniger provisorisch beimpftem. ![]()
Ausserdem sollte man die Mobilität solcher Keime vielleicht nicht unterschätzen, was beim Einlagern topp war kann nach 6-12 Monaten auch bei vernünftiger Abdichtung eingewanderte Fremdkeime enthalten.
Darum denke ich schon das es Sinn macht das Wachstum dieser Fremdkeime bei einzulagernden Backups nicht nur von der Temperatur sondern auch von der Nährstoffseite her zu hemmen.
Und ganz unabhängig von der Keimfrage meine ich irgendwo aufgeschnappt zu haben das va. Dextrose bzw.insgesammt ein hohes Nährstoffangebot die zelluläre Alterung eines Myzels beschleunigt, darum macht es sicher auch Sinn die Nährstoffe zu reduzieren wenn onehin eine monatelange Einlagerung geplant ist.
Geschrieben von: Pachanoi Jan 20 2016, 10:58
Ja aber du hemmst das Mycel doch auch, das bringt dir doch nichts, die Bakterien stehen doch dennoch sozusagen im selben Verhältnis wenn welche vorhanden sind.
Nehmen wir an du hast durch nährstoffärmeren Substrat eine Myceleffizenz oder Produktivität von 30%,
Dann ist doch die Produktivität der Bakterien dementsprechend gehemmt, dass der Peak der Kolonialisation schon nach kürzerer Zeit erreicht ist und die Höchstmaße der Bakterien dann auch nur noch bei nehmen wir an 30% liegt.
Dennoch macht es sogesehen keinen Unterschied zu 100%iges Substrat.
Du kannst natürlich spezielle Nährstoffe nur noch benutzen, die nur auf dein Mycel ansprechen, aber auf diese Nährstoffe sprechen zu 100% auch andere Bakterien, die du dann mit Glück nicht dabei hast.
Ich hoffe du verstehst meinen Gedankenverlauf, aber warte am besten auf eine andere Meinung, ich will meine Meinung nicht unbedingt zu 100% vertreten.
Das zu den Bakterien, über die Mycelalterung weiß ich leider nicht viel.
Geschrieben von: Herr von Böde Jan 20 2016, 11:07
Lol, in meinem Backup brauche ich 0 Myzelwachstum-ein wenig wird es natürlich wachsen - es soll nur die Lagerung überleben.
Die Bakterien werden trotzdem wachsen je langsamer desto besser - oder??
Ich gehe davon aus das ja klar ist das ich mit dem Backup nach der Einlagerung nicht direkt Brutsubstrat beimpfe sondern das Myzel zunächst mal auf anderes Agar bringe um es in Schwung zu bringen, es beurteilen zu können, nicht zulezt um genug Material zu bekommen.
Ja ich glaube ich verste Deinen Gedankenverlauf mir wird nur nicht klar warum Dir dabei kein Licht aufgeht ![]() ...nicht böse gemeint !
...nicht böse gemeint !
Geschrieben von: Pachanoi Jan 20 2016, 11:18
Alles gut ich nehm nichts böse, ist doch schön eine Diskussion zu haben ![]()
Wenn das Myzelwachstum 0 ist, wird es nach und nachsterben, dann wären die Nährstoffe sogesehen bzw einer der Nährstoffe nicht mehr ausreichend vorhanden und du bewirkst einen Rückgang des mycels.
Und hier kommt in meinen Augen der springende Punkt und zwar die Konkurrenzfähigkeit zu den Bakterien ist so nicht mehr gegeben, da Bakterien jetzt den Bereich leichter besiedeln können, wo das Mycel sein Wachstum eingestellt hat oder sogar zurückgegangen ist.
Ich verstehe auch was du meinst, aber das Problem der Bakterien bleibt dasselbe.
Ich würde auch als Backup ein nährstoffreicheres Medium dennoch bevorzugen, umso vitaler ist das Mycel und wenn du es dann Kühl lagerst "stagniert" ( eher gehemmt ) es so gesehen, wie die Bakterien auch.
Wundert euch nicht bei Mycel oder Myzel, das sucht mein IPad sich wahllos aus. ![]()
Geschrieben von: Herr von Böde Jan 20 2016, 11:26
Ok, wenn die Fremdkeimbelastung so hoch ist das ernstliche Konkurrenz zum Zielmyzel entsteht, ja dann habe ich tatsächlich eine kontaminierte Petri die zur Einlagerung nicht geeignet war.
In einer kontifreien (so wie wir es verstehen) Petri sollte es natürlich soweit nicht kommen, es geht nur darum das bakterielle Wachstum so weit auszubremsen das ich nach der Einlagerung sauber überimpfen kann.
Notwendigerweise wächst das Zielmyzel, einfach weil es ja lebt aber eben doch in sehr überschaubarem Maße, gefragt ist das Wachstum nicht und sollte auch nicht nötig sein um Fremdkeime in Schach zu halten.
Geschrieben von: Pachanoi Jan 20 2016, 11:37
In meinen Augen entsteht bei jedem Vorhandensein von Bakterien eine Konkurrenzfähigkeit zu dem Mycel, Bakterien sind nunmal überlebenskünstler und es bremst die Bakterien sogesehen nicht, die maximale Kolonialisierung ist nur früher erreicht, sogesehen ist die Petri trotzdem komplett bedeckt, ansonsten hat man Nährstofffreie stellen.
Hat Waaagh nicht iwas mit Mikrobiologie zutun ?
Der kann uns ja dann bestimmt aufklären in der Hinsicht.
Geschrieben von: Pachanoi Jan 20 2016, 11:38
-doppelpost-
Geschrieben von: Herr von Böde Jan 20 2016, 11:43
Dann würde uns Amateuren sicher keine Pilzzucht gelingen. Potentielle Konkurrenzfähigkeit - ja, tatsächliche Konkurrenz - nein, ist zu verhindern.
Wenn das Zielmyzel quasie stagniert ist jeder Potenzierungsfaktor mit der sich Fremdkeime langsamer vermehren ein echter Gewinn und Nährstoffreduzierung dürfte schon ein bisschen was aus machen.
Bin aber auch gespannt auf Waaaghs Meinung
Geschrieben von: Pachanoi Jan 20 2016, 11:53
Ich versteh deinen Standpunkt ja komplett, ergibt ja auch alles Sinn, nur bin ich von meinem überzeugter, da wir nicht aus Erfahrung sprechen können, müssen wir abwarten bis jemand sich meldet, der sich mit dem Thema besser auskennt.
Ich lasse mich immer gern eines besseren belehren . ![]()
Geschrieben von: Pachanoi Jan 20 2016, 12:01
Was anderes, mein Flümy ist rostbraun geworden, habe es wahrscheinlich zulange sterilisiert, dadurch ist der Zucker kristallisiert, sieht also echt Scheisse aus.
Ich werde am Wochenende wohl weitere Flaschen sterilisieren, man will ja auch noch was erkennen können.
Ist mir tatsächlich mit dem MEA noch nie passiert.
Beimpft habe ich die Flaschen trotzdem, schauen wir mal in 1-2 Wochen ob sich da was tut und was sich da tut. ![]()
Geschrieben von: Herr von Böde Jan 20 2016, 12:18
Ich bin noch nicht dazu gekommen, habe immer ne 3%ige Dextroselöung genommen, ca. 200ml 30 min sterilisiert, langt dicke.
Noch nen Tip: wenn Du in einem normalem Schraubglas arbeitest macht es Sinn den Deck-Glasrand vorher mit Silikon zu versiegeln (ganz normaler Aquariensilikon hält das aus), ohne Unterdruck im Glas sind die oft nicht wirklich luftdicht und auch kein Polyfil zur belüftung nehmen sondern 2 Silikonports in den Deckel kleben, dann eine dicht mit Polifyl und anschliessender Aluschicht umantelte Kanüle durch reicht für den Luftaustausch (beim Entnehmen wir Luft nachgesaugt).
Sei froh das Du ne Reinbank hast ![]()
Geschrieben von: Pachanoi Jan 20 2016, 12:56
Nené, die Reinbank steht erst in 1-2 Monaten, ich kauf mir nach und nach die Komponenten zusammen, jetzt fehlt der Hepa, sind nochmal knapp 250€ und hat zudem eine Lieferzeit von 20 Tagen.
Ich habe Malzextrakt aufgekocht abgefüllt und den Deckel leicht zugeschraubt mit Alufolie umwickelt und dann in den Autoklaven gestellt.
Ich hab die Flaschen blöderweise mit heißem Malzextrakt für 50 Minuten in den Autoklav gestellt und bis zum nächsten Tag dort drinnen auskühlen lassen, kurz beimpft, zugemacht und noch einmal mit Frischhaltefolie großzügig umwickelt.
War leider zulange, da die Flüssigkeit noch um die 70 grad hatte, sonst lasse ich sie auch nur 20-30 Minuten sterilisieren.
Geschrieben von: Waaagh Jan 20 2016, 14:43
Oki, viele Punkte auf einmal.
Ich versuch mich kurz zu halten:
-Genetik immer selektieren, d.h besonders rhizomorphe Stellen ausschneiden und auf eine neue Petri legen, das ruhig 3-4 mal machen bis der Strain nicht mehr "flauschig" wächst.
Hier kannst du mM nach die meiste Optimierung herausholen
-Verhindern der Degeneration der Genetik, wichtig hier einfach nicht immer im Kreislauf verkehren also nicht nur Sporen-animpfen-FK ernten und wieder damit die nächsten animpfen.
-Lieber immer auf den selektierten Strain zurückgreifen, möglich über Flümy oder Petris
-Eigene Klone herstellen :
Also für das Verständnis , du arbeitest hier mit Dikaryon Stämmen.
Das heißt mehrere Kerne im Mycel, Sporen (ein Kern) keimen aus ,wachsen zueinander und werden zum Dikaryon.
Also am Besten Stück Trama nehmen , auf den Deckel der Petri kleben und Sporen fallen lassen.
Oder Sporenabdruck gut verdünnen, ausplattieren.
2 Einzelkolonien nehmen (Monokaryon) ausschneiden, selektieren und zusammen auf einer Platte Dikaryon bilden lassen. Logisch hast du dann nur diese beiden Kerne im Dikaryon
Hat also nicht mit Mycelsträngen im Hut zu tun etc.
-Für Lagerung von Kulturen einfach normales Medium herstellen, mit winzigen Stück Mycel beimpfen , kurz anwachsen lassen und dann ab in den Kühlschrank.
Sollte locker ein Jahr vital sein.
So ich hoffe ich habe alles beantwortet.
Geschrieben von: Herr von Böde Jan 20 2016, 15:26
Ok, leider nicht so ganz die Fragen getroffen. ![]()
Der Aufbau bzw. die Entwicklungstadien von Myzel ist mir schon klar. Sporen bilden monokariotisches Myzel welches sich zu dikayotischem - fruchtbarem- Myzel vereinigt.
Dieses kann selektiert werden um isolierte Genetik zu gewinnen.
Ein Weg ist der über die Selektion von Petris - und dem Überimpfen kleiner geignet erscheinende Myzelstücke - darin hab ich inzwischen Übung ![]()
Aber, Deine Ausführungen werfen gleich eine neue Frage auf:
Wie gewinne ich monokariotes Myzel und va. halte es in dem Zustand, genau das brauche ich ja wenn ich verschiedene Strains mal kreuzen will ??
Du hattest da so selbstverständlich von geschrieben als wärs ein Kinderspiel ![]()
Ich denke mal dazu brauchts geignetes optisches Werkzeug- Mikroskope ?
Was brauch ich da?
Eine Frage war nun wie lange eine solche Genetik die ja auf viele Petris verteilt werden kann tauglich bleibt.
Also, ich habe vom Teacher und vom A+ gut selektierte Genetik, nämlich die GT1 und A+1 auf einigen Petris. Natürlich beimpfe ich Körnersubstrat immer mit Stücken von diesen Petris. Meine Erfahrung war nun das nach 3-4 Monaten, etwa 3 oder 4 Casinggenerationen (mit Generationen meine ich Casings bzw. die Brut dafür die in Abständen von Wochen mit dieser Genetik von Petris beimpft wurden) schon deutlich an Vitalität verlieren - was natürlich andere Gründe als das Alter haben kann.
Also kann ich mit isolierter Cubegenetik tatsächlich nur so kurz arbeiten oder kann ich tatsächlich über 1-2 Jahre immer neue Petris und Körnersubstart mit dieser Genetik beimpfen?
Die Frage nach dem FK-Klon war evtl. nicht gut gestellt, ich weiss nicht mehr wo, aber irgendwo las ich das einzelne Fruchtkörper die aus einer Multimyzelkultur - also nicht einer isolierten Gentik- hervorgehen durchaus aus mehren dikarioten Myzelien bestehen können und das ein einzelner Klonvorgang deshalb nicht garantiert schon isolierte singuläre Gentig selektiert zu haben.
Also, habe ich da etwas falsch verstanden, ist das extrem selten oder sogar die Regel ?
Es wäre ja praktischer einen Print zum Keimen und zur Fruchtung zu bringen und dann eben das zu klonen was gut mit den angebotenen Bedingungen zurecht kommt und man spart sich Isolationsschritte, der Klon müsste nur noch auf mehrere Petris verteilt werden.
Müsste man aber das Klonmyzel tatsächlich erst noch weiter selektieren verliert man natürlich nur Zeit.
Geschrieben von: Waaagh Jan 20 2016, 17:03
Für Monokaryen wiegesagt einfach etwas Lamellentrama , zb eine Lamelle an den Deckel der Petrischale kleben. Zb mit etwas parafin etc.
Deckel zu, und warten bis die Sporen fallen, beziehungsweise einfach stark verdünnte Sporenlösung herstellen.
Du brauchst kein Mikroskop, Lupe wäre für den Anfang ganz hilfreich.
Dann nimmst du die auskeimende Spore und selektierst sie auf eine neue Platte.
Das ganze mehrmals machen, und schon hast du diverse Monokaryen. Ohne zweiten Pilz kann kein Dikaryon entstehen.
Sicher sein kannst du dir, wenn sie richtig beschissen langsam wachsen.
Monokaryen sind nämlich ganz schöne Weicheier.
Und produzieren auch nichts an Psilocybin ![]()
So muss jetzt erstmal wieder ins Labor, der Schuh drückt.
Geschrieben von: Herr von Böde Jan 21 2016, 08:52
Supi danke !
Werd das bei Zeiten mal testen ![]()
Noch ein paar Worte zur Myzelselektion aus geklonten FK bzw. zu den ominösen Fk die aus verschiedenen dikarioten Myzelien bestehn und ein paar weitere Verständnissfragen die seit Beginn des ganzen Projekts unklar blieben sind beantwortet ![]()
Die 4 Casings sehen gut aus es sind übrigens die ersten die komplett ohne Perliteboden gebastelt wurden, dh ich muss mit der Feuchtigkeit etwas vorsichtiger sein.

Auch die A+ (nicht die A+1 sondern unselektierte bzw. nur vorselektierte Genetik) legen erkennbar los:

Geschrieben von: Waaagh Jan 21 2016, 12:18
Puh also zu den Genetikfragen, also ich würde einfach den selektierten Strain erhalten.
Das heißt du nimmst du hast ein Backup mit Petris, von dem du animpst immer.
Und das musst du einfach versuchen immer mal neu anzuimpfen und vital zu halten.
Sieht man ja eigentlich ganz gut.
Ich würde einfach nur Multisporegrows vermeiden.
Und zur Grundlage nochmal , ein Dikaryon hat 2 haploide Kerne, die sich beide bei Zellteilung mitteilen. Du wirst also in deinem Mycel nur diese 2 Kerne finden. 
Nach Verschmelzen der beiden Kerne in der Basidie, folgt die Meiose
Die 4 haploide Kerne erzeugt, welche sich zu Basidiosporen entwickeln.
Also wenn du mit 2 monokaryen anfängst, werden immer nur die beiden Kerne zu finden sein.
Anders natürlich in den Sporen nach der Meiose (Crossing Over zb.)
Aber wenn die Wichtel einmal wachsen, was willst du da noch optimieren.
Mit 4 Casings solltest du doch mehr als versorgt sein.
Im übrigen finde ich das letze Casing etwas flauschig, und hätte spontan gesagt es ist zu lange durchwachsen.
Für gewöhnlich fruchte ich recht schnell nachdem sich das erste Mycel gleichmäßig durch die Deckschicht arbeitet.
Geschrieben von: Herr von Böde Jan 21 2016, 13:34
Lol, ja bei den max. 10-12g die ich derzeit alle 4 Wochen verbrauche bin ich in der Tat mehr als versorgt.
Wie an andrerer Stelle schon erwähnt enden wohl 95% der Erträge als Schabenfutter oder schlich im Müll / Kompost (die Mäuse bekommen nichts mehr, höchstens alte Casings ![]() ).
).
Mir geht es schlicht ums Experiment und das Verbessern der Methode.
Also mehr potenter Ertag in kürzest möglicher Zeit.
Just for fun, nicht für die tägliche Pilzmahlzeit ![]()
(Ich halte auch Ameisen, Vogelspinnen, Schlangen und Geckos dazu diverse Futtertiere - also wer nicht verstehen kann das Pilzkultur einfach Spaß machen kann - mir machen manch komisch erscheinende Dinge nunmal Spaß ![]() )
)
Diese Casings wurden am 07.01. gebastelt und gingen am 13.01 in die Fruchtung (also Deckel ab + Umzug vom Inkubator in die Fruchtungsbox), das Bild wie sie da aussahen ist weiter oben zu finden (S.16) ![]()
Im Vergleich zum vorherigen Durchgang habe ich viel viel weniger Overlay (da mussten teilw. 2-3 mal neu Abgedeckt werden) , ausserdem eine zuverlässigere, schnelle Fruchtung und führe das grad darauf zurück das ich die Gläser habe etwas länger durchwachsen lassen (kein Platz in den Fruchtungsboxen) also mehr Myzelbildung zugelassen habe als zuvor.
Als Laie hätte ich die Flauschigkeit im unteren Casing auf unzureichende Selektion zurückgeführt, gedacht das da einfach eine "flauschige Genetik" mitspielt.
Die beiden unteren Casings stammen von der selben Petrie (2ter Selektionsschritt) und sind auch exakt gleich alt und gleich beahndelt worden.
Wie gesagt die Genetik der Ständerpilze ist mir nicht ganz unbekannt.
Was mir noch immer nicht klar ist ist ob Fruchtkörper aus mehreren dikarioten Myzelien zusammengesetzt sein können, wenn sie nicht aus einer Kultur mit isolierter Genetik entspringen, ob das häufig oder ehr eine Ausnahme ist. Das ist die Frage ![]()
Wie gesagt, mir gehts ums Experimentieren, darum werden auch sicher Fruchtkörper aus solch unselektierter Kutur geklont werden, hilfreich wäre das Wissen ob ich mit solcher Klonung dann schon isolierte Genetik habe oder ob die Wahrscheinlichkeit hoch ist doch mehrere dikariote Myzelien in dem Fk-Stückchen zu haben.
Geschrieben von: Pachanoi Jan 21 2016, 15:40
Monokaryote bilden kein Psilocybin aus, dein FK, wird das wohl enthalten also ist er dikaryot.
Ich kenn mich nicht so sehr damit aus, aber würde nach Waaagh dann ja so sein?
Hab mir jetzt erstmal ein Buch dazu bestellt, damit ich etwas tiefer im Thema bin.
Hab dir auch ne PN geschickt HvB, vielleicht hast du ja auch Interesse daran :)
LG
Geschrieben von: Herr von Böde Jan 21 2016, 16:19
Lol, drücke ich mich denn so schwer verständlich aus ??
Selbstverständlich enthält der FK kein monokariotes Myzel die Frage ist ob er zwangsläufig aus nur einem dikariotem Myzel besthet oder ob an seiner Bildung auch 2 oder noch mehr dikariote Myzelien beteiligt sein können.
Es geht doch um die Selektion einer isolierten dikarioten (fruchtbaren) Genetik, habe ich die also gesichert vor mir wenn ich einen Fk aus Multisporenkultur - oder gar einen wild wachsenden- klone ??
Das es keinen Sinn macht einen FK der onhehin schon aus selektierter (auf Petri) Genetik enstand ist ja klar.
Huch sorry, hatte die PN gestern gelesen ... und dann vergessen. Danke für den Tipp aber, wie gesagt diese Grundlagen sind mir allesamt bekannt nur das ich irgendwo las das an der Bildung einzelner Fruchtkörper durchaus mehr als nur ein "geschlechtsreifes" Dikarion beteiligt sein kann, ich find aber die Quelle nicht mehr und die Frage bleibt offen.
Geschrieben von: Waaagh Jan 21 2016, 16:41
Also dann nochmal :
2 Monokaryen werden zum Dikaryon und machen Fruchtkörper.
Wenn du Fruchtkörper siehst haben sie immer nur 2 Kerne,
Ausnahmen sollten einige Ascomyceten sein wo Trikaryophasen vorkommen.
Anderer Fruchtkörper, andere Kerne.
Bei Multisporegrows kannst du also schon unterschiedliche Genetik in verschiedenen FK haben.
Geschrieben von: Herr von Böde Jan 21 2016, 16:55
Danke !!
OK, pro Zelle habe ich 2 Kerne und der Zellverband im Fk besteht aus identischen Zellen.
Supi, das wollte ich wissen.
Das ich beim Mukltisporengrow eben Fk mit jeweils unterschiedlichem Genom bekommen kann macht ihn ja garda interessant.
Geschrieben von: Pachanoi Jan 21 2016, 20:03
Sorry, nein eigentlich nicht, ich habe es wohl falsch verstanden. ![]()
Geschrieben von: Herr von Böde Jan 21 2016, 20:45
![]() kP
kP
Geschrieben von: Herr von Böde Jan 23 2016, 06:41
Der erste B+ ist fertig, alles andere wächst halbwegs homogen:




Geschrieben von: Pachanoi Jan 23 2016, 13:15
Ist der eine b+ FK so riesig oder die anderen so klein? ![]()
Sieht ja aus wie ein Mammutbaum unter den Cubensis ![]()
Bei meinem Flümy bildet sich schon ein kleiner Flaum um das Mycel, scheint zu funktionieren, sobald ich ein Bild machen kann, sodass man das Mycel auch erkennt, stell ich es rein ![]()
Geschrieben von: Herr von Böde Jan 23 2016, 14:08
Ja, das wirkt so. Sicher kein Rekordpilz vielleicht 10- 12g frisch (hab ihn nicht gewogen).
Der war auch schon ein richtiger Fk als alle anderen noch weisse Pünktchen waren ![]() :
:
und 1nen Tag später
Vom Wuchs her vergleichbar mit mittelgroßen A+, etwas dicker vielleicht.
Sind aber auch nur Minicasings mit evt. 370-max.400 ml Roggen/SiFu-brut.
Bin gepannt wie die sich in voluminöseren Casings machen. ![]()
Geschrieben von: Pachanoi Jan 23 2016, 14:16
Ja das würde mich auch interessieren, soll ja angeblich der größte Strain sein.
Interessant wäre hier der Unterschied zum Kompostsubstrat.
Kompost soll ja Wachstum von bis zu 30cm hervorbringen.
Freu mich schon auf weitere Bilder ! :)
Geschrieben von: Herr von Böde Jan 23 2016, 14:29
Bis jetzt ist ein Teacher mit einer Frischmasse von 38 g der Rekordhalter
(im 3ten Flush glaub ich sogar), der Wuchs auf ca. 1500ml Roggenbrut in einer 2,5l Eisdose ![]() .
.
Aber ein ähnlich großert FK (36 g Teacher oder PF.o) wuchs einzeln auf einem wegen massivem Overlay schon afgegebenen Minicasing n max. 480 ml inkl Brut und Casingschichten.
Geschrieben von: Pachanoi Jan 23 2016, 14:54
Ja den habe ich gesehen, 38gr frisch ist schon was ![]()
Wenn du 1500ml Körnerbrut hast, hast du diese vorher noch "zerbröselt" oder war es schon so in der Form gewachsen, dass es in die Eisdose gepasst hat?
Meine KS-Substrat-Blöcke habe ich vorhin auf meinen Pilz-Abfall-Kompost geworfen, hab keine Fruchtungskammer zurzeit und die Luft im Fruchtungsraum ist zurzeit einfach zu trocken, so habe ich dieses Jahr ein Paar KS im Garten wachsen ![]()
Geschrieben von: Herr von Böde Jan 23 2016, 15:04
Ja klar wurde das zerbröselt. Die Dose hätt ich nicht mit den Körnern sterilisiren können.
Kann auch sein das es nur 1200 ml Brut waren.
Jedenfalls der Inhalt aus 3-4 435ml Gläsern mit Brut- vorher isoliertes Myzel von einer Petri natürlich.
Geschrieben von: Pachanoi Jan 23 2016, 17:27
Okay,
Ich hab auch mit "hart" Plastikboxen schlechte Erfahrungen gemacht.
Ich hatte mir mal diese steri-PP-Boxen gekauft, die Pilzgrowboxen die man aus den typischen Shops kennt für 1l Inhalt glaube ich.
Sollten eigentlich sterilisierbar sein.
Ich habe so einige davon in meinem Autoklav bei niedrigstem Druck (1-1,5 bar, entspricht da 124 Grad) schmelzen lassen, ich hatte mir gedacht, dass ich so die wiederverwenden kann, haben auch 1,4€/Box gekostet.
Die PP-Beutel, Unicorn Bags sind, wenn sie in Aluminiumfolie eingewickelt sind, mir hingegen nie geschmolzen und erfüllen ihren Zweck, ich werde demnächst auch einen mal wiederverwenden um zu schauen ob das klappt.(50bags für 20€;
1kg trocken Roggen, bzw 1,8kg gekochter Roggen passen da bestens rein, sollte bis 2,5/3kg feucht aber auch reichen)
Geschrieben von: Herr von Böde Jan 23 2016, 17:43
Ja, die Beutel sind schon klasse wenn man sie dicht bekommt ![]()
Ausserdem wäre damit Flümy fast Pflicht wenn man steriel beimpfen will und dem trau ich ohne Hepa nicht so recht.
Naja spätestens wenn ich bei den Seitlingen ohne Beutel nicht mehr kontifrei weiterkomme muss ich mich damit nochmal auseinandersetzen.
Bisher - auf die Psilos bezogen- gehts sehr gut ohne und das Vermischen von Brut aus verschiedenen Gläsern scheint kein Problem zu sein wenn vernünftig isoliert wurde und man nur ein Myzel hat, Kontis gabs dadurch schon gar nicht wobei das Risiko natürlich steigt wenn da mal ein übersehenes "faules Glas" dabei ist. Aber damit könnte ich leben.
Du wickelst die in Alu ein...gute Idee. Das hatte ich bei den Bags noch nicht probiert und mir beim Verschliessversuch mit Heisskleber (der unter Druck bei deutlich unter 180 Grad klebrig wird !!!) den halben Topf versaut ![]()
Edit
Boah, ich stell gard fest das der "Cubinkubator" extreme Temperaturschwankungen aufweist (max 46,8 Grad C, min 15,4 Grad C) noch sieht alles lebendig aus aber sehr unterschiedlich bewachsen die Schälchen vom 14.01 (darum wirds nicht am Thermometer liegen ![]() )
)
Ich werd wohl Montag das isolierte B+ Myzel welches jetzt eigendlich auf Körner gehen sollte nochmal überimpfen bevor Brut besiedelt wird ![]() Wenn ich Pech hab sind viele Keime reingesaugt worden durch die Temperaturschwankungen
Wenn ich Pech hab sind viele Keime reingesaugt worden durch die Temperaturschwankungen ![]()
Geschrieben von: hogie Jan 23 2016, 18:13
Ausserdem wäre damit Flümy fast Pflicht wenn man steriel beimpfen will und dem trau ich ohne Hepa nicht so recht.
Die unicorn-Bags sind klasse, an einem ordentlichen Schweißgerät führt aber kein Weg vorbei. Von Flüssigmycel halte ich nichts. Außerdem bewachsen die großen Bags viel zu langsam, wenn nicht genügend Imfstellen da sind. Du brauchst einen Hepa von der Größe, dass du die Bags steril befüllen kannst und verschweißen kannst. Pilzfarmen machen das imho genauso und vermischen bereits durchwachsene Brut mit dem sterilen Substrat, füllen es dann in die Bags. So macht es dann wohl richtig Spaß.
Sehr billiges Getreidesubstrat für Speisepilze ist Futtergerste. Die ist aber ziemlich schmutzig und stellt erhöhte Anforderungen an die Sterilisation. Die Gefahr, Luftnester nicht richtig herausgespült zu bekommen ist bei den Bags groß. Sicher geht das nur mit angepassten Vakuumphasen. Der Feldautoklav eignet sich vorzüglich dafür, zumindest am Anfang eine gründliche Vakuumphase zu machen. Wenn mal Dampf in den Bags muss man vorsichtig sein, dass sie nicht platzen.
Geschrieben von: Pachanoi Jan 23 2016, 19:08
Ja meine Unicorn Bags verschweiße ich mit dem schweißgerät, das bei Lidl im Angebot war, Silvercrest für 20€.
Sehr zuverlässig bisher und auch eine ordentliche Schweißnaht. Ich verschweiße sie dennoch doppelt.
@hogie warum hältst du von Flümy nichts? Ist mein erstes Mal, das ich Flümy angesetzt habe.
Das Problem mit den Impfstellen hatte ich auch anfangs, jetzt wird mehr besiedeltes Agar in den Beutel geimpft und ordentlich durchgeschüttelt.
Geimpft über Sporen wird bei mir ja eigentlich nicht.
@HvB ich verschweiße meine Beutel erst nach dem sterilisieren, wenn sich die Beutel im Autoklav aufblasen würden, würden diese Platzen oder an heißen stellen aufschmelzen und mir mein Autoklav einsauen...
Aber ich vakuumisiere sie auch beim verschweißen ein wenig um evtl Keime mit raussaugen zu können, falls vorhanden.
Ich freue mich auch schon auf meine Reinbank, die werde ich hier auch mal vorstellen sobald sie fertig ist. :)
Geschrieben von: Herr von Böde Jan 23 2016, 20:19
Hm, 20-30,- fürn Schweissgerät sollten schon drin sein, hatte da ehr den 10fachen Preis im Kopf. Und da wär die Hepaanlage dann schon ehr angesagt (auch wenn ich nicht so recht weiss wo ich die noch aufbauen soll. ![]()
Läuft das mit Netzstrom? Wier dick ist die Naht?
Also mit dem Heisskleber hatte ich die Beutel schon dicht (blos eben nicht nur die Beutel...).
Geplatzt war da nichts, wenn auch bedenklich aufgebläht.
Bei langsamer Temperaturerhöung- und reduzierung sollte der Mikrofliter schon für Druckausgleich sorgen.
Flümy hat halt das Problem das Kontis schwer zu erkennen und unmöglich zu beseitigen sind. (Darum hatte ich auch geschrieben das ich mich da ohne Hepa nicht mehr so recht rantraue). Ausserdem muss man bedenken das es zusätzliche Feuchtigkeit ins Substrat bringt.
Für Seitlinge die auch ohne Getreide auskommen sollte das aber ganz gut funktionieren, Hefen - mein großes Problem- sollten da nicht so große Chancen haben.
Es ist sicher viel geeigneter als Myzelstücke um große Substratmengen zu beimpfen, aber man kann halt auch viele Körner damit versauen.
Geschrieben von: hogie Jan 23 2016, 20:36
Sehr zuverlässig bisher und auch eine ordentliche Schweißnaht. Ich verschweiße sie dennoch doppelt.
@hogie warum hältst du von Flümy nichts? Ist mein erstes Mal, das ich Flümy angesetzt habe.
Yep. mindestens 2mm Nahtbreite und ordentlich Power für die dicken Folien ist zwingend nötig. Dass das ein 20 Euro-Gerät packt, halte ich für unwahrscheinlich.
Ein qualitativ brauchbares Flüssigmycel herzustellen, ist aufwändig. Auf jeden Fall musst du mit bereits selektierter Genetik steril beimpfen und dann in einem autoklavierbaren Blender mixen, dass keine störenden Mycelquallen deine Kanülen verstopfen. Eine sterile Werkbank ist unabdingbar.
Nach der Sterilisation die Bags zu verschließen, ist eine elementare Schwachstelle, es sei denn dein Hepa ist so groß, dass auch der Autoklav hinein passt. Wenn man keinen hohen Durchsatz braucht, einfach langsam abkühlen lassen, auf keinen Fall den Druck weg nehmen oder gegen Ende mit Überdruck beaufschlagen (Druckluft oder Stickstoff).
Geschrieben von: Pachanoi Jan 23 2016, 20:46
Läuft mit Netzstrom, die Naht ist ca 3mm Dick, schätze ich. Sieht auch richtig schön fest aus.
Ja die Hepaanlage wird mich im Endeffekt 450€ Kosten, ist dann aber auch was für die Ewigkeit.
Aber auch ohne Hepa und selbst ohne Glovebox ist es gut möglich ohne Kontis, Pilze zu kultivieren. Ich habe momentan keine Glovebox mehr und somit meine Sachen alle rel. Unsteril beimpft, man muss nur einige bedenkliche Faktoren beseitigen oder eindämmen, so arbeite ich nur mit sterilen Und desinfizierten Sachen und die Luft über der Arbeitsfläche wird mit Wasser eingesprüht um Partikel durch die Wassertropfen zu binden. Und alles was in Kontakt kommt natürlich auch desinfiziert.
Naja ich werde es schon sehen, habe nicht allzu große Probleme beim beimpfen gehabt und ansonsten ist es Lehrgeld und man ist um eine Erfahrung reicher ![]()
An sich ist Flümy in meinen Augen eine sehr praktische Beimpfungs Möglichkeit, nur ob es praktisch alles gut verläuft werde ich schauen müssen.
Mein Flümy hier einmal, die Partikel die dort rumschwimmen müssten kristallisierter Zucker sein, so war die Flüssigkeit nach dem sterilisieren, kann aber auch wo ich gerade nachdenke vielleicht teilweise die Dichtung des Aluminiumsdeckels sein...
Zu erkennen ist etwas mycelflaum um die Agarplatte, scheint normal zu sein oder?
Geschrieben von: hogie Jan 23 2016, 20:52
Das mit der Ewigkeit ist gar nicht so einfach. Denn du musst sicherstellen, dass der Hepa nicht auf die Reinraumseite durchwachsen werden kann.
Geschrieben von: Herr von Böde Jan 23 2016, 20:55
Wenn das kristallisierter Zucker wäre hättest Du eine dickflüssige, gesättigte Zuckerlösung und eindeutig zuviel Zucker ![]()
Das sind wohl ehr Carbonate die beim Erhitzen von Leitungswasser ausfällen (wobei das ganzschön viel ist).
Das Agarstück ist riesig, viel Angriffsfläche für Kontis ich hatte immer ne Nadelspitze Myzel oder ein Körnchen Brut zum Flümybeimpen genommen, das langt schon.
Aber vielleicht läufts ja astrein, bin gespannt ![]()
Geschrieben von: Pachanoi Jan 23 2016, 20:55
Ich verstehe leider nicht was du meinst hogie.
Zu der Naht, ich bin selbst überrascht das so ein Lidl Angebot in der Preisklasse so klasse Arbeit leistet, die Naht ist doch 2mm dick.
Danke HvB, mir wurde zur damaligen Zeit gesagt das dass kristallisierter Zucker im Agar wäre, aber es sind sehr wahrscheinlich Carbonate aus dem Leitungswasser, das benutze ich immer zum aufkochen. Ergibt auch mehr Sinn. ![]()
Ja schauen wir mal, ist halt das erste Mal, wird schon schief gehen ![]()
Geschrieben von: hogie Jan 23 2016, 21:35
Nimm nächstes Mal einfach demin. Wasser.
Was genau hast du nicht verstanden?
Powered by Invision Power Board ()
© Invision Power Services ()
